Щелочную реакцию имеют химические разрыхлители теста (сода, карбонат аммония) и изделия, приготовленные с их применением (печенье, пряники).Общую щелочность определяют и рассчитывают так же, как и общую кислотность, но для титрования применяют 0,1н раствор соляной или серной кислоты.
Порядок выполнения работы
Порядок определения общей (титруемой) кислотности
Сущность метода:
Метод основан на титровании исследуемого раствора раствором 0,1моль/дм3 щелочи в присутствии индикатора фенолфталеина.
Проведение испытания
Навеску измельченной пробы мучных кулинарных, мучных кондитерских, булочных изделий (25г), взвешенную с точностью 0,01г, без потерь переносят в коническую колбу 250см3. Затем к навеске добавляют всю воду (250см3), нагретую до 60-70°C, и встряхивают жидкость 3 мин., после чего оставляют колбу на 1 мин. Отстоявшийся жидкий слой фильтруют в стакан или коническую колбу через вату, марлю или фильтровальную бумагу. Затем в две конические колбы отмеривают пипеткой по 50см3 фильтрата. К полученному фильтрату (болтушке) добавляют 2-3 капли спиртового раствора фенолфталеина и титруют 0,1 моль/дм3 (0,1н) раствором щелочи до слабо-розового окрашивания, не исчезающего в течение 1 мин.
Навеску (5г) из муки (дрожжевое или дрожжевое слоеное тесто) помещают в ступку и растирают с 50см3 воды до образования однородной массы. Болтушку переносят в сухую коническую колбу. К полученному фильтрату (болтушке) добавляют 2-3 капли спиртового раствора фенолфталеина и титруют 0,1 моль/дм3 (0,1н) раствором щелочи до слабо-розового окрашивания, не исчезающего в течение 1 мин.
Навеску творожных полуфабрикатов и кулинарных изделий (5г) отвешивают в стеклянный стакан, добавляют 50см3 воды, нагретой до 35-40°C, и тщательно растирают стеклянной палочкой с резиновым наконечником. К полученному фильтрату (болтушке) добавляют 2-3 капли спиртового раствора фенолфталеина и титруют 0,1 моль/дм3 (0,1н) раствором щелочи до слабо-розового окрашивания, не исчезающего в течение 1 мин.
Напитки и сиропы фильтруют. Затем в три конические колбы вместимостью 250см3 мерным цилиндром наливают по 100см3 дистиллированной воды, освобожденной от двуокиси углерода. От средней пробы напитка отбирают пипеткой по 10см3 в каждую из колб (темноокрашенные напитки берут в количестве 5см3). Сиропы отбирают пипеткой по 2см3 в колбы с 200см3 дистиллированной воды. К полученным фильтратам (болтушкам) добавляют 2 - 3 капли спиртового раствора фенолфталеина и титруют 0,1 моль/дм3 (0,1н) раствором щелочи до слабо-розового окрашивания, не исчезающего в течение 1 мин.
Одну из колб с напитком, разведенным водой, используют при титровании для сравнения окраски титруемого раствора с первоначальной.
Интенсивно окрашенные фильтраты титруют, используя в качестве индикатора спиртовой раствор тимолфталеина. Конец титрования устанавливают по появлению синей окраски, не исчезающей в течение 1 мин.
Можно титровать окрашенные фильтраты, применяя в качестве индикаторов синюю лакмусовую бумагу. По мере титрования капли титруемой жидкости наносят при помощи стеклянной палочки на полоску лакмусовой бумаги. Титруют до исчезновения покраснения. Чтобы лучше уловить исчезновение красной окраски на лакмусовой бумаге, следует под конец титрования рядом с каплей испытуемой жидкости нанести каплю дистиллированной воды для сравнения и заканчивать титрование, когда не будет заметно разницы в оттенках двух капель.
Проводят не менее двух параллельных определений.
Кислотность булочных, мучных кондитерских и кулинарных изделий (Х, град.) рассчитывают по формуле:
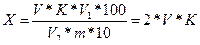
где:
К - поправочный коэффициент гидроксида натрия или калия концентрацией 0,1 моль/дм3;
V - объем раствора гидроксида натрия или калия, израсходованный на титрование, см3;
V1 - объем дистиллированной воды, взятый для растворения навески, см3;
100 - коэффициент пересчета на 100 г продукта;
V2 - объем фильтрата, взятый для титрования, см3;
m - масса навески, г;
10 - коэффициент перерасчета раствора гидроксида натрия или калия концентрации 0,1 моль/дм3 в 1 моль/дм3.
Допустимое расхождение между результатами параллельных определений не должно превышать 0,2°. За конечный результат принимают среднее арифметическое двух параллельных определений, вычисленное с точностью до 0,1°.
Если кислотность требуется выразить в процентах какой-либо кислоты, то градусы кислотности умножают на соответствующий миллиэквивалент, который равен для кислот: уксусной - 0,060; молочной - 0,090; яблочной - 0,067; лимонной - 0,070; винной - 0,075.
Кислотность (Х, град) полуфабрикатов из муки (теста) рассчитывают по формуле:

где
2 - коэффициент для пересчета результатов титрования в градусы.
К - поправочный коэффициент гидроксида натрия или калия концентрацией 0,1 моль/дм3;
V - объем раствора гидроксида натрия или калия, израсходованный на титрование, см3;
Кислотность (0Т) творожных полуфабрикатов (изделий) рассчитывают по формуле:

где:
20 - коэффициент пересчета результатов титрования в градусы Тернера;
К - поправочный коэффициент гидроксида натрия или калия концентрацией 0,1 моль/дм3;
V - объем раствора гидроксида натрия или калия, израсходованный на титрование, см3;
Расхождение между результатами параллельных определений не должно превышать 2°Т. За конечный результат анализа принимают среднее арифметическое, вычисленное с точностью до 0,1°.
Кислотность напитков и сиропов (Х, %) в расчете на преобладающую кислоту вычисляют по формуле:


где:
V – объем титрованного раствора гидроокиси натрия, израсходованного на титрование, см3;
с – молярная концентрация титрованного раствора гидроокиси натрия, моль/дм3;
m – масса навески, г.;
М – молярная масса, г/моль, равная для:
Яблочной кислоты М(½С4Н6О5) – 67,0
Винной кислоты М(½С4Н6О6) – 75,0
Лимонной кислоты моногидрата М(⅓С6Н8О7*Н2О) – 70,0
Уксусной кислоты М(С2Н4О2)– 60,0
Щавелевой кислоты М(½С2Н2О4) – 45,0
Молочной кислоты М (С3Н6О3)– 90,1
V0 – объем, до которого доведена навеска, см3;
V1 – объем фильтрата, взятого для титрования, см3
За окончательный результат испытания принимают среднее арифметическое результатов двух параллельных определения, относительное расхождение между которыми не должно превышать 5% (Р=0,95). Результаты округляют до первого десятичного знака.
Порядок определения активной кислотности
Сущность метода:
Метод основан на измерении разности потенциалов между думя электродами (измерительным и электродом сравнения), погруженным в исследуемую пробу. Определяют активную кислотность электрометрически с помощью pH-метров разных марок
Проведение испытаний:
Подготовка прибора:
Электроды рН-метра хранят в условиях, оговоренных в нормативно-технической документации по эксплуатации прибора. Перед каждым проведением испытаний электроды тщательно промывают дистиллированной водой. После исследования продуктов, содержащих жир, электроды очищают ватным тампоном, смоченным этиловым спиртом, насыщенным водой, и этиловым спиртом.
Перед проведением испытаний осуществляют проверку прибора в соответствие с нормативно-технической документацией по эксплуатации прибора по стандартным буферным растворам.
Подготовка проб.
Бульоны фильтруют через бумажный складчатый фильтр в сухую колбу.
Из натуральных мясных полуфабрикатов готовят водную вытяжку. Для этого из разных мест исследуемого образца мяса (без жира и соединительной ткани) отбирают навеску массой 10г, измельчают и помещают в коническую колбу вместимостью 250см3. Затем в колбу наливают 100см3 предварительно прокипяченной и охлажденной дистиллированной воды и настаивают мясо в течение 15 мин., периодически встряхивая колбу. Полученную вытяжку фильтруют через бумажный складчатый фильтр в сухую колбу.
Проведение испытаний
Из подготовленной пробы отбирают в стакан продукт в количестве, достаточном для погружения электродов. Для проведения испытаний продуктов твердой или очень густой консистенции подготовленную пробу продукта предварительно разбавляют примерно в 2 раза дистиллированной водой. В консервах, имеющих твердую и жидкую фазы, допускается проводить определение рН непосредственно в жидкой части продукта.
При использовании прибора, не обеспеченной системой термокомпенсации, температура пробы должна быть 20±20С
Концы электродов погружают в исследуемый продукт и после того, как показания прибора примут установившееся значение, отсчитывают величину рН.
За окончательный результат принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не должно превышать 0,1 (Р=0,90).
Порядок определения щелочности
Содержание щелочей регламентируется в песочном тесте, выпеченных из него полуфабрикатах для тортов и пирожных, а также других мучных изделиях, изготовляемых с применением химических разрыхлителей.
Сущность метода:
Определение щелочности методом титрования основано на нейтрализации щелочных веществ, содержащихся в навеске, кислотой в присутствии бромтимолового синего до появления желтой окраски. Выражают щелочность в градусах. За градусы титруемой щелочности принимают количество кубических сантиметров раствора соляной кислоты (серной кислоты) концентрацией 1 моль/дм3 (1н), необходимое для нейтрализации щелочных веществ, содержащихся в 100 г продукта.
Проведение испытаний.
Навеску измельченной пробы (25г), взвешенную с точностью до 0,01г, помещают без потерь в сухую бутылку (типа молочной) вместимостью 500см3, вливают 250см3 дистиллированной воды, закрывают пробкой и тщательно перемешивают взбалтыванием. Содержимое колбы оставляют на 30 мин., взбалтывая каждые 10 мин., затем фильтруют через вату, или два слоя марли, или фильтровальную бумагу в сухую колбу или стакан. Пипеткой вносят 50см3 фильтрата в коническую колбу вместимостью 250см3, прибавляют 2 - 3 капли бромтимолового синего и титруют 0,1моль/дм3 раствором серной или соляной кислоты до появления желтого окрашивания.
Щелочность Х (в градусах) вычисляют по формуле:
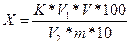
где:
К - поправочный коэффициент 0,1 моль/дм3 раствора соляной или серной кислоты, использованного для титрования;
V - объем раствора серной или соляной кислоты, израсходованный на титрование, см3;
V1 - объем дистиллированной воды, взятый для растворения навески, см3;
100 - коэффициент перерасчета на 100 г продукта;
V2 - объем фильтрата, взятый для титрования, см3;
m - масса навески, г;
10 - коэффициент пересчета 0,1 моль/дм3 раствора серной или соляной кислоты в 1 моль/дм3.
Щелочность вычисляют с точностью до 0,1 градуса. Расхождения между параллельными определениями, выполненными в одной лаборатории, не должны превышать 0,2 град., выполненных в разных лабораториях - 0,3 градуса.
Контрольные вопросы
- С чем связана кислотность продуктов питания?
- Источники пищевых кислот, разновидности пищевых кислот?
- Влияние пищевых кислот на качество пищевых продуктов?
- Методы определения кислотности?
- Что такое активная кислотность?
- Что такое общая (титруемая) кислотность?
- В каких случаях определяют щелочность, сущность метода определения щелочности?
Лабораторная работа № 11
МЕТОДЫ ОПРЕДЕЛЕНИЯ ПОВАРЕННОЙ СОЛИ
Цель: овладение методами количественного определения поваренной соли в сырье и в продуктах питания и проведение сравнительного анализа полученных данных
Задание:
1. Определить содержание поваренной соли в представленных образцах сырья и пищевых продуктов различными количественными методами.
2. Провести математическую обработку полученных данных.
3. Провести сравнительный анализ полученных данных, представленных в виде сводной таблицы.
4. Сделать заключение о проделанной работе.
Теоретические сведения
В приготовлении пищи поваренная соль употребляется как важная приправа. Соль имеет хорошо знакомый каждому человеку характерный вкус, без которого пища кажется пресной. Такая особенность соли обусловлена физиологией человека, но люди зачастую потребляют соли больше, чем необходимо для физиологических процессов.
В пищевой промышленности и кулинарии используют хлорид натрия, чистота которого должна быть не менее 97 %. Его применяют как вкусовую добавку и для консервирования пищевых продуктов. Такой хлорид натрия имеет товарное название поваренная соль, порой также употребляются названия пищевая, столовая, а также уточнение названия в зависимости от её происхождения — каменная, морская, и по составу добавок — йодированная, фторированная и т. д. Такая соль является кристаллическим сыпучим продуктом с солёным вкусом без привкуса, без запаха (за исключением йодированной соли), в котором не допускаются посторонние примеси, не связанные с методом добывании соли. Кроме хлорида натрия, поваренная соль содержит небольшое количество солей кальция, магния, калия, которые придают ей гигроскопичности и жёсткости. Чем меньше этих примесей в соли, тем выше её качество.
Выделяют сорта: экстра, высший, первый и второй. Массовая доля хлористого натрия в сортах,%:
· экстра — не менее 99,5;
· высший — 98,2;
· первый — 97,5;
· второй — 97,0.
Массовая доля влаги в выварочной соли сорта «экстра» 0,1 %, в высшем сорте — 0,7 %. Допускают добавки йодида калия (йодистого калия), йодата калия, фторидов калия и натрия. Массовая доля йода должна составлять (40,0 ± 15,0) × 10 −4 %, фтора (25,0 ± 5,0) × 10 −3 %. Цвет экстра и высшего сортов — белый, однако для первого и второго допускается серый, желтоватый, розовый и голубоватый оттенки в зависимости от происхождения соли. Пищевую поваренную соль производят молотой и сеяной. По размеру зёрен молотую соль подразделяют на номера: 0, 1, 2, 3. Чем больше номер, тем больше зерна соли.
В кулинарии хлорид натрия потребляют как важнейшую приправу. Соль имеет характерный вкус, без которого пища кажется человеку пресной. Такая особенность соли обусловлена физиологией человека. Однако зачастую люди потребляют соли больше, чем нужно для физиологических процессов.
Хлорид натрия имеет слабые антисептические свойства — 10-15 % содержание соли предотвращает размножение гнилостных бактерий. Этот факт обусловливает её широкое применение как консерванта.
Порядок выполнения работы
Порядок определение поваренной соли аргентометрическим методом (метод Мора)
Сущность метода:
Метод основан на титровании хлоридов в нейтральной среде раствором нитрата серебра в присутствии индикатора хромата калия.
В нейтральных растворах азотнокислое серебро образует с хлористым натрием белый осадок хлористого серебра, а с хромовокислым калием – темно-красный осадок хромовокислого серебра. Так растворимость хлористого серебра меньше, чем хромовокислого, то вначале образуется белый осадок хлористого серебра по уравнению:

После того, как весь хлор связан, избыток азотнокислого серебра реагирует с хромовокислым калием по уравнению:

Покраснение раствора или появление красного осадка хромовокислого серебра свидетельствует о том, что весь хлор связан с серебром.
Метод предназначен для определения массовой доли соли в полуфабрикатах, в которых нормируется этот показатель, а также в блюдах (изделиях) в случае разногласий при органолептической оценке.
Проведение испытаний
Навеску предварительно измельчают в мясорубке с диаметром отверстий решетки 3-4,5 мм и тщательно перемешивают. Навеску средней пробы около 20-25г взвешивают с точностью до 0,01 г в химическом стакане или фарфоровой чашке, приливают 40-50см3 горячей (70-80°C) дистиллированной воды, хорошо размешивают продукт стеклянной палочкой и количественно, без потерь, переносят при помощи воронки в мерную колбу вместимостью 200-250см3, смывая прилипшие частицы навески водой.
Колбу доливают дистиллированной водой до половины объема, закрывают пробкой и помещают в аппарат для встряхивания на 15 мин. При отсутствии аппарата для встряхивания содержимое колбы настаивают 25-30 мин, периодически взбалтывая.
Далее колбу доливают дистиллированной водой до метки, закрывают пробкой, содержимое колбы хорошо перемешивают и фильтруют через сухой складчатый фильтр или вату в сухой стакан или колбу.
В связи с тем, что хромат серебра растворяется в кислотах, метод Мора применим лишь в нейтральной или слабощелочной среде, поэтому после охлаждения содержимого до комнатной температуры проверяют реакцию среды по универсальной индикаторной бумаге и при наличии кислот их нейтрализуют 0,1 моль/дм3 (0,1н) раствором щелочи в присутствии фенолфталеина. Для этого 10см3 водной вытяжки нейтрализуют 0,1моль/дм3 (0,1н) раствором щелочи в присутствии фенолфталеина.
В коническую колбу емкостью 200-250см3 пипеткой отбирают 50см3 водной вытяжки, прибавляют тот объем 0,1моль/дм3 (0,1н) раствора щелочи, пошедший на нейтрализацию кислот, затем приливают 1см3 10% раствора хромовокислого калия и титруют 0,1моль/дм3 (0,1н) раствором азотнокислого серебра до появления кирпично-красной окраски, не исчезающей в течение 1 мин.
При определении содержания хлорида натрия в кулинарных полуфабрикатах или изделиях из рыбы или в пробах с интенсивной окраской, затрудняющей титрование, навеску рекомендуется озолять. Для этого в тигель берут навеску, подсушивают ее в сушильном шкафу при постепенном повышении температуры до 120-140°C. Высушенную массу осторожно обугливают на газовой горелке до получения остатка темно-серого цвета, легко распадающегося при надавливании стеклянной палочкой. Затем обугленную массу осторожно измельчают палочкой, обрабатывают 4-5 раз небольшими порциями горячей воды (80-90°C), каждый раз сливая жидкую часть посредством стеклянной палочки на бумажный фильтр. Фильтрат собирают в мерную колбу вместимостью 250см3. Остаток в тигле и на фильтре промывают горячей водой до прекращения реакции последних порций фильтрата с нитратом серебра. Для этого небольшую порцию (1-2см3) фильтрата подкисляют в пробирке 1-2 каплями раствора азотной кислоты с массовой долей 10% и прибавляют 1-2 капли раствора нитрата серебра. Если фильтрат остается прозрачным, обработку золы горячей водой заканчивают. При необходимости фильтрат в мерной колбе нейтрализуют раствором щелочи в присутствии фенолфталеина, доводят водой до метки, закрывают пробкой и хорошо перемешивают.
Массовую долю хлорида натрия (Х) в процентах или в граммах в блюде (изделии) рассчитывают по формуле:
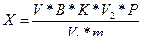
где:
V - объем раствора нитрата серебра, израсходованный на титрование испытуемого раствора, см3;
В - количество хлорида натрия, эквивалентное 1см3 0,1 моль/дм3 (0,1н) раствора нитрата серебра, г (0,00585 для 0,1моль/дм3 AgNO3);
К - поправочный коэффициент к титру раствора нитрата серебра;
Р - масса блюда, г (при определении содержания соли в процентах Р = 100);
V1 - количество фильтрата, взятое для титрования, см3;
m - масса навески, г;
V2 - объем колбы, в которой растворена навеска, см3.
Расхождение между результатами параллельных определений не должно превышать 0,02%.
За конечный результат принимают среднее арифметическое двух параллельных определений, вычисленное с точностью до 0,1%.
Порядок определения поваренной соли меркурометрическим методом
Сущность метода:
Метод основан на осаждении хлорида натрия в водном растворе азотнокислой закисью ртути в кислой среде при добавлении роданистого железа, который окрашивает раствор в красный цвет.
Хлор-ионы реагируют с ионами двухвалентной ртути с образованием малодиссоциированного хлорида ртути (сулемы) по уравнению:
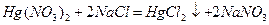
При достижении точки эквивалентности концентрация ионов двухвалентной ртути в растворе резко возрастает, в качестве индикатора для определения конца реакции применяют дифенилкарбазон или дифенилкарбазид. Эти индикаторы в слабокислых растворах образуют с ионами двухвалентной ртути внутрикомплексные соединения, окрашенные в сине-фиолетовый цвет.
Проведение испытаний
Навеску предварительно измельчают в мясорубке с диаметром отверстий решетки 3-4,5 мм и тщательно перемешивают. Навеску средней пробы около 20-25г взвешивают с точностью до 0,01 г в химическом стакане или фарфоровой чашке, приливают 40-50см3 горячей (70-80°C) дистиллированной воды, хорошо размешивают продукт стеклянной палочкой и количественно, без потерь, переносят при помощи воронки в мерную колбу вместимостью 200-250см3, смывая прилипшие частицы навески водой.
Колбу доливают дистиллированной водой до половины объема, закрывают пробкой и помещают в аппарат для встряхивания на 15 мин. При отсутствии аппарата для встряхивания содержимое колбы настаивают 25-30 мин, периодически взбалтывая. По окончании настаивания вытяжку осторожно прогревают для коагуляции белковых веществ, охлаждают, доливают дистиллированной водой до метки, закрывают пробкой, содержимое колбы хорошо перемешивают и фильтруют через сухой складчатый фильтр или вату в сухой стакан или колбу.
В коническую колбу на 100см3 отбирают пипеткой 10-25см3 фильтрата, добавляют 1-2 капли концентрированной азотной кислоты (для создания рН-4,0) и 5 капель 1% спиртового раствора дифенилкарбазона. Затем титруют 0,1моль/дм3 (0,1н) раствором азотнокислой ртути до слабой сине-фиолетовой окраски.
Массовую долю хлорида натрия (Х) в процентах или в граммах в блюде (изделии) рассчитывают по формуле:
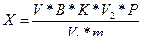
где:
V - объем раствора азотнокислой ртути, израсходованный на титрование испытуемого раствора, см3;
В - количество хлорида натрия, эквивалентное 1см3 0,1 моль/дм3 (0,1н) раствора азотнокислой ртути, г (0,00585для 0,1 моль/дм3 AgNO3);
К - поправочный коэффициент к титру раствора азотнокислой ртути;
Р - масса блюда, г (при определении содержания соли в процентах Р = 100);
V1 - количество фильтрата, взятое для титрования, см3;
m - масса навески, г;
V2 - объем колбы, в которой растворена навеска, см3.
Расхождение между результатами параллельных определений не должно превышать 0,02%.
За конечный результат принимают среднее арифметическое двух параллельных определений, вычисленное с точностью до 0,1%.
Контрольные вопросы
- Какими методами определяется содержание соли продуктах питания?
- В чем заключается сущность аргентометрического метода определения поваренной соли?
- В чем заключается сущность меркурометрического метода определения поваренной соли?
 2020-08-05
2020-08-05 108
108








