Проводят взвешивание грязного картофеля и вымытого и обсушенного картофеля. Загрязненность картофеля выражают в процентах.
Определение крахмалистости картофеля
Крахмалистость картофеля определяют с помощью весов Парова или более точно –по Эверсу. При определении крахмала в картофеле большое значение имеет тщательность взятия аналитической пробы. Масса измельченного на тёрке картофеля сильно расслаивается: крахмал оседает на дно, а сверху отделяется жидкая часть, причём расслоение идёт быстро, поэтому взять правильно 5-граммовую навеску очень трудно. Поэтому после измельчения картофеля на терке его необходимо взбить с помощью миксера в течение 3 минут до получения пенистой, равномерной массы. На технических весах в маленькую фарфоровую чашечку берут навеску исследуемого картофеля 5 г и смывают её 50 мл дистиллированной воды в колбу Штифта на 100 мл. Приливают туда 3 мл 25-процентной соляной кислоты, помещают колбу в сильно кипящую водяную баню и держат при частом перемешивании (особенно вначале) 15 минут. Затем колбу вынимают, прибавляют воды до общего объёма 80–90 мл и охлаждают до 20 ºС. Для осаждения белков и осветления раствора прибавляют 2 мл раствора фосфорновольфрамовой кислоты, потом доливают до метки водой, взбалтыват и фильтруют через двойной складчатый фильтр в сухую колбу. Фильтрат немедленно поляризуют в трубке длиной 200 мл.
При отсутствии фосфорновольфрамовой кислоты для осветления можно применять следующие растворы: раствор сернокислого цинка и раствор железистосинеродистого калия. Вначале приливают 1 мл сульфата цинка, затем после энергичного перемешивания добавляют 1 мл раствора железистосинеродистого калия и снова перемешивают содержимое колбы. Если после добавления осадителей образуется пена, её можно уничтожить, прилив 1–2 капли серного эфира.
При навеске исследуемого картофеля 5 г (в колбе на 100 мл) и поляризации фильтрата в трубке длиной 200 мл, найденное число градусов (среднее из 5 отсчётов) умножают на коэффициент 1,775 (коэффициент Эверса для картофельного крахмала) и получают содержание крахмала в навеске исследуемого картофеля в процентах.
Крахмалистость неоднократно замороженного или насквозь прогнившего картофеля определяют поляриметрическим методом в следующей модификации. Картофель растирают на мелкой терке в кашицу. Навеску кашицы 10,0000 г без потерь смывают 50 мл 1,124%-ной соляной кислоты в мерную колбу на 100 мл. Колбу помещают в кипящую водяную баню на 15 мин.
Далее определение крахмалистости ведут, как и при исследовании зерна (п. 3.2.9). Поляризацию проводят в поляриметрической трубке длиной 100 мм. Показание поляриметра умножают на коэффициент Эверса для картофельного крахмала (1,775) и получают процентное содержание крахмала в картофеле.
Определение влажности картофеля
Опыт делается в двух повторностях. В бюксы вносят 15-20 г чистого кварцевого песка и в каждый бюкс вкладывают стеклянную палочку такой длины, чтобы бюкс с палочкой можно было закрыть крышкой. Далее бюксы высушивают при 105 С в течение 45 мин. После высушивания бюксы закрывают крышками и охлаждают в эксикаторе до температуры 20 ºС (не менее 40 мин). Записываю вес высушенных бюксов с песком и палочкой.
Вымытые клубни обсушивают, не очищая от кожуры, натирают на тёрке. В каждый бюкс на весах вносят навеску картофеля массой 5 г. После этого стеклянной палочкой картофель осторожно и равномерно перемешивают с песком, не допуская потерь песка или картофеля. Не вынимая палочки бюкс высушивают до постоянной массы в течение 3 ч при 105 ºС. Далее бюксы закрывают крышками и охлаждают в эксикаторе до температуры 20 ºС (не менее 40 мин)., взвешивают, записывают массу. Проверкой является установление постоянной массы высушенного вещества. Для этого бюксы снова ставят в сушильный шкаф и высушивают ещё 30 мин при 105 ºС. Повторяют процедуры охлаждения и взвешивания. Расхождение масс бюксов должно быть в пределе ±0,05 г.
ЛАБОРАТОРНАЯ РАБОТА № 2
ОПРЕДЕЛЕНИЕ АМИЛОЛИТИЧЕСКОЙ АКТИВНОСТИ
ФОТОКОЛОРИМЕТРИЧЕСКИЙ МЕТОДОМ
Определение амилолитической активности ферментов
Солода
Сущность метода
Для точного определения активности ферментов необходимо строго соблюдать определенные условия проведения реакции, катализируемой ферментом (температура, рН среды, длительность реакции, концентрация субстрата и способы его приготовления, способы приготовления ферментного раствора).
На скорость ферментативной реакции большое влияние оказывает соотношение фермент-субстрат. Поэтому активность ферментов следует определять при строго постоянном соотношении фермента и субстрата, которое обеспечивает определенную степень гидролиза субстрата.
Активность ферментов находят с помощью графика, выражающего зависимость степени гидролиза субстрата от числа единиц активности фермента, взятого для реакции; на оси абсцисс этого графика откладывают количество взятого для анализа солода (или ферментного препарата), а на оси ординат – степень гидролиза субстрата. В большинстве случаев эта зависимость выражается прямой линией в пределах гидролиза от 15 до 75 %. Прямолинейный участок графика дает возможность по количеству субстрата, превращенного в процессе реакции, определять активность препарата. Для удобства расчета прямая графика может быть представлена в виде уравнения.
Амилолитическая активность (АС) характеризует способность ферментов солода катализировать расщепление крахмала в основном на декстрины с небольшим количеством олигосахаридов. Эта активность главным образом обусловлена присутствием a-амилазы.
В основу определения амилолитической активности положена зависимость степени гидролиза крахмала от числа единиц фермента, взятого для проведения ферментативной реакции.
Для определения амилолитической способности крахмал гидролизуют вытяжкой исследуемого солода и определяют количество оставшегося негидролизованного крахмала после действия ферментов по йодкрахмальной реакции с использованием фотоэлектроколориметра.
При фотоколориметрическом методе определения за единицу амилолитической способности принимают количество фермента, которое катализирует гидролиз крахмала при следующих условиях:
– температура реакции 30 °С;
– рН раствора 4,8…4,9;
– продолжительность реакции 10 минут;
– объем 15 мл (10 мл субстрата и 5 мл ферментного раствора);
– постоянное соотношение в реакционной смеси фермент-субстрат, обеспечивающее гидролиз крахмала на 30 % за 10 мин.
Реактивы
– 1 %-ный забуференный раствор крахмала (картофельного) – навеску растворимого крахмала берут из такого расчета, чтобы в 100 мл раствора содержался 1 г сухого крахмала. Например, если влажность крахмала 13 %, то навеска крахмала в граммах для 100 мл 1 %-ного раствора должна составить:
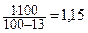
Взвешенную на технических весах навеску крахмала без потерь переносят в мерную колбу на 100 мл, добавляют 25 мл дистиллированной воды и перемешивают, затем добавляют еще 25 мл воды и помещают колбу в кипящую водяную баню, выдерживая ее до полного растворения крахмала и непрерывно помешивая раствор. Содержимое колбы охлаждают до 20 °С, добавляют 10 мл буферного раствора (рН 4,8…4,9), доводят водой до метки и перемешивают;
– буферный раствор (рН 4,8…4,9);
– 0,1 н раствор соляной кислоты;
– основной раствор йода – в тарированном стаканчике с притертой крышкой отвешивают 0,5 г йода и 5,0 г йодированного калия и добавляют 2,0 мл дистиллированной воды. Стаканчик закрывают крышкой, содержимое перемешивают до полного растворения йода. Раствор переливают в мерную колбу с притертой крышкой на 200 мл, доводят до метки дистиллированной водой и тщательно перемешивают. Полученный раствор хранят в темном месте и используют в течение 30 дней;
– рабочий раствор йода – 2 мл основного раствора разбавляют в мерной колбе на 100 мл дистиллированной водой до метки. Перед употреблением необходимо проверить оптическую плотность рабочего раствора йода на фотоэлектроколориметре в кювете с длиной грани 1,0 см при светофильтре с длиной волны l=453 нм.
Оптическая плотность раствора йода должна быть равна 0,160 ± 0,01. В случае отклонения оптической плотности раствора от этой величины ее приводят к необходимой добавлением нескольких капель воды или основного раствора йода;
– солодовая вытяжка – взвешивают на технических весах две навески измельченного солода – одну для определения влажности и вторую для определения АС. Величина навески просяного солода 10 г, ячменного, овсяного и ржаного 5 г. Навеску количественно переносят в химический стакан или коническую колбу на 200…250 мл, добавляют 10 мл буферного раствора (рН 4,7…4,9) и 90 мл дистиллированной воды.
Полученную смесь выдерживают в течение 60 мин при 30 °С, периодически помешивая стеклянной палочкой, затем фильтруют и фильтрат используют в качестве основного раствора для определения АС. Для проведения ферментативной реакции готовят рабочий раствор, пользуясь данными таблицы 1.
Таблица 1 – Приготовление рабочих ферментных растворов солода
| Ожидаемая активность солода, ед.АС | Масса солода в 5 мл рабочего раствора, мг | Расход основного раствора на приготовление рабочего раствора, мл/100 мл |
| Для просяного солода | ||
| 5…10 | 30 | 6 |
| 11…15 | 20 | 4 |
| 16…20 | 10 | 2 |
| Для ячменного, овсяного, ржаного солода | ||
| 16…20 | 20 | 8 |
| 21…30 | 10 | 4 |
| 31…50 | 7,5 | 3 |
Проведение анализа
Осахаривание крахмала ведут в строго определенных условиях:
– температура 30 °С;
– рН среды 4,8…4,9 ед. рН;
– продолжительность реакции 10 мин;
– объем раствора 15 мл (10 мл раствора крахмала +5 мл рабочего раствора ферментов солода).
Для анализа берут две пробирки (18х180 мл), наливают в каждую по 10 мл приготовленного раствора крахмала, ставят в ультратермостат или водяную баню с температурой 30 °С ± 0,5 °С и выдерживают в течение 10 мин. Затем, не вынимая пробирок из термостата, наливают в первую 5 мл дистиллированной воды (контрольный раствор), а во вторую – 5 мл солодовой вытяжки (опытный раствор). Смеси быстро перемешивают и выдерживают точно 10 мин при той же температуре.
После этого пробирки с реакционной смесью вынимают из термостата, отбирают из каждой по 1 мл и переносят в другие пробирки с предварительно налитыми туда 10 мл 0,1 н соляной кислотой, которая прерывает действие ферментов. Жидкости взбалтывают, от каждой пробы отбирают по 1 мл, переносят в новые пробирки, в которые предварительно налито по 10 мл рабочего раствора йода, и содержимое пробирок перемешивают.
Контрольный раствор окрашивается в синий цвет, опытный – в фиолетово-коричневый различной интенсивности, в зависимости от количества гидролизованного крахмала. Далее определяют оптическую плотность полученных растворов в кюветах с длиной грани 1,0 см при красном светофильтре с длиной волны l=656 нм или близкой к этой величине. Колориметрирование проводят по сравнению с дистиллированной водой.
Оптическая плотность контрольного раствора соответствует количеству исходного крахмала субстрата во взятом растворе, а оптическая плотность опытного раствора – количеству крахмала, оставшемуся негидролизованным после действия ферментов. Этот крахмал надо понимать условно, так как фактически в растворе крахмала нет, он превратился в декстрины различной молекулярной массы, которые и дают фиолетово-коричневую окраску. Разность между оптической плотностью контрольного и опытного растворов соответствует количеству крахмала, которое подверглось гидролизу под действием ферментов солода.
Количество гидролизованного крахмала (в г) рассчитывают по формуле:
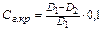 ,
,
где D1 – оптическая плотность контрольного раствора;
D2 – оптическая плотность опытного раствора;
0,1 – количество крахмала, взятое для определения в качестве субстрата, г.
Если окажется, что количество гидролизованного крахмала больше 0,07 или меньше 0,02, то анализ повторяют, изменив разбавление рабочего раствора солодовой вытяжки.
Амилолитическую способность (ед./г) рассчитывают по формуле (3):
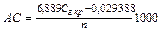 , .
, .
где Сг.кр – количество гидролизованного крахмала субстрата, г;
n – масса солода, содержащаяся в 5 мл раствора, взятого для осахаривания крахмала, мг;
6,889 и 0,029388 – коэффициенты расчетного уравнения, полученные экспериментально для данных условий, установленные с учетом действия фермента в течение 60 мин.
 2020-09-26
2020-09-26 502
502








