Химический эквивалент вещества (Э) – это количество вещества, способное прореагировать (или выделить в результате химической реакции) с 1 моль атомов водорода.
Закон химических эквивалентов – все вещества взаимодействуют друг с другом и образуются в результате реакций в эквивалентных количествах.
Эквиваленты некоторых классов веществ.
Эквивалент простого вещества Ах: 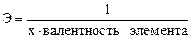
Эквивалент оксида АmОn: 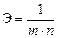
Эквивалент гидроксида М(ОН)х: 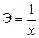
Эквивалент кислоты НхА: 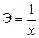
Эквивалент соли (K+n)m(A-m)n: 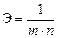 , где m – количество катионов K+n, входящих в состав соли, а n – заряд катиона.
, где m – количество катионов K+n, входящих в состав соли, а n – заряд катиона.
NB! Эквивалент вещества зависит от реакции с участием этого вещества!
С + О2 = СО2 Э(С)= 1/4
2С + О2 = 2СО Э(С)= 1/2
2NaOH + H2SO4 = Na2SO4 + 2H2O Э(H2SO4)=1/2
NaOH + H2SO4 = NaHSO4 + H2O Э(H2SO4)=1
Эквивалентная масса( MЭ ) – масса одного эквивалента вещества; измеряется в г/экв.
Количество эквивалентов nЭ:
Связь между Э, MЭ, M, nЭ, ν.
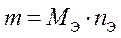 ,
, 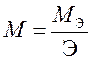 или
или 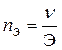
Строение вещества
 2020-09-24
2020-09-24 109
109








