Экспериментальная установка (рис.1) состоит из баллона Б объемом 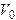 , который с помощью крана К может быть соединен либо с резиновой грушей Г, либо с атмосферой. Разность давлений воздуха в баллоне и в окружающей среде измеряется открытым жидкостным манометром М, заполненным водой или каким-либо маловязким маслом. Разность уровней жидкости в коленах манометра прямо пропорциональна разности давлений воздуха в баллоне и в окружающей среде:
, который с помощью крана К может быть соединен либо с резиновой грушей Г, либо с атмосферой. Разность давлений воздуха в баллоне и в окружающей среде измеряется открытым жидкостным манометром М, заполненным водой или каким-либо маловязким маслом. Разность уровней жидкости в коленах манометра прямо пропорциональна разности давлений воздуха в баллоне и в окружающей среде:
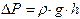 ,
,
где 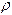 − плотность манометрической жидкости, g − ускорение свободного падения, h − разность уровней жидкости в коленах манометра.
− плотность манометрической жидкости, g − ускорение свободного падения, h − разность уровней жидкости в коленах манометра.
Рассмотрим термодинамические процессы, происходящие с воздухом, заключенным в баллон.
Сжатие воздуха в баллоне. Краном К соединяют баллон с резиновой грушей и накачивают воздух до давления, соответствующего разности уровней жидкости h в манометре, равной 15-20 делений шкалы, после чего кран 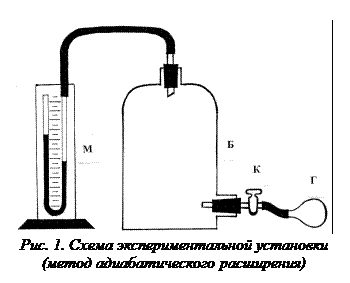 закрывают. При сжатии газ нагревается. Необходимо выждать не менее 3-5 минут, чтобы газ в баллоне охладился до комнатной температуры
закрывают. При сжатии газ нагревается. Необходимо выждать не менее 3-5 минут, чтобы газ в баллоне охладился до комнатной температуры 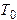 . При установлении равновесия между газом в баллоне и окружающей средой давление в баллоне перестанет изменяться и прекращается изменение уровней жидкости в манометре. В конце первого этапа состояние воздуха в баллоне характеризуется температурой
. При установлении равновесия между газом в баллоне и окружающей средой давление в баллоне перестанет изменяться и прекращается изменение уровней жидкости в манометре. В конце первого этапа состояние воздуха в баллоне характеризуется температурой 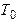 и давлением
и давлением 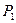 :
:
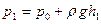 , (4)
, (4)
где 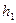 − установившаяся разность уровней манометрической жидкости в конце этапа.
− установившаяся разность уровней манометрической жидкости в конце этапа.
Адиабатное расширение. Поворотом крана К на короткое время соединяют баллон с атмосферой. Как только давление в баллоне станет равным атмосферному, о чем судят по показаниям манометра (h =0), кран закрывают. Поскольку процесс расширения происходит быстро, теплообмен между содержимым баллона и окружающим воздухом не происходит, т.е. наблюдается адиабатное расширение, сопровождающееся понижением температуры. В конце процесса расширения воздух в баллоне имеет давление 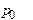 и температуру
и температуру 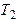 . Изменение параметров состояния газа при совершении адиабатического процесса описывается уравнением Пуассона:
. Изменение параметров состояния газа при совершении адиабатического процесса описывается уравнением Пуассона:
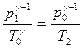 . (5)
. (5)
Изохорическое нагревание. Закрыв кран К, следует дождаться, когда установится тепловое равновесие воздуха в баллоне и окружающей среде. Момент установления равновесия фиксируется по прекращению перемещения уровней жидкости в коленах манометра. В этот момент состояние воздуха в баллоне характеризуется температурой 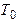 и давлением
и давлением 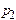 :
:
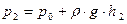 , (6)
, (6)
где 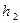 − установившаяся разность уровней жидкости в манометре в конце процесса нагревания.
− установившаяся разность уровней жидкости в манометре в конце процесса нагревания.
Согласно закону Гей-Люссака:
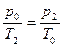 . (7)
. (7)
Исключив из (5) и (7) температуры 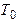 и
и 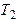 , получаем:
, получаем:
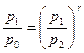 . (8)
. (8)
Логарифмируя обе части соотношения (8), находим:
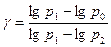 . (9)
. (9)
Разложим 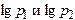 в ряд Тейлора, ограничившись первыми двумя членами ряда, поскольку, как уже было сказано, изменение давления воздуха в баллоне весьма невелико по сравнению с
в ряд Тейлора, ограничившись первыми двумя членами ряда, поскольку, как уже было сказано, изменение давления воздуха в баллоне весьма невелико по сравнению с 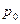 :
:
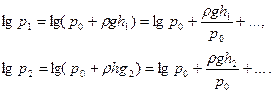
C учетом разложения в ряд расчетная формула приобретает вид:
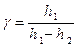 . (10)
. (10)
 2020-10-10
2020-10-10 329
329








