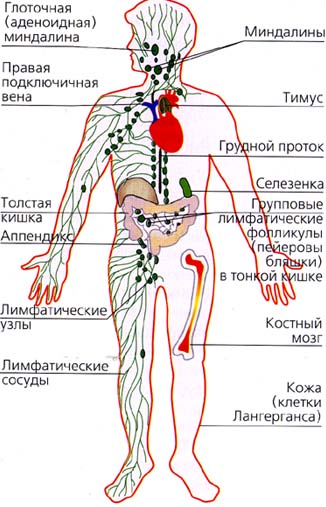
Иммунитет – способ защиты организма от живых тел и веществ, несущих в себе признаки чужеродной информации (Петров Р.В., 1987). Основное предназначение иммунной системы – поддержание генетического постоянства (гомеостаза) организма. Клетки, обеспечивающиезащиту организма от генетически чужеродного, рассеяны по всему организму и организованы в структуры и органы, в совокупности составляющие иммунную (лимфоидную) систему (рис. 1). Лимфоидные органы делятся на центральные и периферические.
 К центральным органам иммунной системы относятся вилочковая железа (тимус) и костный мозг, в которых идут процессы пролиферации и созревания иммунокомпетентных клеток (ИКК) из клеток-предшественников, но не осуществляется иммунный ответ. В тимусе происходит дифференцировка «тимусзависимых» лимфоцитов – Т-лимфоцитов. Становление В-лимфоцитов осуществляется на территории костного мозга. Начальная буква «bonemarrow» (костный мозг) – «B» используется для обоз-
К центральным органам иммунной системы относятся вилочковая железа (тимус) и костный мозг, в которых идут процессы пролиферации и созревания иммунокомпетентных клеток (ИКК) из клеток-предшественников, но не осуществляется иммунный ответ. В тимусе происходит дифференцировка «тимусзависимых» лимфоцитов – Т-лимфоцитов. Становление В-лимфоцитов осуществляется на территории костного мозга. Начальная буква «bonemarrow» (костный мозг) – «B» используется для обоз-
| Рис. 1. Иммунная система человека |
Созревшие в центральных органах иммунной системы Т-, В-клетки поступают в циркуляцию и расселяются по периферическим органам, к числу которых относят лимфатические узлы, селезенку, лимфоидные скопления по ходу слизистых оболочек (рис. 2).
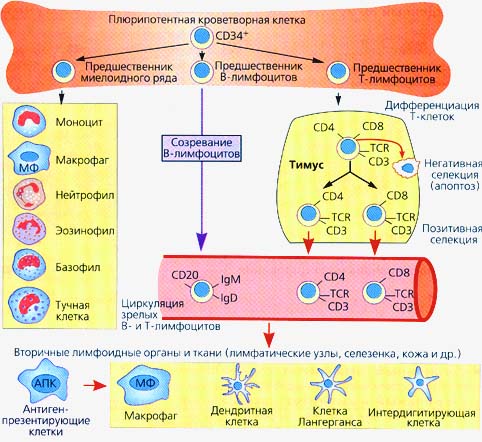
Рис. 2. Схема созревания клеток иммунной системы
Красный костный мозг не является непосредственным лимфоидным органом, однако его следует рассматривать как орган иммунной системы. Здесь обнаруживаются стволовые кроветворные клетки (CD34+Thy1+), которые обладают уникальным свойством – полипотентностью, т.е. способностью к дифференцировке, по меньшей мере, на 11 линий кроветворных клеток (Т- и В-лимфоциты, натуральные киллеры, дендритные лимфоидные клетки, эритроциты, мегакариоциты, нейтрофильные, эозинофильные, базофильные гранулоциты, моноциты/макрофаги, миелоидные дендритные клетки). Стволовые кроветворные клетки обладают способностью к миграции – выходу в кровь и возвращению в костный мозг, что получило название «homing-effect» (инстинкт дома). Именно это свойство стволовых клеток обеспечивает обмен кроветворных клеток между разобщенными кроветворными территориями, в том числе теми, которые входят в состав лимфоидных органов.
Согласно современной теории кроветворения все клетки крови происходят из единой родоначальной клетки – полипотентной стволовой кроветворной клетки, дающей начало двум линиям дифференцировки – лимфоидной и миелоидной. По мере дифференцировки миелоидной стволовой клетки образуются олигопотентные и моно-, или унипотентные, коммитированные предшественники: КОЕ-ГМ (колониеобразующая единица гранулоцитарно-макрофагальная), КОЕ-М (колониеобразующая единица моноцитарно-макрофагальная), КОЕ-МГКЦ (колониеобразующая единица мегакариоцитарная), БОЕ-Э и КОЕ-Э (бурстобразующая и колониеобразующая единица для эритроцитов).
Центральная фигура в иммунитете – лимфоцит (рис. 3). Лимфоциты происходят из лимфоидной стволовой клетки. На долю лимфоидных клеток в костном мозге приходится до 10–15% кариоцитов. В костном мозге формируются ранние предшественники Т- и В-лимфоцитов. Предшественники Т-лимфо-цитов мигрируют в тимус, где происходит их дифференцировка до зрелых Т-клеток. Дифференцировка В-лимфоцитов осуществляется на территории костного мозга, где В-лимфоциты проходят этап антигеннезависимой дифференцировки, заключающейся в формировании специфических рецепторов – иммуноглобулинов (Ig) и избирательной экспрессии мембранных и цитоплазматических маркеров. Самый ранний распознаваемый этап дифференцировки В-лимфоцитов носит название про-В-лимфоцита. На этой стадии проис
| Рис. 3. Сканограмма лимфоцита |
В костном мозге формируются ранние предшественники Т-лимфоцитов, которые затем заселяют тимус. Наиболее ранний Т-клеточный маркер -CD7, появление его на стволовых CD34+-гемопоэтических клетках указывает на Т-клеточную направленность дифференцировки. В незрелых протимоцитах начинается перестройка генов Т-клеточного рецептора (T-cellreceptor – TCR), который придает специфичность активационным процессам в этих клетках. Завершающий этап – формирование TCR на Т-лимфоцитах происходит в тимусе, поэтому клетки-предшест-венники должны мигрировать из костного мозга в тимус. Из клеток-предшественников Т-ряда, покинувших костный мозг, в тимус проникает не более 5%. Судьба клеток, затерявшихся после выхода из костного мозга, неизвестна. Есть данные, что часть из них, попадая в селезенку, трансформируется в NK-клетки.
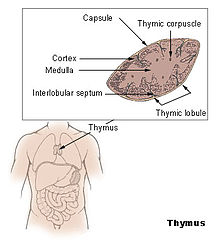
Вилочковая железа (тимус) располагается в верхней части грудины между трахеей и грудиной, над сердцем (рис. 4). Железой стали ее называть потому, что она развивается точно так, как и другие железы: образуются четыре выроста из глоточной кишки, затем они попарно сливаются и образуют типичную железу, соединенную выводными протоками с будущим пищеводом. Затем протоки исчезают.Органогенез в железе заканчивается в период внутриутробного развития, уже после 20-й недели
 она окончательно формируется как орган. Масса вилочковой железы у новорожденного – 10–15 г (для сравнения селезенка – 11 г, щитовидная железа – 4,6 г). В 9–12 лет масса вилочковой железы достигает максимума – 30–40 г, после чего рост прекращается, и в 25–27 лет тимус начинает медленно атрофироваться. У пожилых людей на его месте развивается жировая ткань.
она окончательно формируется как орган. Масса вилочковой железы у новорожденного – 10–15 г (для сравнения селезенка – 11 г, щитовидная железа – 4,6 г). В 9–12 лет масса вилочковой железы достигает максимума – 30–40 г, после чего рост прекращается, и в 25–27 лет тимус начинает медленно атрофироваться. У пожилых людей на его месте развивается жировая ткань.
| Рис. 4. Вилочковая железа (thymus) |
Клетки тимического эпителия продуцируют гормоны тимуса (несколько разновидностей тимозина, тимопоэтин, тимический сывороточный фактор, или тимулин). Часть из них – α1-тимозин, тимопоэтин, тимулин – поступает в кровоток и выполняют функцию гормонов. Полагают, что роль этих субстанций во внутритимусном развитии тимоцитов вспомогательная. Более значимы прямые межклеточные взаимодействия тимоцитов с клетками стромы. Однако гормонам тимуса принадлежит решающая роль во внетимусном «дозревании». Во внешней зоне коры располагаются предшественники Т-лимфоцитов – кортикальные тимоциты, являющиеся следующей стадией развития костномозговых протимоцитов (90% присутствуют здесь с эмбрионального периода, 10% составляют клетки, мигрировавшие из костного мозга). Особым компонентом микроокружения кортикальных тимоцитов являются клетки-няньки, обеспечивающие ранние этапы дифференцировк Т-клеток, с их влиянием связано формирование Т-клеточных рецепторов. Клетки-няньки также играют важную роль в позитивной и негативной селекции Т-клеток (рис. 5). В ходе позитивной селекции проверяется способность Т-клеток вступать в кооперацию с другими ИКК. На поверхности последних экспрессированы антигены гистосовместимости, которые кодируются системой генов, получивших наименование MHC – Majorhystocompitibilitycom
| Рис. 5. Процессы апоптоза в тимусе |
Периферические органы иммунной системы являются местом, где происходит встреча зрелых ИКК с антигенами, антигензависимый этап дифференцировки этих клеток и развитие иммунного ответа. Фактически все периферические лимфоидные органы являются фильтрами, барьерами, где происходит захват антигена, его расщепление и распознавание. Так, в лимфоузлах происходит фильтрация лимфы и тканевой жидкости, в селезенке – крови, а лимфоидные скопления по ходу слизистых оболочек (mucosa-associatedlymphoidtissue – MALT) первыми встречают и распознают большинство антигенов.
В-лимфоциты локализуются в наружных слоях коры лимфатических узлов (рис. 6), краевой зоне и фолликулах белой пульпы селезенки (рис. 7) и экспрессируют на мембране CD19, CD20, CD21, CD22, определяющих фенотип периферических В-клеток. В отсутствие антигенной стимуляции В-лимфоциты через несколько дней гибнут путем апоптоза. После встречи со «своим» антигеном и кооперативных взаимодействий в ходе иммунного ответа происходит активация и пролиферация В-лимфоцитов, в процессе чего на мембране появляются молекулы CD23, повышается экспрессия HLA-DR, а затем осуществляется последняя стадия развития В-лимфоцита – превращение в плазматическую клетку (плазмоцит).
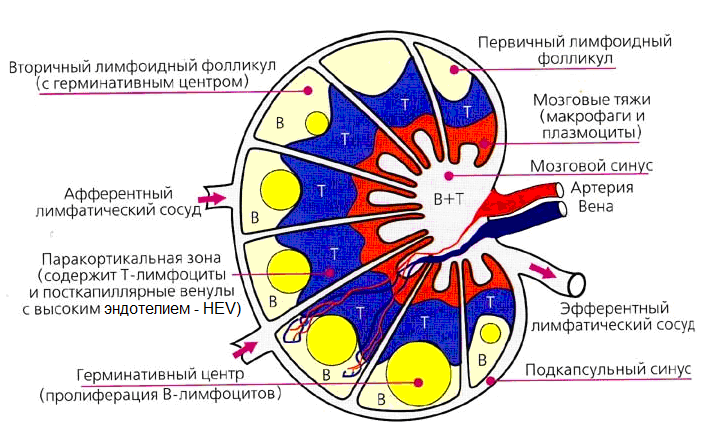
Рис. 6. Схема строения лимфатического узла
 Зрелые плазмоциты син-тезируют и секретируют Ig, теряя при этом большинство В-клеточных мембранных рецепторов, на их поверхности определяется лишь CD38. При этом В-клетка может секретировать антитела четырех классов – IgМ, IgА (представленные двумя подклассами – IgА1 и IgА2), IgЕ и IgG (подклассы – IgG1, IgG2, IgG3, IgG4). Кроме того, имеется и пя
Зрелые плазмоциты син-тезируют и секретируют Ig, теряя при этом большинство В-клеточных мембранных рецепторов, на их поверхности определяется лишь CD38. При этом В-клетка может секретировать антитела четырех классов – IgМ, IgА (представленные двумя подклассами – IgА1 и IgА2), IgЕ и IgG (подклассы – IgG1, IgG2, IgG3, IgG4). Кроме того, имеется и пя
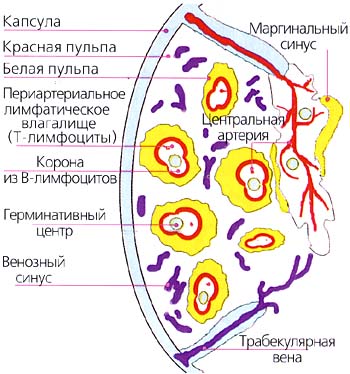
| Рис. 7. Схема строения селезенки |
Наивные Т-лимфоциты (CD4+- или CD8+-клетки), поступающие в периферические лимфоидные органы (лимфатические узлы, селезенка, лимфатические фолликулы) из тимуса, занимают преимущественно специализированные тимусзависимые зоны: паракортикальные зоны лимфатических узлов, параартериальные муфты селезенки и групповых лимфатических фолликулов (пейеровых бляшек). В других участках они смешаны с В-лимфоцитами. Помимо кортикальной зоны Т-клетки обнаруживаются в медуллярной зоне вместе с В-лимфоцитами и плазмоцитами. Причем в этих областях преобладают CD4+-клетки (Т-хелперы) над CD8+-клетками (Т-киллерами), располагаясь скоплениями вокруг дендритных клеток.
Долгое время в иммунологии господствовало представление о том, что Т-лимфоциты CD8-фенотипа являются клетками-супрессорами. В настоящее время считается, что специальных клеток, выполняющих лишь супрессорную роль в иммунном ответе, не существует. Активация Tх1 с соответствующим спектром цитокинов, преимущественно провоспалительного действия, сдерживает развитие гуморального иммунного ответа, связанного с функцией Tх2, продуцирующих цитокины с противовоспалительным эффектом. Tх2, в свою очередь, подавляют проявление функций Tх1. Иными словами, Tх1 являются супрессорами для Tх2, и наоборот. Одновременное включение функций Tх1 и Tх2 тормозит развитие любой формы иммунного ответа и приводит к внешним признакам недостаточности иммунного ответа, что нередко наблюдается при патологических состояниях.
Распределение Т- и В-лимфоцитов между периферическими лимфоидными органами неодинаково. В лимфатических узлах Т-клетки составляют 60–75% всех лимфоцитов, а В-клетки – 15–20%, в селезенке на долю Т-клеток приходится 45-60%, а В-клеток – 35–45% числа всех лимфоидных клеток, в то время как в структурах MALT содержание В-лимфоцитов возрастает до 25–40%. В результате характер иммунного ответа в периферических лимфоидных органах также отличается. Так, с лимфоузлами в основном связано развитие клеточного иммунного ответа, со структурами MALT – гуморального ответа, при этом в селезенке оба главных пути ответа развиваются с примерно равной частотой.
Одной из важнейших черт всех периферических лимфоидных органов является наличие и/или миграция в них антигенпрезентирующих клеток (АПК). К профессиональным АПК относятся дендритные клетки, макрофаги и В-лимфоциты. Главными чертами АПК являются способность к поглощению антигена (путем фагоцитоза, пиноцитоза или макропиноцитоза), а также его обработка для предъявления Т-лимфоцитам. Кроме того, лишь эти клетки способны к первичному захвату антигена, его расщеплению на короткие пептидные фрагменты (процессинг антигенов), их экспрессии на своей мембране и предъявлению (презентации) антигенных фрагментов Т-лимфоцитам в ассоциации с молекулами MHC. Помимо этого, АПК секретируют ряд важнейших медиаторов иммунного ответа, в частности ИЛ-1β, ФНОα, ИЛ-8.
 2020-10-10
2020-10-10 303
303








