Амиды обладают слабыми как кислотными, так и основными свойствами. Причиной пониженной основности аминогруппы в амидах является сопряжение неподеленной пары электронов атома азота с карбонильной группой. При взаимодействии с сильными кислотами амиды протонируются по атому кислорода как в разбавленных, так и в концентрированных растворах кислот.
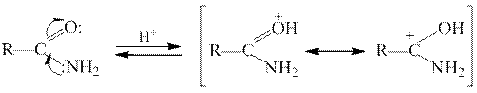
Кислотно-основное взаимодействие лежит в основе образования амидами межмолекулярных ассоциатов, существованием которых объясняются высокие температуры плавления и кипения амидов. Возможно существование двух типов ассоциатов: линейных полимеров и циклических димеров.
Реакции ацилирования.
Из числа реакций ацилирования практическое значение имеет гидролиз амидов, который можно проводить в кислой и щелочной средах. Амиды гидролизуются намного труднее, чем другие функциональные производные карбоновых кислот. Гидролиз амидов проводится в более жестких условиях по сравнению с гидролизом сложных эфиров.
Кислотный гидролиз амидов – необратимая реакция, приводящая к образованию карбоновой кислоты и аммониевой соли:
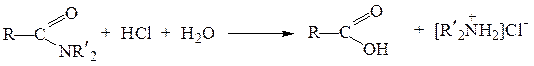
Щелочной гидролиз тоже необратимая реакция; в результате её образуется соль карбоновой кислоты и аммиак или амин:
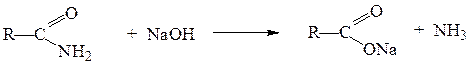
Расщепление азотистой кислотой.
При взаимодействии с азотистой кислотой и другими нитрозирующими агентами амиды превращаются в соответствующие карбоновые кислоты.
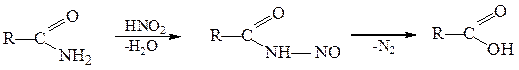
Дегидратация.
Незамещенные амиды под действием оксида фосфора (V) и некоторых других реагентов (POCl3, PCl5, SOCl2) превращаются в нитрилы:
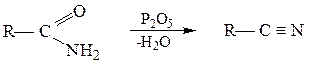
Восстановление.
В зависимости от применяемого реагента амиды могут быть восстановлены в амины (без разрыва связей C─ N) или в альдегиды (с разрывом связи C─ N).
При действии алюмогидрида лития амиды восстанавливаются в первичные, вторичные и третичные амины:
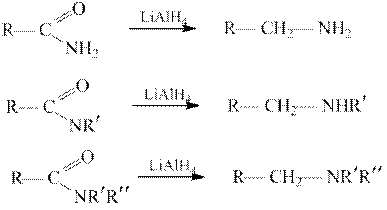
Ацилирование амидов.
При нагревании незамещенных или N -монозамещенных амидов с ангидридами или галогенангидридами образуются имиды, т.е. диацильные производные аммиака
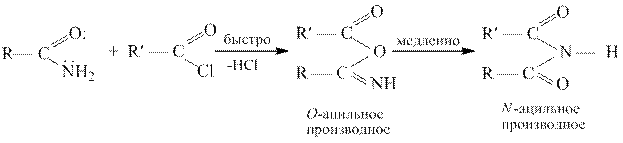
Алкилирование.
Алкилирование амидов, как и ацилирование, можно осуществить по атомам азота и кислорода:
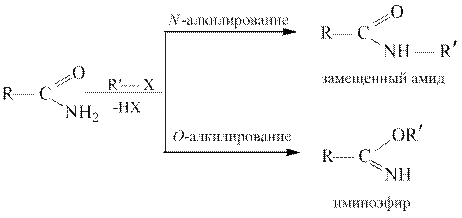
Продукты N -алкилирования термодинамически более устойчивы по сравнению с продуктами О -алкилирования, которые называются иминоэфирами или имидатами.
Галогенирование.
Галогенирование амидов в избытке щелочи сопровождается расщеплением амидов (расщепление по Гофману) и приводит к образованию первичных аминов, имеющих в молекуле на один атом углерода меньше, чем в исходном амиде:
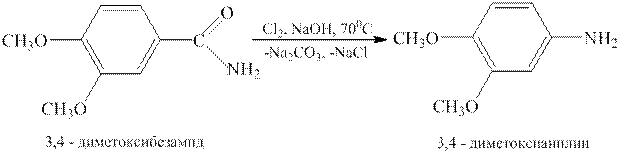
Нитрилы.
Нитрилами (цианидами) называются соединения общей формулы R─ C ≡ N
Нитрилы отличаются по строению от ацильных производных, и к группе функциональных производных карбоновых кислот их относят потому, что они гидролизуются с образованием карбоновых кислот или амидов.
Гидролиз.
Нитрилы относятся к очень слабым ацилирующим агентам, более слабым, чем даже амиды, поэтому они гидролизуются (в кислой или щелочной среде) значительно труднее ацильных производных:
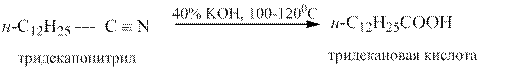
Восстановление.
Нитрилы могут быть восстановлены в первичные амины разными методами – каталитическим гидрированием, натрием в этаноле, алюмогидридом лития, например:
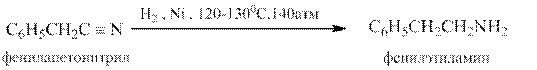
По сравнению с другими функциональными производными карбоновых кислот нитрилы восстанавливаются значительно труднее.
 2020-10-11
2020-10-11 886
886








