Простыми эфирами называют органические вещества, молекулы которых состоят из углеводородных радикалов, соединенных атомом кислорода: R–O–R', где R и R' – различные или одинаковые радикалы.
Простые эфиры рассматриваются как производные спиртов. Названия этих соединений состоят из названий радикалов и слова эфир (название класса). Для симметричных эфиров ROR используется приставка ди перед названием радикала, а в названиях несимметричных эфиров ROR' радикалы указываются в алфавитном порядке. Например, CH3OCH3 – диметиловый эфир; C2H5OCH3 – метилэтиловый эфир.
Симметричные простые эфиры R–O–R получают при межмолекулярной дегидратации спиртов.
При этом в одной молекуле спирта разрывается связь О–Н, а в другой – связь С–О. Реакцию можно рассматривать как нуклеофильное замещение группы HО– (в одной молекуле спирта) на группу RO– (от другой молекулы).
Эфиры несимметричного строения R–O–R' образуются при взаимодействии алкоголята и галогенуглеводорода (синтез Вильямсона). Например, метилэтиловый эфир можно получить из этилата натрия и хлорметана:
C2H5ONa + CH3Cl ® C2H5OCH3 + NaCl
В этой реакции происходит нуклеофильное замещение галогена (Cl–) на алкоксигруппу (CH3O–)
Простые эфиры имеют более низкие температуры кипения и плавления, чем изомерные им спирты. Эфиры практически не смешиваются с водой. Это объясняется тем, что простые эфиры не образуют водородных связей, т.к. в их молекулах отсутствуют полярные связи О–Н.
Простые эфиры – малоактивные соединения, они значительно менее реакционноспособны, чем спирты. Хорошо растворяют многие органические вещества и поэтому часто используются как растворители. Наиболее характерные реакции простых эфиров:
· разложение под действием концентрированных иодоводородной или бромоводородной кислот
R–O–R' + HI ® ROH + R'I
· образование нестойких солей оксония (подобных солям аммония) в результате взаимодействия с сильными кислотами
R2O + HCl ® [R2OH]+Cl-
К важнейшим простым эфирам относятся и гетероциклические кислородсодержащие соединения – этиленоксид (эпоксид) и диоксан.

Диоксан (т. кип. 101°С) – хороший растворитель, смешивается как с водой, так и с углеводородами. За эти качества его назвали "органической водой". Достаточно токсичен. Значительно более опасны галогенсодержащие дибензопроизводные диоксана. Например, печально известный диоксин (2,3,7,8-тетрахлордибензо- п -диоксин).
3. Фенолами называются гидроксиарены или ароматические
гидроксипроизводные.
Фенолы характеризуются более сильными кислотными свойствами, чем спирты, последние в водных растворах не образуют карбониевые ионы AIk – O–, что связано с меньшим поляризующим действием (электроакцепторными свойствами акильных радикалов по сравнению с ароматическими).
Одноатомные фенолы:
  OH OH |  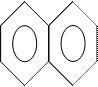 OH OH |
| фенол | α-нафтол |
Спирты и фенолы тем не менее легко образуют водородные связи, поэтому все спирты и фенолы имеют более высокие температуры кипения, чем соответствующие углеводороды.
Если углеводородный радикал не обладает ярко выраженными гидрофобными свойствами, то эти спирты хорошо растворяются в воде. Водородная связь обусловливает способность спиртов переходить при отвердении в стеклообразное, а не кристаллическое состояние.
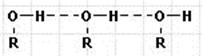
Соединения с двумя и более гидроксильными группами называются многоатомными спиртами и фенолами:
 СН2—ОН СН2--ОН СН2—ОН СН2--ОН |  СН2—ОН СН—ОН СН2—ОН СН—ОН
СН2--ОН | ||||
| 1,2-этандиол (гликоль) | 1,2,3-пропан-триол (глицерин) |
 2014-02-05
2014-02-05 2300
2300
