Катализ гомогенный и гетерогенный. Типы важнейших каталитических процессов. Механизм гомогенного и гетерогенного катализа. Активность и отравляемость катализаторов. Промышленные катализаторы. Активаторы. Носители (трегеры). Оптимальные технологические параметры каталитических процессов. Аппаратурное оформление гомогенных и гетерогенных каталитических процессов.
Катализ - наиболее эффективное средство ускорения большинства химических реакций. С помощью катализаторов не только повышается производительность аппаратуры, но и повышается качество продукции. Катализаторы ускоряют основные реакции (вследствие избирательности) и уменьшают скорость параллельных и побочных процессов. Экономические показатели каталитических процессов значительно выше за счет снижения энергетических затрат (снижается температура процесса).
Катализом называется изменение скорости химических реакций под воздействием катализаторов. Сами катализаторы участвуют в промежуточных реакциях, но восстанавливают свой состав с окончанием акта катализа.
По принципу фазового состояния реагентов и катализатора каталитические процессы различают гомогенные и гетерогенные.
Катализатор может ускорять либо замедлять химическую реакцию, поэтому различают катализ положительный и отрицательный.
Сущность ускоряющего действия катализаторов состоит в понижении энергии активации Е химической реакции в результате изменения реакционного пути.
Катализаторы не смещают равновесия в системе, т.к. увеличивают скорость прямой и обратной реакций в одинаковой мере. Но так как прямая и обратная реакции ускоряются, равновесие достигается значительно быстрее.
На катализаторах помимо основных реакций протекают и побочные, поэтому со временам катализатор теряет свою активность. Активность катализатора есть мера ускоряющего действия его на данную реакцию. Активность, можно выразить величиной Е, разностью скоростей каталитической и некаталитической реакций. Наиболее часто активность катализатора выражают как отношение константы скорости реакции каталитической к константе скорости некаталитической реакции при одинаковых параметрах технологического режима. (С, Р, Т и др.).
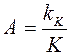
Минимальная температура реакционной смеси, при которой каталитический процесс протекает с достаточной скоростью, называется температурой зажигания. Наиболее желательны процессы с низкой t◦ зажигания, что зависит от активности катализатора.
Важным свойством катализаторов является их отравляемость, т.е. потеря активности под действием посторонних примесей в реакционной смеси, называемых каталитическими ядами. К наиболее типичным ядам относятся соединения серы: H2S, СS2, меркаптаны и другие, окись, углерода, соединения мышьяка, свинца и др.
Катализатор отравляется вследствие сорбции яда на его поверхности. Если сорбция необратима, то и отравляемость катализатора необратима. При обратимой отравляемости катализатора при подаче свежей газовой смеси, лишенной яда, активность его через определенное время восстанавливается.
Катализатор может терять свою активность и из-за спекания своей поверхности, а также в результате осаждения твердых продуктов реакции и пыли.
Некоторые катализаторы обладают избирательностью (селективностью действия), т.е. из нескольких возможных реакций ускоряют только нужную.
В некоторых реакциях катализаторами являются продукты реакции. Такие реакции называются автокаталитическими.
В некоторых реакциях как катализатор действует световая энергия. Это так называемые фотохимические реакции.
ГОМОГЕННЫЙ И ГЕТЕРОГЕННЫЙ КАТАЛИЗ
При гомогенном катализе катализатор и реагирующие вещества находятся в единой фазе (газе или жидкости).
Ускорение процессов при катализе происходит за счет снижения энергии активации в результате образования промежуточного продукта по сравнению с энергией активации образования некаталитического активного комплекса.
Гетерогенный катализ более широко распространен в химической технологии, чем гомогенный. Большинство: гетерогенных каталитических процессов основано на реакциях между газообразными веществами на твердом катализаторе. Механизм ускоряющего действия основан на том, что твердые катализаторы имеют активные центры, т.е. участки поверхности, обладающие повышенной активностью. На этих участках поверхности образуются промежуточные продукты адсорбционного типа. Свойства таких промежуточных продуктов (активных комплексов) влияют на скорость химического превращения, уровень активности катализатора и др. каталитические характеристики.
Катализаторы представляют собой тела с высокоразвитой поверхностью (пористые). Подобный процесс протекает в несколько стадий:
1) диффузия веществ к катализатору;
2) хемосорбция на поверхности катализатора с обрезов ан нем
промежуточных продуктов типа "реагент- катализатор";
3) перегруппировка атомов с образованием промежуточного продукта типа «продукт – катализатор»;
4) десорбция продукта из катализатора;
5) диффузия (отвод) продукта.
Общая скорость лимитируется наиболее медленной частью (стадией). Если наиболее медленные - диффузионные стадии, то процесс протекает в диффузионной области. Если наиболее медленны стадии 2, 3, 4, то процесс протекает в кинетической области.
Свойства твердых катализаторов. Контактные массы
К твердым катализаторам предъявляется ряд требований: активность, стойкость к действию контактных ядов, низкая стоимость, термостойкость, механическая прочность и т.д. Поэтому чаще всего на производстве используют в качестве катализаторов не индивидуальные соединения, а сложные механические смеси, называемые контактными массами.
В состав контактной массы входят, главным образом, 3 составляющие:
- собственно катализатор;
- активатор (промотор);
- носитель (трегер).
Промоторы добавляются для повышения активности катализатора, хотя сами они не обладают каталитическими свойствами. Механизм действия промоторов заключается в том, что они образуют соединения с катализатором, которые обладают повышенной каталитической активностью. Промотор может увеличивать поверхность каталитически активного вещества, повышать термостойкость катализатора, а также иногда уменьшать обновляемость катализатора.
Носители (трегеры) - термостойкие инертные пористые вещества, на которые наносят катализатор. Носители создают пористость контактной массы, увеличивают её механическую прочность и термостойкость, экономят расход дорогого катализатора. Наиболее распространены носители: окись Al, силикагель, алюмосиликат, пемза, кизельгур, уголь и т.д.
Основным методом приготовления контактных масс является осаждение металлов в виде гидроокисей на носители с последующей термической обработкой.
Так как каталитический гетерогенный процесс протекает на поверхности контактной мессы, поэтому основной характеристикой контактным масс является величина удельной поверхности S уд., т.е. поверхность единицы веса или объема катализатора. Для промышленных катализаторов Sуд составляет от нескольких десятков до сотен м2/г.
Контактную массу выпускают в виде таблеток, зерен, цилиндриков, колец и т.д. В ряде случаев контактные массы готовят в виде сеток из сплавов различных металлов.
 2014-02-02
2014-02-02 3280
3280
