Коагуляция – процесс слипания частиц дисперсной фазы с образованием крупных агрегатов.
Коагуляция является следствием нарушения агрегативной устойчивости лиофобных золей. В результате коагуляции система теряет свою седиментационную устойчивость, так как частицы становятся слишком крупными и не могут участвовать в броуновском движении. Разрушение коллоидной системы идет в следующей последовательности:
Нарушение Нарушение
агрегативной → Коагуляция → седиментационной
устойчивости устойчивости
Коагуляция идет самопроизвольно, так как приводит к уменьшению межфазной поверхности, а следовательно, и к снижению свободной поверхностной энергии (G пов = s S).
Различают две стадии коагуляции:
1) медленная (скрытая) коагуляция: частицы укрупняются, но не теряют седиментационной устойчивости;
2) быстрая (видимая) коагуляция: частицы теряют седиментационную устойчивость, при этом, если плотность частиц больше плотности дисперсионной среды, образуется осадок.
Количественной характеристикой коагуляции является скорость коагуляции. Скорость коагуляции vк – это изменение концентрации коллоидных частиц 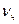 в единицу времени τ при постоянном объеме системы:
в единицу времени τ при постоянном объеме системы:
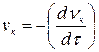 .
.
Знак “–“ стоит перед производной, так как концентрация частиц со временем уменьшается, а скорость всегда положительна.
Чтобы началась коагуляция, частицы должны преодолеть потенциальный барьер Δ Uк. Для этого необходимо уменьшить z-потенциал. Экспериментально установлено, что коагуляция начинается при |z| £ 30 мВ.
Как можно уменьшить z-потенциал?
1) снизить температуру;
2) добавить электролиты.
Рассмотрим механизм коагуляции гидрофобного золя электролитами.
 2014-02-02
2014-02-02 935
935








