Т еплоемкость – это количество теплоты, необходимое для нагревания единицы массы вещества на 1 К.
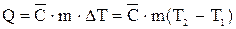 (26)
(26)
Теплоёмкость,рассчитанная на 1 моль вещества, называется молярной, а на единицу массы – удельной.
Размерность удельной теплоемкости  .
.
Размерность молярной теплоемкости 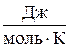 .
.
Различают также понятия истинной и средней теплоемкостей.
Средней молярной теплоемкостью 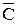 в интервале температур Т1 ¸ Т2 называется отношение конечного количества теплоты Q, которое необходимо подвести к 1 моль вещества, чтобы изменить его температуру от Т1 до Т2, к разности температур Т2 – Т1:
в интервале температур Т1 ¸ Т2 называется отношение конечного количества теплоты Q, которое необходимо подвести к 1 моль вещества, чтобы изменить его температуру от Т1 до Т2, к разности температур Т2 – Т1:
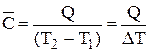 . (27)
. (27)
Истинная молярная теплоемкость С – это отношение бесконечно малого количества теплоты dQ, которое нужно подвести к 1 моль вещества, чтобы повысить его температуру на бесконечно малую величину dT, к этому бесконечно малому приращению температуры:
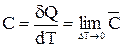 (28)
(28)
Существуют также теплоемкости при постоянном объеме (изохорная теплоемкость, СV) и постоянном давлении (изобарная теплоемкость, СР).
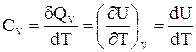 ,
,
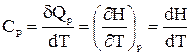 . (29)
. (29)
Следует знать, что теплоёмкость при постоянном давлении Ср больше, чем теплоёмкость при постоянном объёме СV, так как нагревание вещества при постоянном давлении сопровождается работой расширения, т.е.
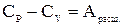 (30)
(30)
Для идеальных газов справедливо уравнение Майера:
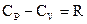 (31)
(31)
Величина R (универсальная газовая постоянная) равна работе расширения 1 моль идеального газа (при р = const) при увеличении его температуры на 1 градус. (R=8,314 Дж/(моль∙К)
В справочниках приведены значения стандартной молярной изобарной истинной теплоемкости С0р, 298, а также средней молярной изобарной теплоемкости (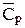 ).
).
Теплоемкость любого вещества - это свойство, зависящее от температуры. Эту зависимость нельзя предсказать теоретически, она определяется экспериментально с помощью специальных устройств – калориметров.
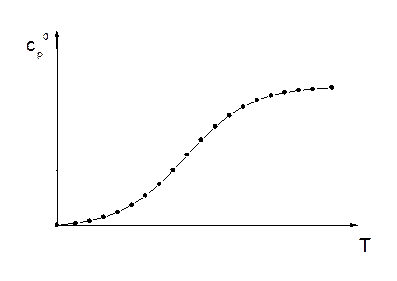 |
Обычно для температур выше комнатной температурную зависимость теплоемкости записывают в виде следующих полиномов:
С0р = а + bТ + сТ2
или С0р = а+ bТ + 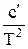 . (32)
. (32)
 2014-02-02
2014-02-02 7209
7209
