Ферменты обладают рядом общекаталитических свойств:
· не смещают каталитическое равновесие
· не расходуются в процессе реакции
· катализируют только термодинамически реальные реакции. Такими реакциями являются те, в которых исходный энергетический запас молекул больше, чем финальный.
В ходе реакции преодолевается высокий энергетический барьер. Разница между энергией этого порога и исходным энергетическим уровнем - энергия активации.
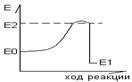
Скорость ферментативных реакций определяется энергией активации и рядом других факторов.
Константа скорости химической реакции определяется по уравнению:
К = P*Z*e- (Ea/RT)
К - константа скорости реакции
Р – пространственный (стерический) коэффициент
Z – количество взаимодействующих молекул
Еа – энергия активации
R – газовая постоянная
Т – универсальная абсолютная температура
е – основание натуральных логарифмов
В этом уравнении Z, е, R, T – постоянные величины, а Р и Еа - переменные. Причём, между скоростью реакции и стерическим коэффициентом зависимость прямая, а между скоростью и энергией активации – обратная и степенная зависимость (чем ниже Еа, тем выше скорость реакции).
Механизм действия ферментов сводится к увеличению ферментами стерического коэффициента и уменьшению энергии активации.
 2014-02-02
2014-02-02 961
961








