Важным показателем структуры полимеров является молекулярная масса. В реальном полимере не бывает, чтобы все макромолекулы имели бы одинаковые размеры и равные молекулярные массы. Существуют определенные распределения макромолекул по этим свойствам внутри данного образца полимера, зависимые, в основном, от условий синтеза полимера.
Распределения по молекулярным массам могут быть обработаны статистически. Можно получить несколько средних величин, пригодных для общего описания средней степени полимеризации и средней молекулярной массы. Наиболее важными являются среднечисловая и среднемассовая молекулярные массы.
В приближении, применимом для полимерных образцов с высокой степенью полимеризации, отношение между средней молекулярной массой (М) и средней степенью полимеризации (n) постоянно:
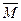 =М0 n,
=М0 n,
где Мо - постоянная величина, примерно равная молекулярной массе звена.
Среднечисловая молекулярная масса Мn вычисляется по формуле:
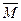 n=
n=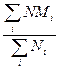 , (2)
, (2)
где Ni - число молекул сорта i, имеющихся в смеси; Mi - их молекулярная масса. Суммирование производится по всем сортам молекул в смеси.
Вместо числа молекул Ni можно использовать число молей тi или мольную долю.
Среднемассовая молекулярная масса Mw получается путем сложения числа граммов g i полимера, молекулы которого имеют молекулярную массу Mi умноженного на эту молекулярную массу, и деления на общую массу полимера в граммах. В этом случае мы также можем использовать массовую долю W. Поэтому
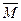 w=
w= 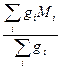 =
= 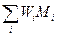 (3)
(3)
Полимер, у которого все молекулы имеют одинаковые массы (М w = М п) называется монодисперсным. Реальные полимеры полидисперсны, так как имеют определенный разброс по молекулярным массам. Отношение М w: Мп используют для оценки разброса молекулярных масс. Чем это отношение больше, тем больше этот разброс и шире дисперсия по молекулярным массам.
Например, смесь из равных количеств двух сортов молекул молекулярными массами 1000 и 100000 соответственно имеет Мw=99020; Мп =50500 и М w/ Мп = 1,96. Если взять равные по массе количества тех же молекул Mw=50500, а Мп=1,980, то Mw/Mп=25,5.
Если макромолекулы полимера имеют линейное строение, то параметры Мw, Мп и Мw/Мп достаточно полно характеризуют топологию системы.
Если макромолекулы разветвлены, то необходимо использовать дополнительные параметры для оценки этой разветвленности. Это усложняет описание системы, однако в принципе это возможно.
Как известно, полимеры, имеющие линейные или разветвленные макромолекулы, являются термопластичные полимерами (термопластами). Термопластичные материалы обратимо изменяют свойства при изменении температуры. При повышении температуры они размягчаются и могут находиться в текучем состоянии и при охлаждении делаются твердыми. Эти полимеры растворимы в соответствующих растворителях. Типичные термопласты – это полиэтилен, поливинилхлорид, капрон, полиметилметакрилат (оргстекло) и т.д.
Вместе с тем существует большая группа полимеров, у которых молекулы имеют сетчатое строение, т. е. весь объем полимера пронизан ковалентными связями между атомами. Эти полимеры называют термореактивными (реактопласты). Реактопласты не имеют текучего состояния, они не растворимы, а могут лишь набухать в растворителях.
В отношении реактопластов теряет смысл понятие молекулярной массы, так как весь образец материала можно рассматривать как одну молекулу. К реактопластам относится резины, отверждённые фенолоформальдегидные, эпоксидные, полиэфирные, кремнийорганические смолы и композиции на их основе.
Топологическая оценка структуры сетчатых полимеров требует другого подхода. Наиболее важной структурной характеристикой этих полимеров является величина средней молекулярной массы полимерной цепи между узлами структурной сетки Мс. Величину Мс можно теоретически рассчитать и определить экспериментально с помощью независимых методов. Более того, в ряде случаев Мс может быть задано и реализовано в ходе синтеза и перера6отки полимера.
1.3. Надмолекулярная структура полимеров.
В результате действия водородных и межмолекулярных сил макромолекулы полимеров, так же как и молекулы низкомолекулярных соединений в конденсированном состоянии, вступают во взаимодействие друг с другом и образуют агрегаты различной степени сложности и с разным временем жизни. Строение агрегатов зависит от химического состава взаимодействующих мономерных звеньев макромолекул, числа и размера атомов или групп, условий (температура, давление, среда и др.). Наиболее устойчивы структуры, в которых число межмолекулярных и водородных связей максимально. В ряде случаев отдельные макромолекулы объединяются во вторичные образования, вторичные — в образования третьего и четвертого порядка. Физическая структура полимерных тел, обусловленная различными видами упорядочения во взаимном расположении макромолекул, называется надмолекулярной структурой.
Изучение надмолекулярной структуры полимеров определяет комплекс их физических свойств, скорость и механизм физико-химических и химических процессов. Вследствие различий в надмолекулярной структуре часто изделия из одного и того же полимера имеют разные свойства.
Влияние надмолекулярных структур на формирование свойств можно проиллюстрировать на примере алмаза и графита — неорганических полимеров, образованных из атомов углерода. Алмаз представляет собой пространственный алифатический полимер кристаллического строения. Каждый атом углерода связан четырьмя ковалентными связями с четырьмя другими атомами в трех направлениях. Длина связей равна длине обычной простой σ-связи С—С, т. е. 0,154 нм. Строение кристаллической решетки алмаза показано на рис. 3, а. Образованные из атомов углерода, лежащих в одной плоскости, циклогексановые циклы имеют конформацию «кресла» (рис. 3,6). Расстояние между атомами ra равно 0,205 нм. Этот полимер отличается чрезвычайно высокой прочностью, твердостью, стойкостью к агрессивным средам.
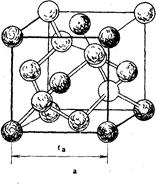 | 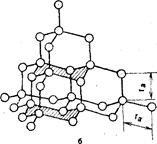 | 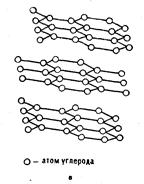 |
| Рис. 3. Надмолекулярная структура алмаза (а, б) и графита (в): а — кристаллическая решетка из атомов углерода; б — кресловидные конформации в плоскостях циклогексановых циклов (заштрихованы два цикла, два цикла в нижней плоскости не заштрихованы); r a — расстояние между атомами С в кристаллической решетке |
У всех атомов углерода четвертые валентные электроны не локализованы. Они образуют «электронный газ» и могут перемещаться внутри плоскости, обеспечивая хорошую электрическую проводимость. Слои расположены друг от друга на расстоянии 0,34 нм и связаны относительно слабыми межмолекулярными силами. Это обусловливает низкую прочность, способность скольжения слоев один по другому (рис. 3, в). Переход электронов из одной плоскости в другие затруднен, вследствие чего электропроводимость графита анизотропна: проводимость вдоль плоскостей в 1014 раз выше, чем поперек плоскостей.
Наиболее разнообразными являются надмолекулярные структуры органических полимеров. По степени упорядоченности элементов надмолекулярных структур их можно разделить на две группы: аморфные и кристаллические. Критерием такого разделения может служить дифракция рентгеновских лучей или электронов, характеризующая степень упорядоченности структур. В кристаллических полимерах, как правило, существует трехмерный дальний порядок в расположении атомов, звеньев и цепей. Аморфные полимеры характеризуются ближним порядком лишь в расположении звеньев. Дальний порядок в расположении звеньев и цепей у них отсутствует. Однако такое деление отнюдь не означает, что аморфные полимеры беспорядочны и бесструктурны, а кристаллические – имеют бездефектную кристаллическую структуру.
 2014-02-02
2014-02-02 2610
2610
