Серная кислота
Получение оксида серы (VI)
Химические свойства оксида серы (VI)
Физические свойства оксида серы (VI)
При плавлении образуется жидкость, состоящая, главным образом, из тримеров.
При обычных условиях триоксид серы – бесцветная жидкость.
- Серный ангидрит термически неустойчив. Его разложение начинается при 450 °С, а при 1200 °С в газовой фазе полностью отсутствуют молекулы SO3:
2SO3 = 2SO2 + O2.
- Бурно взаимодействует с водой с выделением большого количества тепла. Газообразный триоксид серы плохо поглощается водой, так как образуется туман:
nSO3 + H2O = H2SO4· nSO3 (олеум).
- Проявляет свойства типичного кислотного оксида:
SO3 + CaO = CaSO4;
SO3 + NaOH = NaHSO4;
SO3 + 2NaOH = Nа2SO4 + Н2О.
- Серный ангидрит – одно из самых реакционноспособных соединений. Он проявляет только окислительные свойства, например:
2SO3 + C = 2SO2 + CO2;
2SO3 + 2HBr = SO2 + Br2 + H2SO4.
В промышленности производится в огромных масштабах с целью получения серной кислоты:
2SO2 + O2 = 2SO3 (450 °C, катализатор V2O5).
В лаборатории получают термическим разложением некоторых сульфатов:
Fe2(SO4)3 = Fe2O3 + 3SO3.
При растворении триоксида серы в воде образуется сильная серная кислота – один из важнейших продуктов химического производства.
Неразбавленная серная кислота представляет собой ковалентное соединение.
В молекуле серная кислота тетраэдрически окружена четырьмя атомами кислорода, два из которых входят в состав гидроксильных групп. Связи S – O – двойные, а S – OH – одинарные.
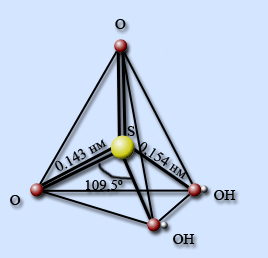
Бесцветные, похожие на лед кристаллы имеют слоистую структуру: каждая молекула H2SO4 соединена с четырьмя соседними прочными водородными связями, образуя единый пространственный каркас.
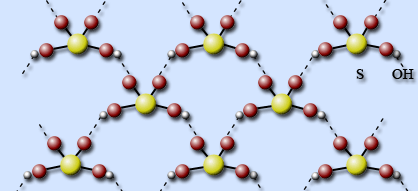
Структура жидкой серной кислоты похожа на структуру твердой, только целостность пространственного каркаса нарушена.
 2014-02-02
2014-02-02 2685
2685








