Введение.
Вопросы лекции:
· Уравнения Гиббса.
· Термодинамические потенциалы.
· Условия термодинамического равновесия однофазной системы.
· Условия термодинамического равновесия многофазных систем.
· Правило фаз Гиббса.
3. Заключение.
К следующему занятию курсанты должны:
ЗНАТЬ: фундаментальные уравнения Гиббса; правило фаз Гиббса; правила расчета термодинамических параметров в частных случаях процессов водяного пара.
УМЕТЬ: применять математический аппарат термодинамики и метод диаграмм сухого и влажного пара к расчету процессов водяного пара; строить графики процессов водяного пара в p-v, T-s, i-s координатах.
ИМЕТЬ ПРЕДСТАВЛЕНИЕ: о методе термодинамических потенциалов и о своеобразии диаграмм двухфазных состояний "жидкость - пар".
4. Задания на самоподготовку:
· конспект лекций
· понятие о таблице свойств воды и водяного пара, см. Приложение 4, ТЕПЛОТЕХНИКА: Учебный справочник / Под ред. д.т.н., проф. Н.М. Барбина. Екатеринбург: УрИ ГПС МЧС России, 2009.
Подпись автора
_____________/ профессор каф. физики и теплообмена, д.ф.-м.н., П.В. Скрипов
Лекция рассмотрена и одобрена на заседании кафедры
Протокол №_______ от «_____»_____________ 2010 г.
Заведующий кафедрой физики и теплообмена
профессор, д.т.н. __________________ / Н.М. Барбин
«_____»______________ 2010 г.
I и II начала ТД и математические свойства дифференциалов теплоты, работы, внутренней энергии, энтальпии, энтропии позволяют развить формализм исследования термодинамических свойств веществ и процессов изменения их состояния. Начала ТД могут быть записаны совместно в одной из форм:
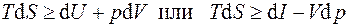 , (4.1)
, (4.1)
где знак равенства относится к обратимым процессам, а знак неравенства - к необратимым. В случае обратимых процессов эти соотношения носят название термодинамических тождеств или фундаментальных уравнений Гиббса:
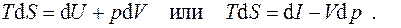 (4.2)
(4.2)
Из уравнений Гиббса можно получить несколько важных для практических целей результатов. Запишем для этого (4.2) в виде
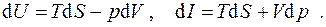 (4.3)
(4.3)
Применив к этим выражениям преобразование Лежандра по переменным 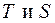 , т.е.
, т.е. 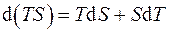 , получим
, получим
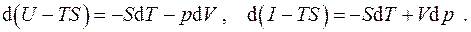
Новые функции состояния
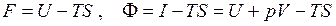 (4.4)
(4.4)
носят названия свободной энергии Гельмгольца (F) и свободной энергии Гиббса ( Φ ). Получили ещё две дифференциальные формы:
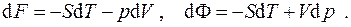 (4.5)
(4.5)
 2014-02-03
2014-02-03 1022
1022








