Основным результатом исследования явилась сравнительная характеристика летальности в группах исследования. При гнойном РП релапаротомия выполнялась в 40,6%; при фибринозном РП – 4,7%; при серозном РП – 0%. Общая летальность в группе составила 16,53%. При гнойном РП – 32,3%. В группе пациентов, которым применён альтернативный метод лечения – программированная релапаротомия, обследовано 58 пациентов; только у двух из них был диагностирован тотальный фибринозный перитонит, потребовавший плановой повторной санации брюшной полости. Основными показаниями к переходу на альтернативную тактику был гнойный РП с высокой степенью бактериальной агрессии, связанной с распространённостью воспаления брюшины и симптомами интоксикации. Летальность составила 25,86%. Дооперационный SIRS-синдром диагностирован у 50 (86,2%) пациентов.
Обработка данных позволяет раскрыть прогностические и дискриминационные свойства критериев новыми статистическими методами. Неизменные параметры характеризуют базисные различия в изучаемых группах и подгруппах исследования, возможности сопоставления результатов лечения без учёта данного критерия. Полученные данные свидетельствуют о достоверных различиях среднего возраста в основных группах сравнения (ТМ 46,8; SEM [0,82] и ПР 39,8; SEM [1,95]; t=0,002), как в генеральных совокупностях, так и при гнойном экссудате (ТМ 49,4; SEM [1,26] и ПР 39,8; SEM [2,01]; t=0,002): что объясняется субъективным отбором пациентов для выполнения ПР. Внутригрупповых различий в соответствии с видом экссудата в ТМ-группе не установлено. При традиционном хирургическом лечении достоверных различий возраста в подгруппах, сформированных в зависимости от констатации прогрессирования РП, не выявлено (t=0,250). При сравнении подгрупп, разделённых по варианту исходов, как в ТМ-группе (t=0,000), так и в ПР-группе (t=0,006) отмечены достоверные различия среднего возраста. На основании полученных результатов можно предположить статистически значимое влияние возраста на исход заболевания в обеих группах исследования. Дискриминационные свойства шкалы [возраста пациента] в отношении исхода лечения в ТМ-группе оценивались по площади под ROC-кривой и составили 0,754 при SEAREA 0,03 (рис.12.9,12.10), что является достоверно хорошим результатом и включает [возраст пациента] в число наиболее информативных предикторов. В отношении прогрессирования перитонита дискриминационные свойства шкалы достоверно отсутствуют (ROCAUC 0,500; SEAREA 0,03).
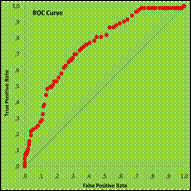
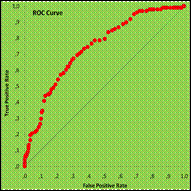
Рис.12.9. Критерий - [Возраст]. Зависимый параметр – [Исход лечения].
ROC-Curve. ТМ+ПР-группа. ROCAUC 0,741; SEAREA 0,03.
Рис.12.10. Критерий - [Возраст]. Зависимый параметр – [Исход лечения].
ROC-Curve. ТМ-группа ROCAUC 0,754; SEAREA 0,03.
Прогностические возможности [возраста пациента] в ТМ-группе в отношении исхода, определённые при помощи критерия χ2 (75,7; p=0,000), критерия сопряженности Пирсона (0,96), критерия Чупрова (0,76) оценены как высокие. Дискриминационные свойства возрастной шкалы присутствуют в ТМ-группе при гнойном экссудате (ROCAUC 0,733; SEAREA 0,04); фибринозном экссудате (ROCAUC 0,801; SEAREA 0,10), серозном экссудате (ROCAUC 0,916; SEAREA 0,09), однако, высокий уровень значимости полученных результатов достигнут только при гнойном экссудате. Прогностические свойства в отношении исхода лечения при всех видах экссудата высокие. Отмечены высокие дискриминационные свойства шкалы возраста в ПР-группе (ROCAUC 0,731; SEAREA 0,08) в отношении исходов, но при низком уровне значимости результатов. Хорошие прогностические характеристики в отношении исходов доказываются только критерием сопряжённости Пирсона (0,90). Примером реализации метода ROC-analysis служит построение ROC-curve, площадь по которой отражает степень дискриминационной способности исследуемой шкалы.
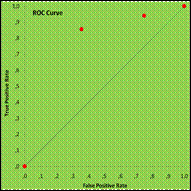
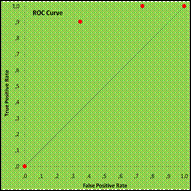
Рис.12.11. Критерий - [Экссудат]. Зависимый параметр – [Исход лечения].
ROC-Curve. ТМ-группа. ROCAUC 0,749; SEAREA 0,03.
Рис.12.12. Критерий - [Экссудат].
Зависимый параметр – [Прогрессирование перитонита].
ROC-Curve. ТМ-группа ROCAUC 0,790; SEAREA 0,03.
Критерий [возраст пациента] в генеральных ТМ- и ПР- совокупностях обладает не самыми высокими прогностическими и дискриминационным свойствами и может быть ограниченно использован для определения вероятности летального исхода, как одиночный предиктор, так и в качестве составляющей совокупности предикторов. Интересным является доказательство влияния характера перитонеального экссудата на исход лечения перитонита. Очевидные выводы подкрепляются новыми статистическими методами. Как постоянный критерий, определяющий исход лечения, фактор [перитонеального экссудата] (рис.12.11,12.12) понятен и известен со времени создания первых классификаций перитонита, основанных на стадийности развития воспаления брюшины [В.Я.Шлапоберский, 1958; К.С.Симонян, 1971; Б.Д.Савчук, 1979; В.Д.Фёдоров, 1974; М.И.Кузин, 1978].
Предполагаемая градация видов экссудата по стадиям развития воспаления, возможная только в ТМ-группе, взята в основу ранжирования для проведения Receiver Operating Characteristic Analysis.
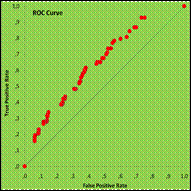
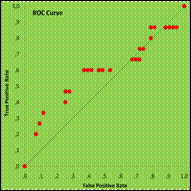
Рис.12.13. Критерий - [Время развития перитонита].
Зависимый параметр – [Исход лечения]. ТМ-группа.
ROCAUC 0,650; SEAREA 0,03.
Рис.12.14. Критерий - [Время развития перитонита].
Зависимый параметр – [Исход лечения]. ПР-группа.
ROCAUC 0,585; SEAREA 0,09.
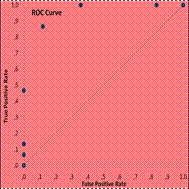 | 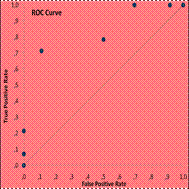 |
Рис.12.15. Критерии – таблица 4 прил. ПР-группа.
Зависимый параметр – [исход лечения].
Дооперационное обследование. (ROCAUC 0,944; SEAREA 0,010).
Рис.12.16. Критерии – таблица 5 прил. ПР-группа.
Зависимый параметр – [исход лечения].
Первые хирургические сутки. (ROCAUC 0,822; SEAREA 0,027).
Полученные данные отражают достаточно высокие дискриминационные свойства параметра [перитонеальный экссудат] при традиционном методе лечения в отношении исхода лечения и прогрессирования перитонита (рис.12.11,12.12) при высоком уровне значимости полученных результатов и незначительной калибровке кривой.
Таким же образом протестирован критерий [время заболевания]. Данный параметр анализируется в соответствии с субъективными данными анамнеза заболевания. В ТМ-группе среднее время развития заболевания составило 45,8ч SEM [2,8]; в ПР-группе – 55,4ч [8,0]. Достоверных различий этого критерия между генеральными совокупностями не отмечено (t=0,263).
Учитывая объём исследования, достоверные различия среднего времени развития болезни отмечены только между ТМ-подгруппами с летальным и витальным исходами (t=0,004), что отражает прогностические свойства критерия в отношении исхода. Имеется выраженная корреляция между временем развития РП и стадийностью воспаления брюшины, отражённой в соответствии с известными классификациями экссудата. Дискриминационные свойства шкалы выражены слабо, что, конечно, находится в обратной зависимости от качества лечения при самых тяжёлых формах заболевания (рис.12.13,12.14).
Данные ROC-analysis и значения χ2 имеются в ряде представленных специальных сводных таблиц (таблицы 1-3 прил.).
Избранные для исследования критерии полиорганной дисфункции не всегда являются определяющими в оценке состояния пациентов. Поиск наиболее информативной комбинации симптомов, обладающих наибольшим дискриминирующим потенциалом – одна из составляющих исследовательской работы. Для проведения тестирования программными средствами проведено тестирование комбинаций критериев по заданным промежуткам их значений. Базисный набор значений включает показатели, отражающие норму (таблица 12.10), описанную в литературных источниках. Принадлежность к программированному, выходящему за рамки описанной нормы, интервалу параметра оценивается как «1»; остальные как «0». Сумма баллов является параметром, в отношении которого определяется дискриминационная возможность. Так проводится поиск составляющих шкалы с весовой ценностью одного критерия равной «1». В качестве тестируемой подгруппы избрана ТМ-подгруппа с гнойным РП.
Следующим этапом исследования было определение межгрупповых дискриминационных максимумов, т.е. набора критериев в данный момент времени, при отклонении от нормы которых, маркируемое как «1» составляет шкалу, имеющую наибольшую дискриминационную силу в отношении исходов и прогрессирования перитонита. Опуская рутинную работу и промежуточные выводы, представляем межгрупповые дискриминационные максимумы в ТМ и ПР-группах.
Особое внимание уделено максимальным достоверным значениям ROCAUC и значениям, превышающим ROCAUC 0,8. Дискриминационные свойства шкалы при достоверном ROCAUC >0,899 обозначались очень высокими, при достоверном ROCAUC >0,749 обозначались высокими. Для подтверждения итогов исследования была использована demo-версия программы MedCalc, в ходе работы с которой проверялись основные результаты.
Были определены основные этапы статистической обработки и этапов прогнозирования. Правильное понимание разграничения этих понятий обеспечивает разработку правильного алгоритма действий при принятии клинических решений. На первом этапе статистического анализа проведен сбор данных и представление их в динамике послеоперационного периода, проведено программирование, позволившее в автоматическом режиме выбирать критерии для работы с базой данных. Применение для сравнения групп и подгрупп исследования t-критерия Стьюдента было дополнено изучением дискриминационных и прогностических свойств по различным направлениям исследования.
Этапы прогнозирования тесно взаимосвязаны с алгоритмом принятия клинических решений. Дооперационный этап затрагивает всю (генеральную) совокупность пациентов, оперированных по поводу РП. На этом этапе не известен вид экссудата, не известны другие характеристики повреждения систем органов. Имеющийся диагностический материал относится ко всей когорте пациентов без какой-либо дифференцировки по хирургической тактике. На этом этапе одиночные диагностические параметры отражают общебиологические закономерности возникновения и прогрессирования болезни, которые по нашему предположению влияют на конечный исход лечения независимо от предпринятых в дальнейшем лечебных мероприятий. Поэтому, на данном этапе, задачами прогнозирования, проведённого по любой конкретной методике, является определение наиболее значимых для прогноза параметров с целью воздействия на них на дооперационном этапе - при подготовке к операции. В клинической практике появление негативных симптомов должно мотивировать медицинский персонал на проведение качественной предоперационной подготовки, тщательный выбор методов обезболивания и, в конечном счёте, проведение адекватного по объёму оперативного вмешательства. Индивидуальный прогноз с определением вероятности летального исхода в этих случаях не является клинико-сатистической задачей, поскольку не учитывает основных факторов, влияющих на качество прогностической модели: вид экссудата и избранную хирургическую тактику. Определение совокупности предикторов, оптимально определяющей прогноз возможно. Применение качественной прогностической модели для расчёта вероятности летального исхода дифференцирует мотивацию применения альтернативных (более эффективных) протоколов лечения в случаях, когда прогнозируемая летальность превышает средние цифры наблюдаемой летальности при РП.
Рис.12.17. Сравнение летальности (%), в ТМ- и ПР-группах исследования
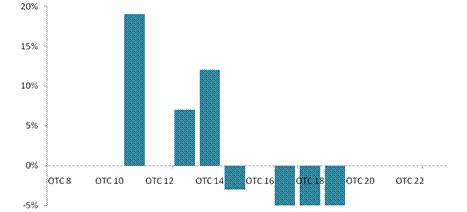 при гнойном РП
при гнойном РП
В интервале балла шкалы ОТС [11-14] наблюдается преимущество ПР-метода
Интраоперационный этап прогнозирования можно считать основным, поскольку основные клинические проблемы решаются именно в этот период. На момент проведения операции известны и могут быть использованы все предшествующие результаты обследования. Верификация вида экссудата приводит к сужению прогностических задач, определению наиболее важных направлений прогнозирования, среди которых – прогноз исходов и осложнений при гнойном РП. Методика анализа, разумеется, предусматривает возможность изучения прогноза при любом виде экссудата, однако, важным элементом клинического прогнозирования является концентрация усилий на наиболее проблемных направлениях. Для определения прогностической модели в этой подгруппе выделяется когорта пациентов с гнойным РП. Определяются классификационные характеристики прогностической модели и возможности её применения. При помощи неё проводится сравнение прогнозированной и наблюдаемой летальности с целью коррекции лечебных мероприятий. Учитывая, что принципы проведения первой операции при гнойном РП практически идентичны при всех тактических вариантах, окончательное определение объёмов и кратности хирургического пособия может проводиться в течение 1-2 послеоперационных суток. На этом этапе прогнозирования возможна дифференцировка хирургической тактики при помощи балла шкалы ОТС. Для этого применяется сравнение наблюдаемой летальности в ПР- и ТМ-группах исследования, стратифицированной по баллу шкалы оценки тяжести состояния или собственной шкалы предикторов.
После определения составных частей совокупности предикторов, наиболее полно дискриминирующей исход лечения, определяются баллы шкалы для каждого случая с РГП. В дальнейшем путём регрессионного анализа определяются параметры уравнения, описывающего зависимость балла шкалы и вариантов исхода отдельно в ТМ- и ПР-группах. При выявлении высокой степени дискриминации исходов эти модели могут быть применены для индивидуального прогноза в соответствующих группах. Однако, совокупность предикторов, наиболее точно описывающая прогноз исходов РГП до выбора метода хирургического лечения может отличаться от набора предикторов, предназначенных для прогнозирования отдельно в ТМ- и ПР-группах. В тех случаях, когда подобранная совокупность обладает лучшим качеством прогнозирования в ТМ- или ПР-группе, чем совокупность, определённая для прогнозирования при РГП в целом, она более пригодна для индивидуального прогноза в соответствующей (ТМ- или ПР-) группе. Существует вероятность того, что доказать преимущества ТМ- или ПР-модели не удаётся. В этих случаях индивидуальный прогноз и дифференцировка хирургической тактики должна проводиться при помощи общей для РГП модели.
Рис.12.18. Сравнение летальности (%), (результаты Z-тестирования)

В интервале балла шкалы ОТС [11-14] наблюдается преимущество ПР-метода
После определения прогноза при помощи ТМ- и ПР-модели предполагается возникновение необходимости подтверждения избранных тактических вариантов. Оно может быть осуществлено путём определения динамики вероятности летального исхода в первые 24-48 часов, то есть до первой программированной релапаротомии. По аналогии с предыдущими этапами, на основании диагностики первых послеоперационных суток определены прогностические модели отдельно для ТМ+ПР-, ТМ- и ПР-групп, а также рассчитывались индивидуальные прогнозы. Для окончательного выбора прогностической модели первых послеоперационных суток оцениваются классификационные свойства и качество моделей. В дальнейшем прогнозированная летальность сравнивается не только между ТМ- и ПР-группами для выбора хирургической тактики, но измеряется динамика индивидуального прогноза. Причиной уменьшения прогнозированной летальности может быть эффективность предшествующего хирургического и реаниматологического пособия. В этих случаях окончательное решение наиболее трудно. Представленный алгоритм анализа и практических решений может служить дополнительным инструментом для определения лечебных мероприятий при РП.
Таблица 12.10
Указатель границ значений критериев, используемых при создании шкалы
| Предиктор | Границы параметров | Единицы измерения | |
| Систолическое артериальное давление | мм Hg | ||
| Диастолическое артериальное давление | мм Hg | ||
| Ректальная температура, С | 35,9 | 39,1 | Градусы С |
| Частота дыхательных движений | / мин | ||
| Лейкоциты крови | /мкл | ||
| Частота сердечных сокращений | / мин | ||
| Среднее артериальное давление | мм Hg | ||
| Балл шкалы комы Glasgow | Баллы | ||
| Оксигенация, SpO2 | у.е., % | ||
| Гематокрит | 29,9 | л/л | |
| Калий | 3,49 | ммоль/л | |
| Натрий | ммоль/л | ||
| Креатинин | 0,59 | 1,41 | мг/100мл |
| Возраст | Годы | ||
| Время развития заболевания | Часы | ||
| Индекс IPM | -1 | Баллы | |
| Число симптомов SIRS | -1 | Баллы | |
| Число симптомов SPOD | -1 | Баллы | |
| Балл шкалы ОТС | Балл | ||
| Систолический объём сердца | 39,99 | 75,01 | мл |
| Минутный объём сердца | мл | ||
| Среднее динамическое давление | 79,999 | 110,001 | мм Hg |
| Общее периферическое сопротивление сосудов | 1199,99 | 2500,01 | дин-см-сек |
| Среднее давление в лёгочных артериях | 24,99 | 55,01 | мм Hg |
| Коэффициент Кваса | 14,99 | 17,01 | у.е. |
Определение наиболее оптимальной хирургической тактики основывается на следующих принципах: применение традиционного метода является наиболее обоснованным при отсутствии существенного отличия в результатах лечения; применение альтернативного метода наиболее обосновано даже тогда, когда результаты лечения наиболее тяжёлых пациентов одинаково неблагоприятны (за исключением случаев неизбежной интраоперационной смерти, агонального состояния).
Таблица 12.11. Этапы прогнозирования исходов лечения РП
| Этап прогнозирования | Изучаемые явления | Группы исследования | Статистический метод | Хирургическая тактика до прогнозирования |
| Дооперационный | Индивидуальные прогностические свойства предикторов | ТМ+ПР | t-критерий, ROC-анализ, χ2 Пирсона, НП χ2 | Не определена |
| Прогностические свойства шкал без учёта вида экссудата | ТМ+ПР | ROC-анализ, НП χ2, χ2 Пирсона, регрессионный анализ | Не определена | |
| Интраоперационный | Прогностические свойства шкал с учётом вида экссудата. Определение преимуществ видов хирургической тактики. | ТМ+ПР | ROC-анализ, НП χ2, регрессионный анализ, χ2 Пирсона, сравнение результатов прогнозирования | Не определена |
| ТМ | Определена | |||
| ПР | Определена | |||
| Первые хирургические сутки | Индивидуальные прогностические свойства предикторов | ТМ+ПР | t-критерий, ROC-анализ, χ2 Пирсона, НП χ2 | Не определена |
| Прогностические свойства шкал с учётом вида экссудата. Подтверждение преимуществ хирургической тактики. | ТМ+ПР | ROC-анализ, χ2 Пирсона, НП χ2, регрессионный анализ | Не определена | |
| ТМ | Определена | |||
| ПР | Определена |
После определения уровня летальности (зависимого параметра прогноза) при различных значениях балла шкалы оценки тяжести состояния пациентов в группах исследования проведено их сравнение. Наблюдаемый уровень летальности в группах исследования указывает на преимущества ПР-метода при [11-14] баллах шкалы ОТС (рис.12.17).
Результаты прогноза, полученные при гнойном РП, могут быть использованы при высоком уровне диагностического обеспечения.
При использовании другого статистического метода – Z-теста получены данные, указывающие на эффективность ПР-метода у пациентов, имеющих невысокую степень тяжести состояния по шкале ОТС. Преимущества ПР-метода, установленные после 5% цензурирования, наблюдались также при [11-14] баллах шкалы ОТС (рис.12.18). Избранные для исследования критерии полиорганной дисфункции не всегда являются определяющими в оценке состояния пациентов. Поиск наиболее информативной комбинации симптомов, обладающих наибольшим дискриминирующим потенциалом – одна из составляющих исследовательской работы. Для проведения тестирования программными средствами проведено тестирование комбинаций критериев по заданным промежуткам их значений. Основной набор значений включает показатели, отражающие норму, описанную в литературных источниках (таблица 12.10). Принадлежность к программированному интервалу параметра оценивается как «1»; остальные как «0». Определялись дискриминационные свойства суммы баллов, являющейся потенциальным предиктором.
Поиск наиболее информативной комбинации симптомов, обладающих наибольшим дискриминирующим и прогностическим потенциалом – основная исследовательская задача, обеспечивающая выработку алгоритма действий для решения сложных диагностических и тактических вопросов.
Этапы принятия решения (таблица 12.11):
Ø Прогнозирование исходов на дооперационном этапе.
Ø Прогнозирование исходов на интраоперационном этапе.
Ø Прогнозирование исходов в течение первых послеоперационных суток.
Ø Прогнозирование исходов в течение последующих послеоперационных суток.
В основе создания шкалы установлен принцип констатации балла - отклонение от интервалов критериев (таблица 12.10), которые в основном являются интервалами нормальных значений. В исследовательских целях изменение границ значений оправдано для поиска наилучших дискриминационных возможностей искомой шкалы, но в настоящем исследовании границы значений предикторов не менялись. Констатация отклонения от нормального интервала обозначалась одним баллом шкалы. Подбор критериев шкалы осуществлялся путём пошагового включения их в шкалу и тестирования на дискриминационную ценность путём ROC-анализа (таблица 12.12).
Таблица 12.12
Дискриминационные максимумы: примеры пошагового включения предикторов.
Зависимый параметр – исход лечения
| Все виды экссудата | [САД], [ЧДД], [GCS], [Оксигенация], [Гематокрит], [Калий], [Натрий], [Креатинин], [СОС], [ККв] | |
| ROCAUC=824 | SEAREA=0,014 | |
| [САД], [ЧДД], [GCS], [Оксигенация], [Гематокрит], [Калий], [Натрий] | ||
| ROCAUC=822 | SEAREA=0,013 | |
| [САД], [ЧДД], [GCS], [Оксигенация], [Гематокрит], [Калий], [Натрий], [Креатинин] | ||
| ROCAUC=834 | SEAREA=0,012 | |
| [САД], [ЧДД], [GCS], [Оксигенация], [Гематокрит], [Калий], [Натрий], [Креатинин], [СОС] | ||
| ROCAUC=0,877 | SEAREA=0,009 | |
На первом этапе определены индивидуальные прогностические свойства предикторов и прогностические возможности шкалы независимо от вида экссудата. Учитывая отсутствие достоверных характеристик экссудата, которые могут быть получены только во время лапаротомии, на этом этапе единственным инструментом прогнозирования была совокупность критериев, обеспечившая наивысшие дискриминационные свойства шкалы. После этого при помощи программы MedCalc проведён уточнённый ROC-анализ и регрессионный анализ, позволившие определить logit-формулу для вычисления прогноза при помощи балла тестируемой шкалы. В результате установлен перечень предикторов, значения которых в совокупности наиболее полно дискриминируют исход заболевания при последующей констатации гнойного РП (таблица 12.13).
Таблица 12.13
Дискриминационные свойства критериев. Зависимый параметр-исход лечения
| Все виды экссудата, дооперационное обследование | [САД], [ЧДД], [GCS], [Оксигенация], [Гематокрит], [Калий], [Натрий], [Креатинин], [СОС], [ККв] | |||
| Дискриминационный максимум (ДМ) | ДМ - Строгое соответствие (MedCalc) | |||
| ROCAUC | SEAREA | ROCAUC | SEAREA | |
| 0,907 | 0,007 | 0,934 | 0,026 | |
| Гнойный экссудат, дооперационное обследование | [САД], [ЧДД], [GCS], [Оксигенация], [Гематокрит], [Калий], [Натрий], [Креатинин], [СОС], [ККв] | |||
| Дискриминационный максимум (ДМ) | ДМ - Строгое соответствие (MedCalc) | |||
| ROCAUC | SEAREA | ROCAUC | SEAREA | |
| 0,884 | 0,011 | 0,891 | 0,035 | |
Для расчёта прогноза исходов на дооперационном этапе определены параметры регрессионного уравнения, полученного при помощи программы MedCalc: logit= -7,6783+1,7557х; где х - число баллов тестируемой шкалы. Установлено высокое качество прогностической модели, подтверждённое классификационными возможностями (89,5%) (таблицы 4, 5 прил.). Совокупность критериев, наиболее полно дискриминирующих исход при гнойном РП, оказалась аналогична предикторам для генеральной совокупности пациентов. Уравнение логистической регрессии в этом случае: logit= -5,8414+1,3161х; где х - число баллов шкалы. Качество исследуемой прогностической модели подтверждается высокими дискриминационными свойствами, статистической значимостью коэффициентов регрессионного уравнения, значением и статистической значимостью критерия χ2 (рис.12.19).
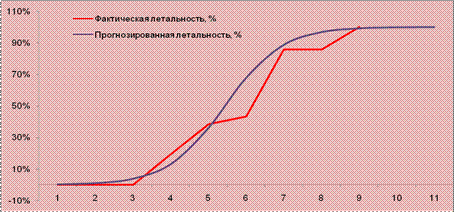
Рис.12.19. Прогнозируемая и наблюдаемая летальность при гнойном РП (%)
Прогнозированная летальность рассчитана с учётом применения обозначенной выше совокупности критериев, но определена по двум направлениям, устанавливающим формулы логистической регрессии отдельно для ТМ- (logit= -5,6699+1,3021х; где х - число баллов шкалы) и ПР-групп (logit= -6,2343+1,3636х; где х - число баллов шкалы) (таблица 12.14). Ретроспективное исследование параметров уравнений регрессии позволило сравнить прогнозированную летальность в группах с традиционным хирургическим лечением и программированными релапаротомиями. Установлено, что при 3-6 баллах исследуемой шкалы имеются прогностические преимущества метода программированных релапаротомий (рис.12.20), наиболее достоверно проявляющиеся при 4-5 баллах. В этих случаях степень тяжести состояния, описываемая совокупностью предикторов даёт основания для выбора альтернативного метода хирургического лечения – метода программированных релапаротомий.
Прогнозированная летальность при 4 и более баллах должна мотивировать лечащий медицинский персонал на использование максимальных возможностей интенсивной терапии, поскольку прогнозируемая в этих случаях больше средней наблюдаемой летальности в обеих группах исследования.
Таблица 12.14. Прогнозированная летальность при гнойном РП (%)
| Балл шкалы | |||||||||||
| ТМ | 0,34 | 1,25 | 4,45 | 14,6 | 38,6 | 69,9 | 89,5 | 96,9 | 99,1 | 99,8 | 99,9 |
| ПР | 0,19 | 0,76 | 2,91 | 10,5 | 31,4 | 64,2 | 87,5 | 96,5 | 99,1 | 99,7 | 99,9 |
| ТМ+ПР | 0,29 | 1,07 | 3,88 | 13,1 | 35,9 | 67,8 | 88,6 | 96,7 | 99,1 | 99,7 | 99,9 |
Результаты, полученные при использовании метода Z-теста, подтверждают преимущество ПР-метода в интервале балла исследуемой шкалы [3-7] с максимумами этого преимущества при [4-5] баллах шкалы.
Таблица 12.15. Дискриминационные свойства критериев:
зависимый параметр – исход лечения в ТМ+ПР-группе
| Гнойный экссудат, первые послеоперационные сутки | [САД], [ДАД], [ЧСС], [GCS], [Оксигенация], [Гематокрит], [Калий], [Натрий] | |||
| Дискриминационный максимум (ДМ) | ДМ - Строгое соответствие (MedCalc) | |||
| ROCAUC | SEAREA | ROCAUC | SEAREA | |
| 0,869 | 0,016 | 0,750 | 0,044 | |
На основе полученных данных появляется возможность дифференцированного подхода к хирургической тактике на интраоперационном этапе. Классификационные возможности шкалы при традиционном хирургическом лечении и программированных релапаротомиях примерно одинаковы и составляют 83-84%. Наряду с дискриминационными свойствами эти параметры характеризуют прогностическую модель как очень хорошую. При этом уточняющий поиск наиболее информативных для прогноза совокупностей критериев может проходить изолированно в группах исследования. Прогноз исходов лечения распространённого гнойного перитонита может быть определён в контексте применения избранной хирургической тактики. Наиболее интересным представляется изучение параметров прогностической модели при лечении методом программированных релапаротомий. Определение индивидуального прогноза проводится после окончательного определения хирургической тактики, однако подбор прогностической модели осуществляется ретроспективно на основе диагностических параметров, характерных для ПР-группы, отобранной без применения алгоритма выбора хирургической тактики.
Установлено, что прогностическая модель при ПР может быть уточнена после выбора наиболее информативной совокупности предикторов, отличной от совокупности, применимой для всех пациентов с гнойным РП (рис.12.15, 12.16). Характеристики прогностической модели обладают статистической значимостью и могут быть применимы для индивидуального прогноза после окончательного выбора хирургической тактики.
Рис.12.20. Дооперационное обследование
Разница прогнозированной летальности в ТМ и ПР-группой
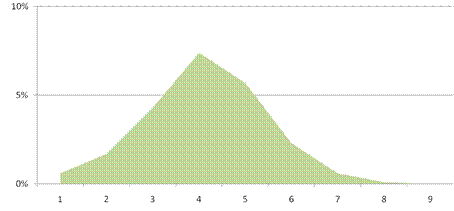
Для подтверждения итогов исследования была использована demo-версия программы MedCalc, в ходе работы с которой проверены основные прогностические характеристики шкалы дооперационного исследования (таблица 12.16).
Рис.12.21. Первые хирургические сутки
Разница прогнозированной летальности в ТМ и ПР-группой

Вычисления показывают, что на интраоперационном этапе (ROCAUC 0,922; SEAREA 0,049) классификационные возможности шкалы оцениваются в 86%. Уравнение логистической регрессии представлено в следующем виде: logit= -10,2251+2,3209х, где x – число баллов шкалы. Расчёт вероятности проводился по формуле: p = ℮logit/(1+℮logit); где p –вероятность наступления летальности; logit – значение уравнения логистической регрессии при имеющемся числе баллов. Полученные результаты отражают прогностические возможности изучаемых параметров и собственной шкалы оценки тяжести состояния (рис.12.21). Представленные данные свидетельствуют о высоких прогностических свойствах шкалы, применимой для ПР-группы на интраоперационном этапе прогнозирования (рис.12.22). В случаях, когда хирургическая тактика не определена интраоперационно остаётся время для принятия окончательного решения – это первые 24-48 часов после первой операции. Для этого изучены прогностические возможности на третьем этапе прогнозирования (таблицы 4,5 прил.).
Таблица 12.16
Дискриминационные свойства критериев в отношении исходов РП в ПР-группе
| [СрАД], [ДАД], [ЧДД], [GCS], [Ректальная температура], [Гематокрит], [Креатинин], [ККв] | |||
| Дискриминационный максимум (ДМ) | ДМ - Строгое соответствие (MedCalc) | ||
| ROCAUC | SEAREA | ROCAUC | SEAREA |
| 0,922 | 0,013 | 0,922 | 0,049 |
В течение первых хирургических суток возможности прогноза исхода гнойного РП оказались несколько меньше. Наиболее полно дискриминирует прогноз исходов совокупность из восьми предикторов (таблица 12.15). Прогнозирование при использовании полученной модели основано на регрессионном уравнении: logit= -3,5409+0,6934х, где x – число баллов шкалы. При помощи данной модели около 76% случаев описаны правильно.
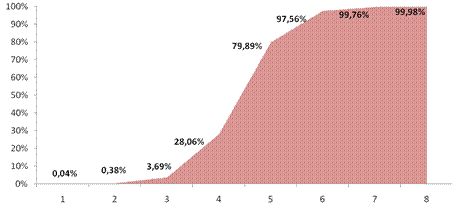
Рис.12.22. Соотношение баллов исследуемой шкалы и прогнозированной
летальности, определённой на интраоперационном этапе обследования в группе
с программированными релапаротомиями.
При сравнении прогнозированной летальности в первые хирургические сутки и на интраоперационном этапе прогнозирования установлено, что у 54% пациентов прогноз ухудшался (таблица 12.17).
Существенные препятствия для эффективного прогнозирования на основании обследования, предпринятого в течение первых послеоперационных суток, возникают в связи с уменьшением классификационных и дискриминационных свойств шкалы. Ограниченное применение полученной прогностической модели обусловливает её применение, как дополнительный инструмент для прогноза исходов и дифференцировки хирургической тактики.
Для оценки возможностей эффективного прогноза прогрессирования РП на основании дооперационного обследования были использованы аналогичные статистические методы. Однако, учитывая незначительные дискриминационные свойства прогностических моделей, недостаточный объём обследования не дают основания для выработки приемлемого алгоритма определения вероятности клинически значимого прогрессирования РП. Учёт дискриминационных возможностей одиночных предикторов указывает на наиболее информативные маркеры, выявленные в различные сроки послеоперационного периода (таблица 12.18). Обоснованное применение методов прогноза прогрессирования РП, вытекающих из результатов регрессионного и ROC-анализа на данном этапе исследования следует считать преждевременным. Рекомендуется учёт наиболее информативных предикторов. Дифференцировка хирургической тактики ориентирована в основном не на прогноз клинических событий, опосредующих исходы, а на окончательный прогноз результатов лечения [Костюченко К.В., 2009].
Таблица 12.17
Динамика прогноза исходов лечения при гнойном РП
| Группы исследования / Динамика | Вся группа | ТМ | ПР |
| Улучшение в течение первых хирургических суток (%) | |||
| Ухудшение в течение первых хирургических суток (%) |
Важнейшим результатом исследования явилось создание концепции прогнозирования исходов (прогрессирования) РП и дифференцировки хирургической тактики в зависимости от наиболее информативных предикторов или их совокупностей. Имеющиеся ограничения, отчасти недостаточный объём обследования в ряде случаев определяют недостаток статистической значимости полученных результатов, что требует разграничения методов в зависимости от их применимости для избранных групп исследования.
Концепция настоящего исследования применима для решения широкого спектра вопросов, связанных с прогнозированием. Особенностью аналитического метода является определение балла шкалы на основе отклонения имеющегося показателя от известных границ (нормальных показателей). Наиболее обосновано дооперационное применение метода.
Определение основных групп критериев, с помощью которых можно дифференцированно подходить к прогнозу исходов РГП, является важнейшим результатом исследования. Различия в прогнозированной летальности могут быть основой для определения прогноза в различных группах заболевания и индивидуального прогноза. Часть критериев, наиболее связанных с прогрессированием РГП, могут быть использованы на соответствующих этапах прогнозирования, как наиболее существенные критерии неблагополучия, могут лежать в основе структуры полиорганной дисфункции, характерной именно для РГП.
Таблица 12.18
Динамика дискриминационных свойств основных одиночных предикторов.
Зависимый параметр: прогрессирование гнойного РП
с релапаротомией «по требованию»
| Предиктор / Послеоперационный период | 0* | ||||
| САД | + | + | + | + | + |
| ДАД | + | + | + | + | |
| Ректальная температура, С | + | + | + | + | |
| ЧДД | + | + | + | + | + |
| Лейкоциты крови | |||||
| ЧСС | + | + | + | ||
| СрАД | + | + | + | + | + |
| Балл шкалы комы Glasgow | + | + | + | + | + |
| Оксигенация, SpO2 | + | + | + | + | |
| Гематокрит | + | + | + | ||
| Калий плазмы крови | + | + | + | + | |
| Натрий плазмы крови | |||||
| Креатинин плазмы крови | |||||
| Возраст |
| ||||
| Время развития заболевания | + | ||||
| Число симптомов SIRS | + | + | + | + | + |
| Число симптомов SPOD | + | + | + | + | |
| Балл шкалы ОТС | + | ||||
| *Изучены в группе ПР+ТМ: хирургическая тактика не определена Отмечены предикторы, при которых отвергается нулевая гипотеза об отсутствии связи значения предиктора и зависимого параметра – прогрессирования РП, pχ2<0,05 | |||||
На основе результатов исследования разработан и внедрён программный продукт MS Excel 2007 (рис.1,2 прил.), обеспечивающий получение данных о вероятности летального исхода при до- и интраоперационном обследовании. В программе заложены возможности констатации SIRS, полиорганной дисфункции, а также расчёта баллов APACHE II, IPM, LODS. Важнейшим элементом программы является получение рекомендаций для оптимизации хирургической тактики на основе интраоперационной диагностики.
Изучение перитонита и осложняющего его сепсиса – это наиболее популярная и важная тема исследований среди хирургов. Однако, препятствия, имеющие место на пути к снижению летальности могут исчезнуть, если исследователи будут продвигаться в двух направлениях: воздействие на патогенетические механизмы перитонита и внедрение новых методов, позволяющих размыкать порочные круги патологии при этом грозном осложнении. Всё это требует доказательного обеспечения.
Несомненно, идеология полиорганной дисфункции и синдрома системной воспалительной реакции является важным этапом для понимания патогенеза перитонита, но возможности изучения в этой сфере не исчерпаны. К примеру, только в последние годы появляются публикации, касающиеся глубоких иммунологических исследований, ещё меньше публикаций касающихся поиска новых факторов, влияющих на клеточные и другие реакции при сепсисе, выявлению неизвестных ранее продуктов метаболизма и регуляции, имеющих важное диагностическое и прогностическое значение.
 2021-12-25
2021-12-25 96
96








