Потенциометрия
Метод возник в 1893 г., когда немецкий химик Р. Беренд впервые провёл потенциометрическое титрование.
Потенциометрический метод анализа основан на зависимости равновесного электродного потенциала (Е) от активности (a) или концентрации (С) вещества в растворе.
Для измерений необходимо составить гальванический элемент из подходящего индикаторного электрода и электрода сравнения, а также иметь прибор для измерения потенциала индикаторного электрода. В качестве таких приборов используют:
§ потенциометр (для особо точных измерений);
§ электронные вольтметры, рН-метры, иономеры – современные потенциометры заводского типа с электронными усилителями тока. Выпускаются серийно. Шкалы калиброваны: мВ, ед. рН, ед. рХ.
По способу выполнения анализа различают прямую потенциометрию и потенциометрическое титрование.
1. Прямая потенциометрия. Измеряют ЭДС гальванического элемента и по зависимости Е = f (a) находят активность иона графическим или расчётным способом. При этом используют:
§ метод градуировочного графика;
§ метод добавок;
§ метод концентрационного элемента.
Точность метода составляет 2–10 %. В аналитической химии его применяют для определения рН, содержания катионов и анионов с использованием ионоселективных электродов (ионометрия).
2. Потенциометрическое титрование. Измеряют ЭДС в процессе титрования, затем строят кривую титрования. По ней определяют объём титранта в точке эквивалентности (т. э.) и рассчитывают результат анализа по закону эквивалентов.
Точность метода составляет 0,1–0,5%. Используют реакции всех типов: кислотно-основные реакции, ОВР, реакции осаждения и комплексообразования. Метод удобен для титрования окрашенных и разбавленных растворов, а также смесей веществ.
Для нахождения т. э. используют 4 графических способа (рис. 17):
§ по интегральной кривой титрования (а) – наиболее простой способ. Проводят 3 касательные (к двум пологим участкам кривой и к скачку), затем полученный между двумя точками пересечения отрезок делят пополам и опускают перпендикуляр на ось абсцисс.
§ по дифференциальной кривой титрования (б) – более точный способ.
§ по второй производной (в) – используется для более точного определения т. э. в случае ассиметричного или малого скачка. Соединяют концы ветвей графика. На пересечении этой прямой с осью абсцисс находят т. э.
§ по кривой в координатах ΔV/ΔE – V(R) (метод Грана) (г) – используется для разбавленных растворов.
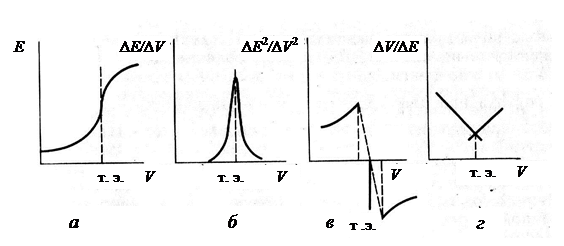
Рис. 17. Графические способы определения т. э.
 2014-02-13
2014-02-13 3145
3145
