Таблица 44 - Дифференцирующие признаки некоторых
Микобактерий по культурально-биохимическим свойствам
Таблица 43 - Дифференциация основных патогенных видов
| Признаки | М. tuberculosis | M. bovis | M. avium |
| Скорость роста | 3-8 недель | 3-8 недель | 2-6 недель |
| Тип роста колоний на глицеринсодержащих средах | Эугонический, колонии R-типа | Дисгонический, колонии R-типа | Эугонический, колонии R-типа |
| Образование пигмента | - | - | - |
| Верхний температурный предел роста | 42° С | 42° С | 44° С |
| Потребность в глицерине | + | _ | + |
| Зависимость роста от натрия пирувата (0,4%) | - | + | - |
| Ниацин тест | + | - | - |
| ТСН-ингибиция (10 мкг/куб.см) | - | + | - |
| Ингибиция толуидиновым голубым | + | + | - |
| Редукция нитратов | + | - | - |
| Уреаза | + | + | - |
| Пиразинамидаза | + | - | + |
Тест на уреазу. Смешивают 1 часть агара с мочевиной и 9 частей стерильной воды, 4 кубических см наливают в пробирку. Затем в субстрат вносят петлю молодой культуры микобактерий. Инкубируют при 37° С до 3 суток. Положительный результат — окрашивание от розового до красного.
Тесты ингибиции. Проводят в отношении пиромицин гидразида (PMN), гидразида тиофен-2-карбоновой кислоты (TCN). Указанные соединения вносят в среду Левенштейна-Йенсена до финальной концентрации 10 мг/мл. Толуидиновый голубой добавляют в среду Петраньяни до концентрации 0,023%.
Тест на деаминирование пиразинамида. Базовая среда бульон «Dubos», содержащая 0,1 г пиразинамида, 2,0 г пировиноградной кислоты и 15 г агара на 1000 мл. Среду разливают по 15 мл в пробирки, автоклавируют при 121° С в течение 15 минут, охлаждают в вертикальном положении. Агар инокулируют молодой культурой микробактерий иинкубируют при 37° С в течение 4 дней. Затем добавляют 1 мл свежеприготовленного 1%-ного водного раствора сульфата аммония железа и помещают пробирки в холодильник на 4 часа. Положительная реакция — розовая полоска в агаре.
В случае необходимости видовой дифференциации в целом в пределах группы медленнорастущих микробактерий прибегают к более подробному изучению их культуральных и биохимических свойств (табл. 38).
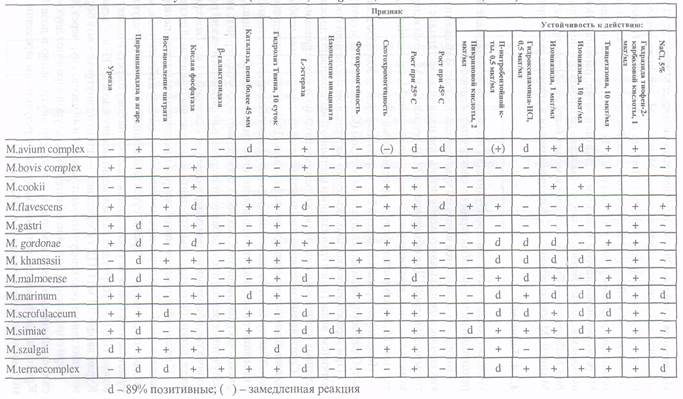
Примечание к таблице 44: «М. bovis complex» включает M. bovis, BCG и М.africanum. «М.теггае complex» включает М. terrae, M. nonchromogenicum и М. triviale. «M.avium complex» включает M.avium и M.intracellure. Новый подвид, не описанный в «Bergey's Manul of Sistematic Bacteriology», M.avium subsp. silvaticum предложен в 1990 г. (Thorel et al.). Те же авторы предложили считать М. paratuberculosis другим подвидом — M.avium subsp. paratuberculosis, но имеющихся данных недостаточно, чтобы легко различать эти подвиды. Вид M.flavescens — быстрорастущий и может быть ошибочно принят за M.szulgai. M.szulgai может быть фотохромогенным в условиях роста при 25° С.
Биопроба. Используют для выявления возбудителя в исследуемом материале и дифференциации видов микобактерий по спектру патогенности. Биопроба отличается высокой чувствительностью. Заражением морских свинок можно выявить возбудитель при наличии в материале 5-6 клеток микобактерий. Для обнаружения М. tuberculosis и М. bovis используют морских свинок, кролики устойчивы к заражению М. tuberculosis. Для выявления М. avium в опыт берут кур не моложе 150 дней.
Используют кроликов массой 2 кг, морских свинок — 300-350 г. Биопробу на туберкулез производят следующим образом. При заражении животных тканевым материалом последний после обработки и нейтрализации измельчают, выдерживают до осаждения крупных частиц, надосадочную жидкость используют для заражения.
Соотношение материала и жидкости берется с таким расчетом, чтобы на 1 мл конечной взвеси приходилось около 1 г ткани. Для заражения исследуемой культурой бактериальную массу снимают с поверхности плотной питательной среды и помещают в предварительно взвешенную емкость (бюкс, пенициллиновый флакончик), на аналитических весах определяют массу бактерий и, исходя из полученных результатов, добавляют стерильный физиологический раствор в количестве, обеспечивающем содержание 1 мг бактерий в 1 мл. Бактериальная масса должна быть тщательно растерта до получения гомогенной суспензии.
С целью обнаружения микобактерий в исследуемом материале последний вводят в дозе 1-2 мл двум морским свинкам подкожно в область паха, курам — в подкрыльцовую вену. Через 30 суток зараженных животных исследуют туберкулиновой пробой. У морских свинок удаляют на боку шерсть и вводят внутрикожно ППД — туберкулин для млекопитающих в дозе
25 ТЕ в объеме 0,1 мл. Курам вводят 0,1 мл ППД туберкулина — для птиц внутрикожно в бородку. У морских свинок реакцию учитывают через 24 и 48 часов, у кур через 30-36 ч.
При определении вида микобактерий культурой заражают двух морских свинок подкожно, двух кроликов и двух кур внутривенно в дозе
1 мг/мл. Критерии дифференциации микобактерий по результатам заражения различных животных представлены в таблице 45.
 2014-02-17
2014-02-17 810
810








