V комплекс
II комплекс
IV комплекс
III комплекс
III комплекс –комплекс цитохромов b-c 1, кроме цитохромов в нем имеются 2 железо-серных белка. Всего насчитывается 8 полипептидных цепей.
Функция:
1. Принимает электроны от коэнзима Q и передает их на цитохром с.
2. Переносит протоны Н+ на наружную поверхность внутренней митохондриальной мембраны.
IV комплекс – цитохромы аа3 или цитохромоксидаза, всего содержит 8 полипептидных цепей. В комплексе также имеется 2 иона меди.
Функция:
1. Принимает электроны от цитохрома с и передает их на кислород с образованием воды.
2. Переносит протоны Н+ на наружную поверхность внутренней митохондриальной мембраны.
II комплекс – как таковой не существует, его выделение условно, включает в себя ФАД-зависимые ферменты – ацил-S-КоА-дегидрогеназа, сукцинатдегидрогеназа, митохондриальная глицерол-3-фосфат-дегидрогеназа.
Функция:
1. Восстановление ФАД в окислительно-восстановительных реакциях,
2. Обеспечение передачи электронов от ФАДН2 на железосерные белки внутренней мембраны митохондрий. Далее эти электроны попадают на коэнзим Q.
Некоторые авторы выделяют V комплекс ферментов:
V комплекс – это фермент АТФ-синтаза, состоящий из??? белковых цепей, подразделенных на две большие группы: Одна группа формирует субъединицу Fо (произносится со звуком "о", а не "ноль" т.к о лигомицин-чувствительная) – ее функция каналообразующая, по ней выкачанные наружу протоны водорода устремляются в матрикс. Другая группа образует субъединицу F1 – ее функция каталитическая, именно она, используя энергию протонов, синтезирует АТФ.
Для синтеза 1 молекулы АТФ необходим проход 3-х протонов Н+.
На основании вышеизложенного построена схема окислительного фосфорилирования:
1. Ферменты дыхательной цепи расположены в строго определенной последовательности: каждый последующий белок обладает большим сродством к электронам, чем предыдущий (он более электроположителен, т.е. обладает более положительным окислительно-восстановительным потенциалом). Это обеспечивает однонаправленное движение электронов.
Дополнение
Способность окислительно-восстановительной пары обратимо отдавать электрон выражают окислительно-восстановительным потенциалом Е0'. В биохимии принято пользоваться понятием восстановительный потенциал. Чем более отрицательной величиной выражается восстановительный потенциал системы, тем выше ее способностьотдавать электроны. При сравнении восстановительного потенциала пары НАДН / НАД = -0,32 В и пары Н2О / 1/2О2 = +0,82 В видно, что электроны будут переходить к воде. В действительности между названными донором и акцептором электронов имеется много промежуточных соединений.
2. Все атомы водорода, отщепленные дегидрогеназами от субстратов в аэробных условиях достигают внутренней мембраны митохондрий в составе НАДН или ФАДН2.
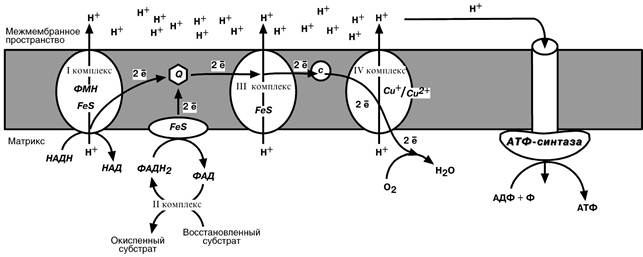 |
3. Здесь они передают свои электроны в дыхательную ферментативную цепь, по которой электроны движутся к своему конечному акцептору – кислороду. В результате образуется вода.
Дополнение
Можно провести аналогию со смесью водорода и кислорода, которая получила название "гремучая смесь". При малейшей искре эта смесь взрывается с образованием воды и выделением тепла. В организме такая реакция происходит постоянно, но при этом она идет порционно, "ступеньками", что позволяет использовать часть выделяемой энергии для выкачивания протонов водорода в межмембранное пространство.
4. Поступающие в дыхательную цепь электроны богаты свободной энергией. По мере продвижения их по цепи они теряют энергию. Эта энергия используется I, III, IV комплексами дыхательных ферментов для перемещения протонов водорода в межмембранное пространство.
Дополнение
Как известно из физики, энергией называется способность тела совершать работу. При перемещении электрического заряда энергия электронов убывает и частично превращается в теплоту.
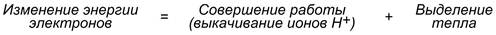
Другая часть энергии затрачивается на выкачивание водорода из матрикса в межмембранное пространство и создание градиента.
5. Выкачивание протонов водорода происходит не случайно, а в строго определенных участках мембраны. Эти участки называются участки сопряжения (или, не совсем точно, пункты фосфорилирования). На этих участках расположены I, III, IV комплексы дыхательных ферментов. В результате работы этих комплексов формируется градиент протонов водорода между внутренней и наружной поверхностями внутренней митохондриальной мембраны. Такой градиент обладает потенциальной энергией.
Градиент получил название электрохимический или протонный градиент ( Dm,"дельта мю"). Он имеет две составляющие – электрическую (DY, "дельта пси") и концентрационную (DрН):
Dm = DY + DрН
Дополнение
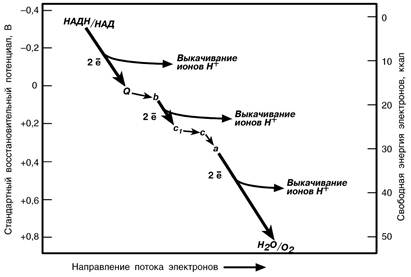
На схеме показаны стандартные восстановительные потенциалы пары НАДН/НАД и Н2О/О2 и уменьшение свободной энергии электронов при движении через всю дыхательную цепь от НАДН к кислороду. Полное изменение стандартной свободной энергии в этом процессе вычисляют по формуле
DGo'= – nFDE'o,
где DGo– изменение стандартной свободной энергии в калориях, n ‑ число перенесенных электронов, F – число Фарадея (23062 кал/(В × моль)), DE'o– разность стандартных потенциалов электронодонорной и электроноакцепторной системы
DGo'= –2 × 23062 × (0,82 – (–0,32)) = –52,6 ккал
Таким образом, исходя из стандартной энергии гидролиза АТФ равной 7,3 ккал, клетка получает количество энергии достаточное для синтеза 7 молекул АТФ (52,6: 7,3 = 7,21). По графику видно, что в трех участках изменение энергии электронов наиболее значительно. Эти участки называются участками сопряжения или фосфорилирования, т.к. за счет этой энергии происходит перенос ионов Н+ через мембрану и в дальнейшем фосфорилирование АДФ до АТФ.
6. Протоны теряют свою энергию, проходя через АТФ-синтазу. Часть этой энергии тратится на синтез АТФ.
Дополнение
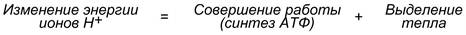
Так же как в случае с электронами, энергия ионов водорода (протонного градиента) не расходуется попусту. Двигаясь по электрохимическому градиенту, ионы водорода выделяют энергию, часть которой используется на синтез АТФ.
 2014-02-09
2014-02-09 2830
2830
