РЕАЛЬНЫЕ ГАЗЫ
ЛЕКЦИЯ 17
Законы идеальных газов не предсказывают, например, такое явление как конденсация. Причина заключается в том, что молекулы взаимодействуют друг с другом.
Малая сжимаемость газов при высоких давлениях, а также способность жидких и твердых тел сопротивляться сжатию, указывают на то, что между молекулами действуют также и силы взаимного отталкивания. Силы притяжения и отталкивания действуют одновременно.
На малых расстояниях преобладают силы отталкивания F1r, на дальних - силы взаимного притяжения F2r..
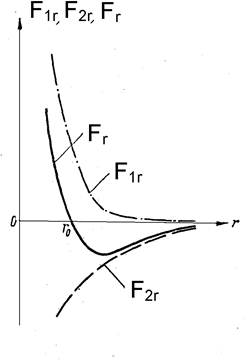
Рис.16.4
При r=r0 силы F1r и F2r взаимно уравновешиваются и результирующая сила Fr = 0. Если r >r0, то преобладают силы взаимного притяжения, если r < r0, - преобладают силы отталкивания.
Таким образом, r0 – это такое равновесное расстояние между молекулами, на котором они находились бы при отсутствии теплового движения.
В состоянии устойчивого равновесия система, состоящая из двух взаимодействующих частиц, обладает минимальной потенциальной энергией. Дальнейшее уменьшение r приводит к увеличению W n и превращению ее из отрицательной в положительную.
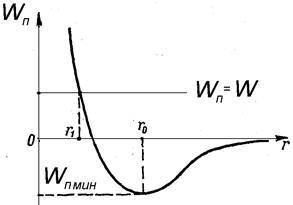
Рис.16.5
 2014-02-18
2014-02-18 859
859







