Химические реакции
Химическая связь(ковалентная и ионная)
Химическая связь - это то, чем соединяются атомы между собой в различные молекулы, ионы, кристаллы.
Между ионами положительными и отрицательными (катионными и анионами, которые представлены в таблице растворимости) образуется ионная связь.
Например, NaCL = Na+ + CL-
Ковалентная связь – это связь с образованием общих электронных пар.
Н2 Н-Н Н(:) Н, Н-CL
ковалентная неполярная ковалентная полярная
одинаковые неметаллы разные неметаллы
Химические реакции - это превращение одних веществ в другие.
Экзотермические реакции происходят с выделение теплоты, а эндотермические с поглощением теплоты и требуют постоянного нагревания в течении всей реакции.
Пусть в данной реакции выделилось 150 кДж теплоты. Сколько грамм магния сгорело?
2Mg+O2=2MgO+Q 600 (кДж)
m (Mg)= ν* Mr
Mr (Mg) = 24 г/моль
х моль - 150 кДж
2 моль - 600 кДж
х=(2*150)/600=0,5 моль
m (Mg)= 0,5*24= 12 г
Ответ:12 г.
Скорость химической реакции – это изменение концентрации в единицу времени.

Единица измеренная скорости: Моль/л •с
С - это молярная концентрация: количество растворенного вещества в объеме растворителя. С= ν/V, где ν - количество вещества(моль), V-объем (л)
Закон действующих масс: скорость химической реакции прямопропорцональна произведению концентраций реагирующих веществ, взятых степенях равных их коэффициентам в химическом уравнении.
N2 + 3H2= 2NH3
υ= k[N2]*[H2]3
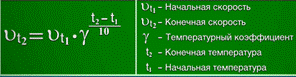
Правило Вант-Гоффа: при повышении температуры на каждые 10 градусов скорость химической реакции возрастает в 2-4 раза.
 2014-02-24
2014-02-24 877
877








