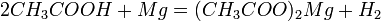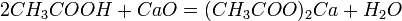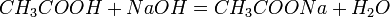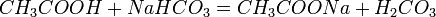Спирты
Природные источники УВ - См печатные листы
Применение углеводородов
1. Высокая теплота сгорания углеводородов обусловливает использование их в качестве топлива. 2. Метан в составе природного газа находит все более широкое применение в быту и на производстве. Получило распространение применение пропана и бутана в виде "сжиженного газа", особенно в тех местностях, где нет подводки природного газа. Жидкие углеводороды используются как горючее для двигателей внутреннего сгорания в автомашинах, самолетах и т. д.
Как весьма доступный углеводород, метан все в большей степени используется в качестве химического сырья.
3. Метан — основной источник получения водорода в промышленности для синтеза аммиака и ряда органических соединений.
CH4 + H2O = 3H2 + CO
4. Для некоторых синтезов
5. Хлорметан CH3Cl — газ. Как вещество, легко переходящее в жидкое состояние и поглощающее большое количество теплоты при последующем испарении, он применяется в качестве хладагента в холодильных установках.
6. Дихлорметан CH2Cl2, трихлорметан (хлороформ) CHCl3 и тетрахлорметан CCl4 — жидкости; они используются как растворители. Тетрахлорметан применяется, кроме того, при тушении огня (особенно в тех случаях, когда нельзя использовать воду), так как тяжелые негорючие пары этого вещества, образующиеся при испарении жидкости, быстро изолируют горящий предмет от кислорода воздуха.
Спирты́ (устар. алкого́ли, от лат. spiritus — дух) — органические соединения, содержащие одну или более гидроксильных групп (гидроксил, −OH).
| Одноатомные | Многоатомные | Ароматические спирты (Фенолы) | |
| C2H5OH - этанол | 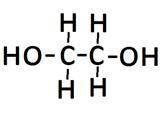 этиленгликоль
С2Н2(ОН)2 этиленгликоль
С2Н2(ОН)2
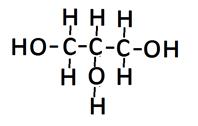 глицерин
С3Н5(ОН)3 глицерин
С3Н5(ОН)3
| 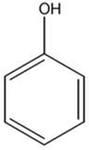 С6Н6 - фенол С6Н6 - фенол
| |
| Физические свойства | |||
| Прозрачные жидкости, с приятным запахом, в неограниченных количествах растворяются в воде, некоторые яды | твердые кристаллические вещества, без цвета, токсичны, плохо растворимы в воде | ||
| Применение: | |||
| 1. в медицине 2.в пищевой промышленности 3. для синтеза новых веществ (например полимеров) 4. горючее 5. в быту | 1. в медицине 2. горючее 3.косметичекая промышленность 4. взрывчатые вещества 5. в быту | 1. в пищевой промышленности 2. для получение взрывчатых веществ 3. пол. фенолформальдегидных смол 4. медицине 5. синтетические волокна 6.моющие средства | |
| Химические свойства | |||
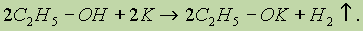

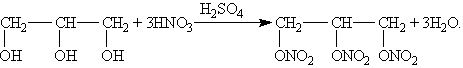
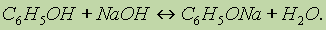
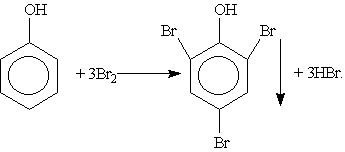
| |||
- это класс органических соединений, молекулы которых содержат одну или несколько функциональных карбоксильных групп -COOH.
Физические свойства:
Низшие карбоновые кислоты — жидкости с острым запахом, хорошо растворимые в воде. С повышением относительной молекулярной массы растворимость кислот в воде и их плотность уменьшаются, а температура кипения повышается. Высшие кислоты, начиная с пеларгоновой (н-нонановой) СН3-(СН2)7-СООН, — твердые вещества, без запаха, нерастворимые в воде. Низшие карбоновые кислоты в безводном виде и в виде концентрированных растворов раздражают кожу и вызывают ожоги, особенно муравьиная кислота и уксусная кислота.
Химические свойства:
1) Карбоновые кислоты при реакции с металлами, их оксидами или их осно́вными гидроксидами дают соли соответствующих металлов:
Также карбоновые кислоты могут вытеснять более слабую кислоту из её соли, например:
2) Карбоновые кислоты в присутствии кислого катализатора реагируют со спиртами, образуя сложные эфиры (реакция этерификации):
 2014-02-24
2014-02-24 888
888