Основные свойства дисперсных систем
определяются нескомпенсированной поверхностной энергией
Механизм возникновения поверхностной энергии рассмотрим на примере системы жидкость – газ (рис. 2). Для молекул, находящихся в объеме жидкой фазы, силы межмолекулярного взаимодействия симметричны, равнодействующая их равна 0.
Для молекул, расположенных на межфазной поверхности, симметрия сил нарушается: притяжение со стороны молекул газа слабее, чем со стороны молекул жидкости. В результате возникает результирующая сила, направленная внутрь более плотной (жидкой) фазы. Эту силу часто называют внутренним давлением. Чем сильнее различаются межмолекулярные взаимодействия в граничащих фазах, тем больше внутреннее давление. Так, для воды оно составляет 1,5×109 Па (14 800 атм.). Поэтому плотность капельных жидкостей практически не изменяется при увеличении внешнего давления. Такие жидкости называют несжимаемыми.

Нереализованная способность поверхностных молекул к взаимодействию обуславливает появление свободной поверхностной энергии G пов .
|
|
|
Общая поверхностная энергия системы определяется площадью поверхности S и удельной поверхностной энергией s, называемой поверхностным натяжением:
G пов = sS.
С точки зрения термодинамики, поверхностное натяжение – это работа обратимого процесса образования единицы площади новой поверхности при постоянных температуре Т, давлении р и составе жидкости.
Для образования новой межфазной поверхности необходимо перевести часть молекул из объема жидкости в поверхностный слой, затратив при этом работу против внутреннего давления, стремящегося втянуть молекулы поверхностного слоя внутрь фазы, т. е.
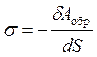 ,
,
где dА обр – термодинамически обратимая работа; она отрицательна, так как совершается над системой.
При р, Т = const
-dA обр = dG,
где G – свободная энергия Гиббса,
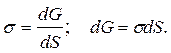
В результате действия s текучие системы принимают форму с минимальной поверхностью фазы при заданном объеме – форму сферы. Поэтому такие жидкости называют капельными.
Поверхностное натяжение на границе двух конденсированных фаз называет межфазовым. Оно образуется на поверхности раздела двух взаимно нерастворимых жидкостей, твердого тела с жидкостью и двух твердых тел и обозначается соответственно sж-ж, sт-ж, sт-т.
Поверхностное натяжение с ростом температуры снижается. Это связано с ростом давления насыщенного пара и уменьшением нескомпенсированности межмолекулярного взаимодействия. Поэтому при оценке значений s необходимо указывать температуру.
При 293 К s воды составляет 72,75 мДж/м2, подсолнечного масла – 33, сырого молока – 45-60, а сухих вин – 46-52 мДж/м2, что ниже s воды.
 2014-02-24
2014-02-24 876
876








