Элементы IА и IIА подгрупп, у которых заполняется внешний ns-уровень, относятся к s-элементам: ns1 – Li, Na, K, Rb, Cs, Fr называют щелочными, а ns2 – Be, Mg, Ca, Sr, Ba, Ra – щелочноземельными.
Основные характеристики:
1) Степени окисления элементов ns1 и ns2 всегда равны номеру группы (+1 и +2).
2) В основном состоянии атомы ns2-элементов не имеют неспаренных электронов, поэтому образованию ковалентной связи в соединениях этих элементов предшествует возбуждение ns2 → ns1np1 с последующей гибридизацией sp-типа, определяющей линейное строение трехатомных молекул ЭX2.
3) Для ns1-элементов характерно образование двухатомных молекул Э2(σсв)2(σ*)0; для ns2-элементов образование Э2 невозможно из-за равной заселенности связывающих и разрыхляющих σ-орбиталей.
4) Величины E°s-элементов предопределяют их восстановительные свойства, увеличиваясь при движении в подгруппе сверху вниз. Все s-элементы вытесняют водород из воды и кислот, восстанавливают оксиды металлов и неметаллов до простых веществ.
5) Ионность связи Э–Х возрастает в подгруппе сверху вниз, а в случае оснований удлинение связи Э–OH ведет к увеличению основности.
6) В соединениях LiX и BeX2 связь Э–Х преимущественно ковалентная (малополярная).
s-Металлы хранят в инертной атмосфере или под слоем жидких углеводородов, а получают обычно электролизом расплавов. Соли s-элементов окрашивают пламя в цвета: лития – в алый, натрия – в желтый, калия – в сине-фиолетовый, рубидия – в темно-красный, цезия – в бледно-голубой, кальция – в оранжево-красный, стронция – в темно-красный, бария – в светло-зеленый.
Большинство солей растворимо в воде. К нерастворимым относят LiCO3, KClO4, ЭCO3, ЭSO4, Э3(PO4)2 (Э = Ca, Sr, Ba), некоторые ЭF2.
При сжигании в атмосфере кислорода щелочных металлов образуются пероксиды M2O2. Только литий при обычных условиях сгорает в кислороде до Li2O. Начиная с калия, наряду с M2O2, образуются надпероксиды (KO2, RbO2, CsO2) и озониды (KO3, CsO3).
Щелочноземельные элементы при взаимодействии с кислородом при аналогичных условиях дают оксиды, пероксиды получаются труднее, чем для щелочных элементов. Так, пероксид бария BaO2 получают нагреванием на воздухе оксида бария при 700 ºC. Пероксиды остальных металлов этой группы получают «мокрым» способом при действии пероксида водорода на гидроксиды:
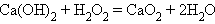
Оксиды s-элементов имеют основной характер, что подтверждается характером их взаимодействия с кислотными оксидами:
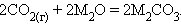
Исключение, как и следует ожидать, составляет BeO – он амфотерен:
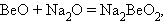 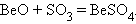
|
Пероксиды проявляют окислительно-восстановительную двойственность за счет пероксид-иона 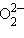 :
:
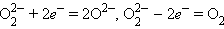
Окислительные свойства пероксидов выражены сильнее, чем восстановительные. Пероксиды и надпероксиды, как сильные окислители, легко разлагаются разбавленными кислотами и водой:
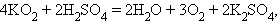
| ||
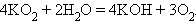
| ||
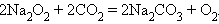
|
Последняя реакция используется для получения кислорода в подводных лодках и космических кораблях.
Гидроксиды s-элементов получают при взаимодействии оксидов с водой. Большой ионный радиус s-элементов делает их гидроксиды сильными основаниями, а увеличение радиуса в группе сверху вниз приводит к усилению основности гидроксидов от Li к Cs и от Mg к Ba; амфотерен только Be(OH)2.
Из-за малого радиуса атома энергия связи в молекуле водорода наибольшая из всех атомных гомонуклеарных молекул VIIА и IА групп:
|
Водород следует рассматривать как не имеющий полных аналогов химический элемент, поэтому его помещают либо в первую, либо в седьмую группу. К группе галогенов водород можно отнести из-за легкой замещаемости водорода галогенами в органических соединениях и способности к образованию аниона H– (гидрид-иона).
Второй элемент первого периода – гелий – формально входит в VIIIА подгруппу. Гелий – типичный инертный элемент, его неспособность вступать в химическое взаимодействие с другими элементами предопределена устойчивостью его электронной конфигурации 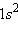 . К типично химическим соединениям можно отнести лишь молекулярный ион
. К типично химическим соединениям можно отнести лишь молекулярный ион 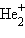 и гидрид гелия HeH с электронной формулой
и гидрид гелия HeH с электронной формулой 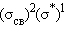 и кратностью связи 0,5.
и кратностью связи 0,5.
p-Элементы имеют общую электронную конфигурацию ns2np1–6 и образуют подгруппы IIIА, IVА, VА, VIА, VIIА и VIIIА периодической системы.
В подгруппе IIIА рассматривают отдельно B, Al и подгруппу галлия (Ga, In, Tl), в IVА – C, Si и подгруппу германия (Ge, Sn, Pb), в VА – N, P и подгруппу мышьяка (As, Sb, Bi), в VIА – O и подгруппу халькогенов (S, Se, Te, Po), в VIIА – галогены (F, Cl, Br, I, At), в VIIIА – Ne, Ar и подгруппу криптона (Kr, Xe, Rn).
В отличие от s-элементов, p-элементы поливалентны (табл. 8.5). Высшие положительные степени окисления равны номеру группы, отрицательные – числу неспаренных электронов для элементов IVА–VIIА подгрупп. Для элементов подгруппы Kr возможны только формально положительные четные степени окисления.
При переходе сверху вниз в подгруппах возрастает разница энергий s- и p-подуровней, поэтому легким элементам свойственны высшие степени окисления, тяжелым – низшие. Так, в подгруппе IVА стабильность соединений Э2+ возрастает в ряду Ge2+ < Sn2+ < Pb2+. В той же последовательности уменьшается устойчивость соединений Э4+.
Восстановительные свойства p -элементов в группе сверху вниз усиливаются, а окислительные ослабевают.
Кислотно-основные свойства соединений, содержащих группировку Э–O–H, определяются относительной прочностью связей Э–О и О–Н. Если связь Э–О прочнее связи О–Н, то гидроксид диссоциирует по кислотному типу Э–О–Н = Э–О– + H+. Если прочнее связь О–Н, то соединение диссоциирует как основание Э–О–Н = Э+ + OH–. Связь Э–О тем прочнее, чем больше заряд и меньше радиус иона элемента. Увеличение заряда и уменьшение радиуса Э усиливает связь Э–О, делает ее более ковалентной, а следовательно, более ионной и менее прочной связь О–Н.
На основании этих представлений можно сформулировать некоторые закономерности в изменении кислотно-основных свойств гидроксидов p-элементов:
1) При одинаковой степени окисления кислотные свойства гидроксидов в группе сверху вниз уменьшаются вследствие роста эффективного радиуса иона Эn+.
Так, в IIIА группе происходит усиление основных свойств: H3BO3 – кислота, Al(OH)3 и Ga(OH)3 – амфотерные соединения, In(OH)3 – амфотерный гидроксид с преобладанием основной ионизации, Tl(OH)3 – основание.
В IVА группе Ge(OH)2, Sn(OH)2, Pb(OH)2 – амфотерные соединения, их основность растет от Ge к Pb; у Ge(OH)2 преобладает кислотная ионизация, у Pb(OH)2 – основная.
В VА группе также наблюдается общая закономерность: HNO2 и H3PO3 – слабые кислоты, H3AsO3 – амфотерная кислота, Sb(OH)3 – амфотерное основание, Bi(OH)3 – основание. Все гидроксиды p-элементов VIА и VIIА групп являются кислотами. Сила кислот уменьшается сверху вниз в каждой группе. Так, H2SO4 и H2SeO4 – сильные кислоты, теллуровая H2TeO4 – слабая кислота. В ряду слабых кислот SO2 · H2O – H2SeO3 – H2TeO3 у теллуристой кислоты проявляется амфотерность. Кислотные свойства также ослабевают от Cl к I, например, HClO и HBrO – слабые кислоты, а HIO – амфотерное соединение.
2) С увеличением положительной степени окисления элемента уменьшается эффективный радиус, поэтому кислотные свойства гидроксидов усиливаются. Так, SO2 · H2O и HNO2 – слабые кислоты, а H2SO4 и HNO3 – сильные; TlOH – сильное основание, Tl(OH)3 – слабое; Pb(OH)2 – гидроксид основного характера, PbO2 · nH2O – кислотного.
3) Кислотные свойства гидроксидов в периоде возрастают с ростом Z. Это объясняется тем, что в результате увеличения заряда растет ковалентность связи Э–О и, как следствие этого, ионность связи О–Н.
Как известно, p-элементы второго периода по свойствам мало похожи на своих аналогов третьего и последующего периодов. Примером тому могут служить диоксиды углерода CO2 и кремния SiO2.
Трудно найти другие два электронных аналога, обладающими такими различиями: диоксид углерода CO2 – газ, диоксид кремния (кремнезем) SiO2 – очень твердое вещество, плавящееся при 1710 °C. Диоксид углерода существует в мономерном состоянии в виде молекул с двойными связями между углеродом и кислородом (О=С=О). Диоксид кремния образует непрерывную сетку, в которой нет двойных связей: каждый атом кремния связан с четырьмя атомами кислорода, и каждый атом кислорода в свою очередь связан с двумя атомами кремния.
Резко отличаются свойства соединений других аналогов – азота и фосфора, кислорода и серы. Если N2 и O2 – газообразные вещества, молекулы которых имеют кратные связи, (N≡N, O=O), то простые соединения фосфора и серы – полимерные кристаллические вещества. Наиболее устойчивы четырехатомные молекулы P4, имеющие форму тетраэдра, и циклические молекулы S8.
Наблюдаемые отличия в химических свойствах p -элементов третьего периода от свойств их аналогов второго периода связаны с появлением в третьем периоде свободного d -подуровня, способного участвовать в образовании химических связей. Влияние свободных d -орбиталей проявляется в следующем:
1) Возбужденные p -электроны занимают d -орбитали, увеличивая тем самым валентные возможности элементов. Так, в отличие от кислорода (2 s 22 p 4), у серы (3 s 23 p 43 d 0) осуществляется переход двух электронов на 3 d -подуровень. Степень окисления серы достигает шести, а sp 3 d 2-гибридизация определяет октаэдрическое строение SF6. Степень окисления фосфора в соединениях PCl5 и KPCl6 равна +5, а координационное число – пяти (sp 3 d -гибридизация) и шести (sp 3 d 2-гибридизация).
2) Благодаря d -орбиталям в соединениях элементов третьего периода связи упрочняются. Так, в ионах 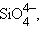
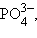
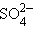 кроме σ-связей, образованных sp 3-гибридными орбиталями центрального атома и p -орбиталями кислорода, возникает дополнительное связывание за счет свободных 3 d -орбиталей кремния, фосфора, серы и неподеленных электронных пар кислорода. Это связывание стабилизирует основные σ-связи. Поэтому, несмотря на увеличение радиуса кремния по сравнению с углеродом, связи Si–O (445 кДж), Si–F (567 кДж), Si–Cl (382 кДж) прочнее связей С–О (359 кДж), C–F (487 кДж) и C–Cl (340 кДж). Однако связь Si–H (319 кДж) слабее связи C–H (414 кДж) из-за отсутствия не поделенных электронных пар у водорода, так же как связь Si–Si (222 кДж) слабее связи С–С (348 кДж) из-за увеличения ковалентного радиуса кремния.
кроме σ-связей, образованных sp 3-гибридными орбиталями центрального атома и p -орбиталями кислорода, возникает дополнительное связывание за счет свободных 3 d -орбиталей кремния, фосфора, серы и неподеленных электронных пар кислорода. Это связывание стабилизирует основные σ-связи. Поэтому, несмотря на увеличение радиуса кремния по сравнению с углеродом, связи Si–O (445 кДж), Si–F (567 кДж), Si–Cl (382 кДж) прочнее связей С–О (359 кДж), C–F (487 кДж) и C–Cl (340 кДж). Однако связь Si–H (319 кДж) слабее связи C–H (414 кДж) из-за отсутствия не поделенных электронных пар у водорода, так же как связь Si–Si (222 кДж) слабее связи С–С (348 кДж) из-за увеличения ковалентного радиуса кремния.
Благородные газы имеют электронную конфигурацию ns2np6 (у гелия 1s2) и составляют VIIIА группу. По мере возрастания порядкового номера растут радиусы атомов и их поляризуемость. Это приводит к усилению межмолекулярных взаимодействий, к повышению температур плавления и кипения, к увеличению растворимости газов в воде и других растворителях. Для благородных газов известны следующие группы соединений: молекулярные ионы, соединения включения и валентные соединения.
К d -элементам относят те элементы, атомы которых содержат валентные электроны на (n – 1)d ns-уровнях и составляют побочные (IIIВ–VIIВ, IВ, IIВ) подгруппы, занимая промежуточное положение между типичными s-металлами (IА, IIА) и p-элементами. Из 109 элементов периодической системы 37 относятся к d-элементам; из них последние 7 радиоактивны и входят в незавершенный седьмой период. Электронное строение атомов d-элементов определяет их химические свойства. 3d-Элементы по химическим свойствам существенно отличаются от 4d- и 5d-элементов. При этом элементы IVВ–VIIВ подгрупп очень схожи по многим химическим свойствам. Это сходство обусловлено лантаноидным сжатием, которое из-за монотонного уменьшения радиусов при заполнении 4f-орбиталей приводит к практическому совпадению радиусов циркония и гафния, ниобия и тантала, молибдена и вольфрама, технеция и рения. Элементы этих пар очень близки по физическим и особенно по химическим свойствам; первые шесть элементов встречаются в одних рудных месторождениях, трудно разделяются; их иногда называют элементами-близнецами.
Атомы d-элементов характеризуются общей электронной формулой (n – 1)d1–10ns0–2. Некоторые из тяжелых d-элементов не являются полными электронными аналогами.
Отличительной особенностью переходных элементов является образование фаз переменного состава. Это, во-первых, твердые растворы внедрения и замещения и, во-вторых, соединения переменного состава. Твердые растворы образуются элементами с близкими электроотрицательностями, атомными радиусами и одинаковыми кристаллическими решетками. Чем больше отличаются элементы по своей природе, тем менее они растворяются друг в друге и тем более склонны к образованию химических соединений. Такие соединения могут иметь как постоянный, так и переменный состав. В отличие от твердых растворов, в которых сохраняется решетка одного из компонентов, для соединений характерно образование новой решетки и новых химических связей. Другими словами, к химическим соединениям относят лишь те фазы переменного состава, которые резко отличаются по строению и свойствам от исходных.
Для соединений переменного состава характерны следующие особенности:
а) Состав этих соединений зависит от способа получения. Так, в зависимости от условий синтеза оксиды титана имеют состав TiO1,2–1,5 и TiO1,9–2,0; карбиды титана и ванадия – TiC0,6–1,0 и VС0,58–1,09, нитрид титана TiN0,45–1,00.
б) Соединения сохраняют свою кристаллическую решетку при значительных колебаниях количественного состава, то есть имеют широкую область гомогенности. Так, TiC0,6–1,0, как следует из формулы, сохраняет решетку карбида титана при недостатке в ней до 40 % атомов углерода.
в) Природа связи в таких соединениях определяется степенью заполнения d -орбиталей металла. Электроны внедренного неметалла заселяют вакантные d -орбитали, что приводит к усилению ковалентности связей. Именно поэтому доля металлической связи в соединениях начальных элементов d -рядов (IV–V групп) понижена.
Наличие ковалентной связи в них подтверждается большими положительными энтальпиями образования соединений, более высокими твердостью и температурой плавления, меньшей электропроводностью по сравнению с образующими их металлами
f-Элементы делятся на лантаноиды и актиноиды.
Лантаноиды - семейство из 14 элементов (4f-элементы), следующих за La, общий символ Ln. Электронные конфигурации Ln отражают внутреннюю периодичность, проявляющуюся в некоторых свойствах Ln3+, у которых 4f-орбитали заполняются сначала по одному (подсемейство церия: Ce – Gd), а потом по второму электрону (подсемейство тербия: Tb – Lu). Уменьшение атомных и ионных радиусов приводит к лантаноидному сжатию, вследствие которого элементы, следующие за Lu, по своим свойствам оказываются очень похожими на своих предшественников по группам (Zr и Hf, Nb и Ta, Mo и W, Tc и Re). Cеребристо-белые металлы, тускнеющие во влажном воздухе, при нагревании разлагают воду, взаимодействуют со всеми кислотами (кроме H3PO4 и HF), образуя преимущественно ионы Ln3+, другие степени окисления свойственны Ce, Pr, Tb, Dy (4+), Sm, Eu, Tm, Yb (2+). С H, B, C, N, O, халькогенами, галогенами образуют вполне устойчивые соединения. По химическим свойствам достаточно схожи, разделяют ионообменной хроматографией и экстракцией. Разделенные Ln3+ используют для получения химических соединений с нужными люминесцентными, спектроскопическими и магнитными свойствами, изготовления неодимовых стекол (лазеры), люминесцентных преобразователей (приборы ночного видения), изготовления постоянных магнитов (SmCo5). Основная доля используется в виде смесей металлов или оксидов и других соединений с природным содержанием Ln для изготовления катализаторов, легирующих добавок в металлургии, полировочных паст, аккумуляторов газообразного водорода (LnNi5) и др.
Актиноиды - семейство из 14 элементов, следующих за Ac, (5f-семейство), общий символ An. Первые три – Th, Pa, U – встречаются в природе, их наиболее долгоживущие изотопы – 232Th (T1/2 = 1,4·1010 лет), 231Pa (T1/2 = 3,43·104 лет), 238U (T1/2 = 4,5·109 лет). Остальные An были получены ядерным синтезом в лабораториях США и России, все радиоактивны. Делятся на два подсемейства Th – Cm (цискюриды) и Bk – Lr (транскюриды). Первое подсемейство во многом отличается от соответствующих лантаноидов, проявляя помимо An3+ и более высокие степени окисления An4+ (Th, Pa, Am, Cm), An4+, 5+, 6+ (U, Np, Pu) и даже Pu7+. Второе подсемейство по химическим свойствам ближе к соответствующим лантаноидам, хотя для менделевия известны соединения Md1+, а для лоуренсия – Lr4+.
Лантаноиды – элементы, у которых к электронной конфигурации лантана последовательно добавляются 14 4f-электронов. Общая электронная конфигурация лантаноидов – 4f2–145d0–16s2. Электронные конфигурации и степени окисления 4 f -элементов (лантаноидов) представлены в Приложении В.
Периодический характер заполнения 4 f -орбиталей сначала по одному, а потом по два электрона предопределяет внутреннюю периодичность свойств лантаноидов. Периодически изменяются металлические радиусы, степени окисления, температуры плавления и кипения, величины магнитных моментов, окраска и другие свойства
Электрохимический ряд напряжений металлов позволяет определить химическую активность металлов. Чем ниже значение стандартного окислительно-восстановительного потенциала, тем активнее металл и сильнее его восстановительные свойства.
Стандартные окислительно-восстановительные потенциалы представлены в Приложении Б.
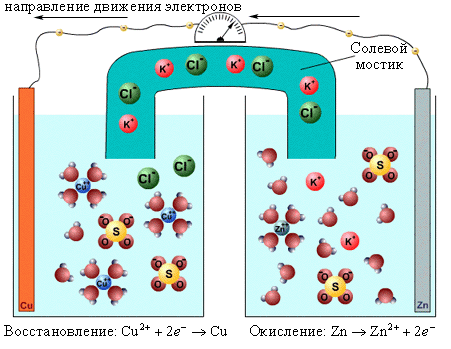
Если процессы окисления и восстановления пространственно разделить, то любую окислительно-восстановительную реакцию можно использовать для получения электрической энергии. Такие устройства называют химическими источниками тока (ХИТ). Простейший ХИТ – гальваническая ячейка (рис. 9) – представляет собой сосуды, в которых два электрода, помещенные в раствор соответствующих электролитов, соединены солевым мостиком, представляющим собой стеклянную трубку, заполненную раствором такого электролита, катионы и анионы которого характеризуются одинаковой подвижностью.
|
| Рисунок 9 - Гальванический элемент Даниэля–Якоби |
При замыкании внешней цепи начинается окислительно-восстановительная реакция, о чем свидетельствует возникновение электродвижущей силы (ЭДС).
Реакция CuSO4 + Zn = Cu + ZnSO4 в электрохимическом варианте является основой гальванического элемента Даниэля–Якоби, схема которого
(–)Zn¦Zn2+||Cu2+¦Cu(+)
отражает современную систему обозначений для гальванических элементов. Слева записывается анод Zn¦Zn2+, на котором возникает избыток электронов и происходит процесс окисления – отрицательный полюс (–). Справа – катод Cu2+¦Cu – электрод с недостатком электронов, положительный полюс (+). Одна вертикальная черта изображает фазовый раздел между металлом и раствором электролита. Двойная вертикальная линия отделяет анодное пространство от катодного.
Электроны по внешнему участку цепи, металлическому проводнику, переходят от отрицательного полюса к положительному. Внешнюю цепь на схеме не изображают. В круглых скобках знаками плюс и минус обозначают полюсы электродов.
Если малоактивный металл погружен в раствор соли с концентрацией больше равновесной, то происходит переход ионов из раствора на металл, заряженный положительно). В любом случае возникает двойной электрический слой, и появляется разность электрических потенциалов, или гальвани-потенциал.
Система, состоящая из металла, погруженного в раствор электролита, называется электродом, то есть электроды в электрохимии – это системы из двух токопроводящих тел.
Потенциал электрода зависит от активности ионов 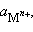 . Разность потенциалов стандартного водородного электрода и какого-нибудь другого электрода, измеренная при стандартных условиях, называется стандартным электродным потенциалом и обозначается E °.
. Разность потенциалов стандартного водородного электрода и какого-нибудь другого электрода, измеренная при стандартных условиях, называется стандартным электродным потенциалом и обозначается E °.
Каждый гальванический элемент состоит из двух электродов (окислительно-восстановительных пар), один из которых является поставщиком электронов (анод), а другой их принимает (катод). В гальванических элементах источником электрического тока является химическая реакция.
Любая химическая реакция термодинамически разрешена, если ΔG < 0. Из соотношений ΔG = –nFE и ΔG° = –nFE° следует, что электрохимическая реакция, а в общем случае любая окислительно-восстановительная реакция может протекать самопроизвольно, если E > 0 или для стандартных условий E° > 0.
ЭДС гальванического элемента равна разности электродных потенциалов составляющих его электродов. В соответствии с принятой формой записи гальванического элемента его ЭДС равна электродному потенциалу правого электрода (окислителя) минус электродный потенциал левого электрода (восстановителя).

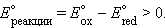
Пользуясь этими соотношениями и таблицей стандартных электродных потенциалов, можно предсказать возможность осуществления многих окислительно-восстановительных реакций.
В случае элемента Даниэля–Якоби (–)Zn¦Zn2+||Cu2+¦Cu(+)
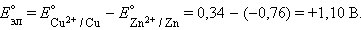
Для нестандартных условий ЭДС элемента Даниеля–Якоби находится из разности электродных потенциалов, вычисленных по уравнению Нернста:
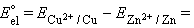
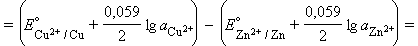
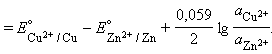
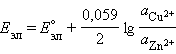
Для реакции
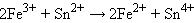
| ||
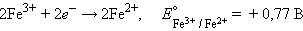
| ||
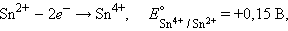
|
осуществляемой в элементе 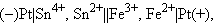
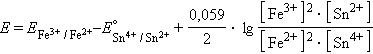
Величины электродных потенциалов определяются концентрациями (активностями) всех ионов, участвующих в окислительно-восстановительной реакции. Так, в элементе
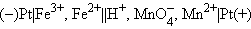
протекает реакция
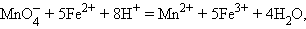
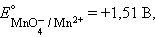 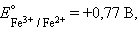
|
и уравнение Нернста для этого элемента имеет вид:
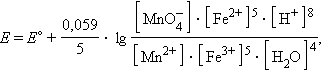
| ||
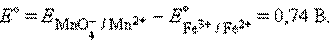
|
Вуравнении Нернста для реакции под знаком логарифма в числителе стоят концентрации исходных веществ, а в знаменателе – продуктов реакции в степенях стехиометрических коэффициентов.
Итак, сопоставляя электродные потенциалы соответствующих систем, можно заранее определить направление, в котором будет протекать окислительно-восстановительная реакция при любых (нестандартных) условиях. Окисленная форма вещества с более высоким потенциалом является окислителем для восстановленных форм с более низким потенциалом.
Однако в большинстве случаев о направлении реакции можно судить по разности стандартных электродных потенциалов 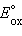 –
– 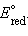 В случае, когда эта разность близка к нулю, для определения направления реакции используют разность не стандартных, а реальных (с учетом активности ионов) потенциалов, вычисленных по уравнению Нернста.
В случае, когда эта разность близка к нулю, для определения направления реакции используют разность не стандартных, а реальных (с учетом активности ионов) потенциалов, вычисленных по уравнению Нернста.
Равновесное состояние любой окислительно-восстановительной реакции характеризуется нулевой ЭДС (Δ G равн = 0). Тогда из уравнения Нернста следует
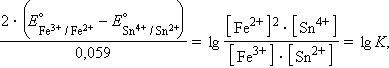
то есть представляется возможность определить константу равновесия из электрохимических данных.
При 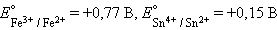
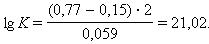
Следовательно, реакция 2Fe3+ + Sn2+ = 2Fe2+ + Sn4+ будет самопроизвольно протекать слева направо, поскольку константа равновесия ее очень велика (K = 1 · 1021).
В общем виде связь ЭДС с K выражается уравнением
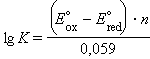
Электрохимическая коррозия. В основе коррозийных процессов лежат окислительно-восстановительные реакции металлов с окружающей средой, сопровождающиеся переходом металлов в более термодинамически устойчивое состояние.
Рассмотрим коррозию железа как электрохимический процесс. Ржавление железа есть не что иное, как анодная реакция
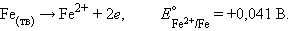
Катодная реакция – восстановление атмосферного кислорода:
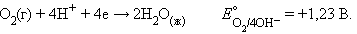
Водородные ионы поставляет вода. Если бы в воде не было растворенного кислорода, то коррозия была бы невозможна. Следовательно, железо корродирует в слое воды, насыщенном кислородом. Таким образом, начальную стадию коррозии железа можно передать реакцией
2Fe + O2 + 4H+ → 2FeO + 2H2O
На скорость коррозии существенное влияние оказывает концентрация ионов H+. Повышение pH приводит к замедлению коррозии, поскольку восстановление O2 из H2O замедляется. При pH = 9–10 коррозия железа практически прекращается.
Известно, что в водной среде ионы Fe2+ в присутствии кислорода окисляются до Fe3+. Вторая стадия коррозии соответствует реакции образования гидратированного оксида железа (ржавчины) Fe2O3∙nH2O (рис. 10):
4Fe2+ + O2 + 4H2O + xH2O = 2Fe2O3∙xH2O + 8H+
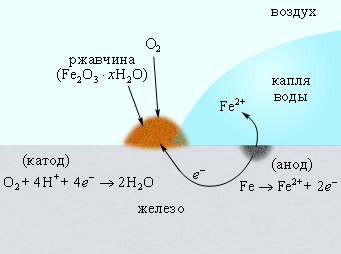
Рисунок 10 - Коррозия железа кислородом воздуха, растворенным в воде
Для защиты железа от коррозии используются всевозможные покрытия: краска, слой металла (олова, цинка). При этом краска и олово предохраняют от коррозии до тех пор, пока защитный слой цел.
Появление в нем трещин и царапин способствует проникновению влаги и воздуха к поверхности железа, и процесс коррозии возобновляется, причем в случае оловянного покрытия он даже ускоряется, поскольку олово служит катодом в электрохимическом процессе (рис. 11).
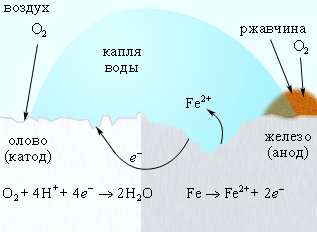
|
| Рисунок 11 - Коррозия «белой жести» |
Оцинкованное железо ведет себя иначе. Поскольку цинк выполняет роль анода, то его защитная функция сохраняется и при нарушении цинкового покрытия (рис12).
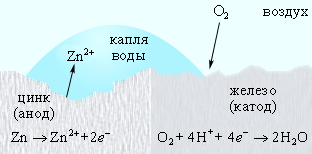
Рисунок 12 - Катодная защита в оцинкованном железе
Катодная защита широко используется для уменьшения коррозии подземных и подводных трубопроводов и стальных опор высоковольтных передач, нефтяных платформ и причалов.
 2014-02-24
2014-02-24 2429
2429








