Рассмотрим термодинамическую систему, представляющую собой идеальный газ. Химический потенциал идеального газа равен:
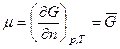 ,
,
где 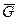 – мольная энергия Гиббса (изобарный потенциал 1 моль идеального газа).
– мольная энергия Гиббса (изобарный потенциал 1 моль идеального газа).
Так как
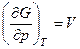 ,
,
то 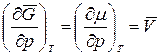 ,
,
где 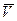 – мольный объем идеального газа (объем 1 моль газа).
– мольный объем идеального газа (объем 1 моль газа).
Если процесс протекает при Т = const, частную производную можно заменить полной. Тогда
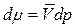
Уравнение состояния 1 моль идеального газа:
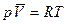 ;
;
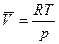 ,
,
тогда
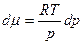
Проинтегрируем в интервале от р0 до р:
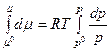
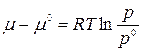
где μ 0, р 0 – химический потенциал и давление идеального газа в стандартном состоянии.
За стандартное состояние принято состояние идеального газа при р 0= 1 атм.
Тогда
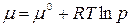 . (2.3)
. (2.3)
Стандартный химический потенциал – это химический потенциал при давлении газа 1 атм. Химический потенциал в стандартном состоянии μ 0 зависит только от температуры и не зависит от давления, т.е. μ 0 = f(T). Из уравнения (2.3) видно, что под знаком логарифма стоит безразмерная величина, равная отношению давления р к стандартному давлению р 0 = 1 атм.
Поскольку μ = 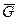 , можно записать
, можно записать
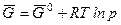
где 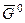 – стандартная мольная энергия Гиббса.
– стандартная мольная энергия Гиббса.
 2014-02-12
2014-02-12 1627
1627








