Рассмотрим систему, состоящую из k независимых компонентов и m фаз, находящуюся в состоянии термодинамического равновесия при р, Т = const. Общее условие равновесия в системе имеет вид:
dG = 0.
Общая энергия Гиббса складывается из энергий Гиббса каждой из фаз:
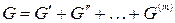 .
.
Продифференцируем:
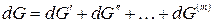 .
.
Для каждой из фаз
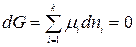 .
.
Подставим значение dG для каждой фазы:
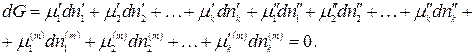
Пусть без нарушения равновесия из первой фазы во вторую перешло бесконечно малое число моль 1-го компонента. При этом числа моль всех остальных компонентов постоянны во всех фазах и значения внешних параметров не изменяются: р, Т = const. Тогда условие равновесия приобретает вид:
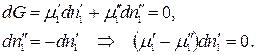
Произведение равно нулю, если хотя бы один из множителей равен нулю, но согласно условию 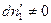 , тогда
, тогда
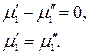
Следовательно, химический потенциал первого компонента одинаков в обеих фазах. Рассматривая аналогичные частные случаи для других компонентов и фаз, получим:
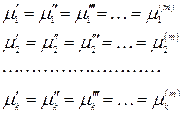
Полученное уравнение является условием равновесия в m -фазной
k -компонентной системе и называется теоремой равновесия Гиббса:
условием термодинамического равновесия в гетерогенной системе является равенство химических потенциалов каждого компонента во всех фазах при Р, Т = const или V, Т = const
В качестве примера рассмотрим двухфазную трехкомпонентную систему. Условие равновесия для такой системы имеет вид:
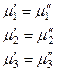 ,
,
где 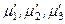 – химические потенциалы 1, 2 и 3-го компонентов в одной фазе;
– химические потенциалы 1, 2 и 3-го компонентов в одной фазе;
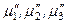 – химические потенциалы 1, 2 и 3-го компонентов в другой фазе.
– химические потенциалы 1, 2 и 3-го компонентов в другой фазе.
 2014-02-12
2014-02-12 3376
3376
