ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА ТЕПЛОВЫЕ ЭФФЕКТЫ
ЛЕКЦИЯ 3
Температура оказывает большое влияние на тепловой эффект химических реакций. Количественно охарактеризуем это влияние.
а.) Рассмотрим процесс, протекающий при 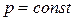 . Пусть энтальпия исходных веществ, участвующих в данном процессе, будет
. Пусть энтальпия исходных веществ, участвующих в данном процессе, будет 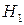 , а энтальпия веществ в конечном состоянии
, а энтальпия веществ в конечном состоянии 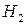 . Если в системе протекает реакция:
. Если в системе протекает реакция:
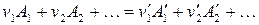 ,
,
то, с учетом (24), изобарная теплоемкость системы в исходном состоянии:
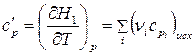 , (37)
, (37)
для продуктов реакции:
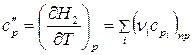 . (38)
. (38)
Вычтем почленно уравнение (38) из (37), получим:
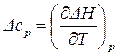 , (39)
, (39)
где 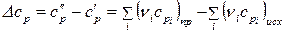 – разность между суммами.
– разность между суммами.
б.) 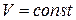
Аналогично для процесса, протекающего при постоянном объеме изохорная теплоемкость системы для исходных веществ и продуктов реакции:
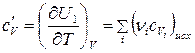 ,
,
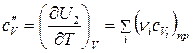 .
.
Следовательно,
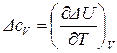 , (40)
, (40)
где 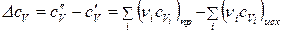 .
.
Уравнения (39) и (40) дифференциальная форма записи закона Кирхгоффа: температурный коэффициент теплового эффекта химической реакции (термодинамического процесса), протекающей при 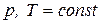 или
или 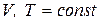 , равен разности сумм мольных теплоемкостей продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов.
, равен разности сумм мольных теплоемкостей продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов.
Температурный коэффициент – это производная, которая показывает на сколько изменяется величина (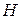 или
или 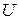 ) при изменении температуры на 1 град.
) при изменении температуры на 1 град.
В дальнейшем ограничимся рассмотрением только процессов, протекающих при 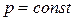 , т.к. при
, т.к. при 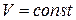 все аналогично.
все аналогично.
В уравнении (39) разделим переменные 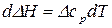 и проинтегрируем его в пределах от 0 до
и проинтегрируем его в пределах от 0 до 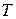 , получим:
, получим:
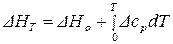 – интегральная форма записи закона Кирхгоффа.
– интегральная форма записи закона Кирхгоффа.
где 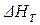 ,
, 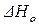 – тепловой эффект процесса при температуре
– тепловой эффект процесса при температуре 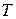 и при абсолютном нуле температуры.
и при абсолютном нуле температуры.
Для расчета по этому уравнению теплового эффекта процесса при любой температуре необходимо знать зависимость 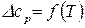 в интервале от 0 до
в интервале от 0 до 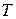 и
и 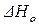 .
. 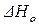 можно определить, имея набор экспериментальных данных, методами статистической термодинамики. Но получить такие данные не возможно. Т.е. данное уравнение имеет скорее теоретическое, чем практическое значение.
можно определить, имея набор экспериментальных данных, методами статистической термодинамики. Но получить такие данные не возможно. Т.е. данное уравнение имеет скорее теоретическое, чем практическое значение.
Гораздо удобнее с практической точки зрения провести интегрирование уравнения (39) в определенных пределах от 298 до 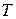 . В результате получим:
. В результате получим:
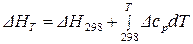 , (41)
, (41)
где 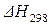 – тепловой эффект процесса при стандартных условиях. Рассчитывается методами статистической термодинамики на основании экспериментальных данных. Значения
– тепловой эффект процесса при стандартных условиях. Рассчитывается методами статистической термодинамики на основании экспериментальных данных. Значения 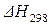 приведены в справочнике.
приведены в справочнике.
Зависимость 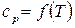 теплоемкости веществ в интервале температур от 298 до
теплоемкости веществ в интервале температур от 298 до 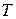 чаще всего выражается экспериментальным уравнением вида:
чаще всего выражается экспериментальным уравнением вида:
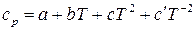 , (31)
, (31)
Тогда для реакции (процесса):
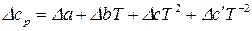 ,
,
где 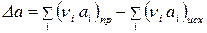 ;
;
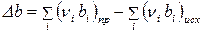 и т.д.
и т.д.
Пример: для реакции 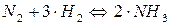
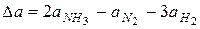 ;
;
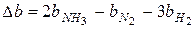 и. т.д.
и. т.д.
После подстановки значения 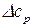 в уравнение (41) и его интегрирования, получим:
в уравнение (41) и его интегрирования, получим:
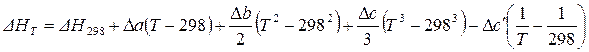 . (42)
. (42)
Уравнение (42) позволяет производить расчет теплового эффекта процесса при любой температуре.
На практике можно встретиться со случаем, когда в интервале температур от 298 до 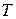 одно из реагирующих веществ изменяет свое агрегатное состояние, т.е. имеет место фазовый переход (ф.п.). В этом случае интервал интегрирования разбивается на 2 части: от 298 до
одно из реагирующих веществ изменяет свое агрегатное состояние, т.е. имеет место фазовый переход (ф.п.). В этом случае интервал интегрирования разбивается на 2 части: от 298 до 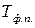 и от
и от 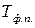 до
до 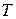 . Тогда с учетом величины теплового эффекта фазового перехода уравнение (41) перепишется:
. Тогда с учетом величины теплового эффекта фазового перехода уравнение (41) перепишется:
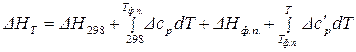 .
.
Если несколько веществ изменяют агрегатное состояние, то температурный интервал разбивается на соответствующее число интервалов и уравнение (41) аналогично преобразуется.
 2014-02-12
2014-02-12 851
851








