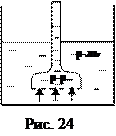 В сосуд, заполненный индивидуальной жидкостью, например, водой, поместим другой сосуд, с днищем из полупроницаемой мембраны, через которую способны проникать молекулы растворителя, но не могут проникать молекулы растворенного вещества из раствора, которым заполнен внутренний сосуд (рис. 24).
В сосуд, заполненный индивидуальной жидкостью, например, водой, поместим другой сосуд, с днищем из полупроницаемой мембраны, через которую способны проникать молекулы растворителя, но не могут проникать молекулы растворенного вещества из раствора, которым заполнен внутренний сосуд (рис. 24).
Поскольку химический потенциал чистого растворителя во внешнем сосуде больше химического потенциала растворителя в растворе, которым заполнен внутренний сосуд, то в системе будет протекать процесс, направленный в сторону выравнивания химических потенциалов растворителя во внешнем и внутреннем сосудах. То есть растворитель начнет проникать из внешнего сосуда во внутренний через полупроницаемую мембрану. В результате уровень жидкости во внутреннем сосуде будет повышаться до тех пор, пока давление избыточного столба жидкости во внутреннем сосуде не скомпенсирует давление, под действием которого растворитель переходит из внешнего сосуда во внутренний. Это давление называют осмотическим. Осмотическое давление – это давление, которое нужно приложить к раствору для предотвращения проникновения растворителя в раствор через полупроницаемую перегородку. Осмотическое давление рассчитывают по уравнению
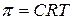 , (169)
, (169)
где 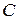 – молярность растворенного вещества.
– молярность растворенного вещества.
Уравнение Вант-Гоффа (169) показывает, что осмотическое давление разбавленного раствора равно давлению, которое оказывало бы растворенное вещество на стенки сосуда, если бы оно в виде идеального газа при той же температуре занимало объем, равный объему раствора (закон Вант-Гоффа).
Если известно осмотическое давление в разбавленном растворе можно определить молекулярный вес растворенного вещества. Выразим молярную концентрацию 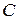 через массы растворителя
через массы растворителя 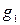 и растворенного вещества
и растворенного вещества 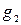 :
:
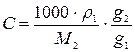 .
.
Подставляя последнее уравнение в (169), получим
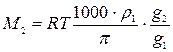 . (170)
. (170)
Если растворенное вещество способно к диссоциации или ассоциации в растворе, то осмотическое давление рассчитывают по формуле:
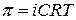 ,
,
где 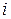 – изотонический коэффициент – учитывает диссоциацию и ассоциацию.
– изотонический коэффициент – учитывает диссоциацию и ассоциацию.
Явление осмоса лежит в основе различных методов очистки и разделения смесей, которые называют мембранными. Наиболее важным и распространенным методом очистки является диализ, основанный на удалении через полупроницаемую мембрану молекул и ионов из очищаемого раствора во внешний раствор при атмосферно давлении. Необходимую разность концентраций поддерживают путем обновления внешнего раствора. Диализ – процесс длительный.
Если со стороны раствора приложить внешнее давление, превышающее осмотическое, то растворитель будет переходить через полупроницаемую перегородку из раствора в чистый растворитель и будет идти концентрирование раствора. Данное явление называют обратным осмосом, а метод разделения жидких смесей – обратно-осмотическим.
Аналогично, но с использованием полупроницаемых мембран с бóльшим размером пор, разделяют системы, содержащие ВМС или вещества коллоидной степени дисперсности (КСД). В данном случае метод разделения называют ультрафильтрацией. Иначе, ультрафильтрация это диализ, который ведут при повышенном внешнем давлении.
Если система содержит более крупные частицы, то для разделения таких смесей используют полупроницаемые мембраны с еще большим размером пор, а метод разделения называют микрофильтрацией.
Обратный осмос, методы ультра- и микрофильтрации (баромембранные методы) широко применяют в пищевой промышленности. Обратный осмос используют для обессоливания воды и извлечения ценных компонентов. Ультрафильтрацию применяют для концентрирования соков, молока и др.
 2014-02-12
2014-02-12 684
684








