Электростатическая теория растворов
Для теоретического расчета среднего ионного коэффициента активности электролита Дебаем и Гюккелем разработана электростатическая теория разбавленных растворов сильных электролитов. В теории сделан ряд допущений:
1. ионы рассматривают как точечные заряды, при этом расстояния между ионами бесконечно велики по сравнению с размерами ионов;
2. учитывают только электростатическое взаимодействие между ионами в растворе, а всеми другими видами взаимодействий пренебрегают;
3. введено понятие ионной атмосферы, под которой подразумевают статистическое образование из противоположно заряженных ионов вокруг так называемого центрального иона. При этом электростатическое взаимодействие между ионами заменено взаимодействием между их ионными атмосферами.
4. диэлектрическая проницаемость раствора принимается равной диэлектрической проницаемости чистого растворителя.
На основе сделанных допущений получено уравнение для расчета среднего ионного коэффициента активности 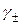 электролита:
электролита:
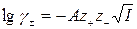 , (177)
, (177)
где 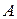 – теоретический коэффициент, зависящий от ДИЭЛЕКТРИЧЕСКОЙ проницаемости растворителя
– теоретический коэффициент, зависящий от ДИЭЛЕКТРИЧЕСКОЙ проницаемости растворителя 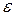 и температуры, для водного раствора при 298 К
и температуры, для водного раствора при 298 К 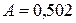 ;
;
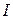 – ионная сила раствора:
– ионная сила раствора:
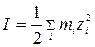 , (178)
, (178)
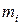 ,
, 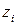 – моляльность и заряд
– моляльность и заряд 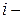 го иона.
го иона.
Уравнение (178) носит название предельного закона Дебая-Гюккеля: при данной ионной силе раствора средний ионный коэффициент активности электролита в предельно разбавленном растворе является величиной постоянной и не зависит от природы растворенного электролита.
Теория Дебая-Гюккеля позволяет рассчитать также коэффициент активности отдельного 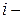 го иона
го иона 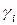 в растворе:
в растворе:
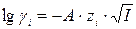 , (179)
, (179)
Закон Дебая-Гюккеля справедлив для предельно разбавленных растворов (с ионной силой 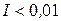 ). Достаточно строгой теории, которая позволила бы рассчитать значение среднего ионного коэффициента активности электролита в концентрированных растворах до сих пор не разработано.
). Достаточно строгой теории, которая позволила бы рассчитать значение среднего ионного коэффициента активности электролита в концентрированных растворах до сих пор не разработано.
 2014-02-12
2014-02-12 734
734








