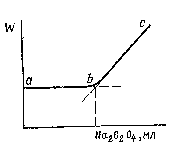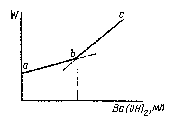точку эквивалентности находят, строя график зависимости электрической проводимости от объема израсходованного реактива.
При этом получают не менее четырех отсчетов электрической проводимости до точки эквивалентности и четыре – после точки эквивалентности.
Через полученные точки проводят прямые линии.
Точка пересечения этих линий соответствует точке эквивалентности.
Для уменьшения влияния разбавления на электрическую проводимость титрование, как правило, проводят в 10 – 20 раз более концентрированным раствором реактива.
Тип кривой, показанный на рисунке 2, получается во всех случаях, когда более
подвижный ион в процессе титрования заменяется менее подвижным.
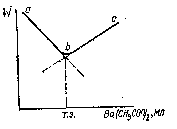
Рис.2. Кондуктометрическое титрование сульфата натрия ацетатом бария
в) Титрование ацетата кальция раствором оксалата натрия
Ca(CH3COO)2 + Na2C2O4 = Ca C2O4↓ + 2 CH3COO Na
При титровании ионы Ca2+(l(+) = 5,04 См · м2/кг-экв), заменяются ионами натрия Na+ (l(+) =
4,26 См · м2/кг-экв), что мало сказывается на общей электрической проводимости раствора. В этом случае в процессе титрования до достижения точки эквивалентности
электрическая проводимость будет практически оставаться неизменной, а после нее избыток Na2C2O4 вызовет резкое увеличение электропроводности (рис. 3).
|
г) Титрование сульфата натрия гидроксидом бария
Na2SO4 + Ba(ОН)2 = BaSO4↓ + 2 NaОН
В этом случае в процессе титрования подвижные ионы SO42- (l(-) = 6,87 См · м2/кг-экв) заменяются более подвижными гидроксид-ионами ОН- (l(-) = 17,40 См · м2/кг-экв), и до точки эквивалентности происходит постепенное возрастание общей электропроводимости, а за этой точкой – ее более резкое увеличение за счет избытка
Ba(ОН)2 (рис.4). Таким образом, в процессе титрования электрическая проводимость постоянно возрастает.
|
 2014-02-12
2014-02-12 2047
2047