| Элемент К+ AI3+ Zn2+ Fe2+ Нг Cu2+ Hg2+ Ag+ Pt+ Au+ Ен, В –2,92 –1,66 –0,763 –0,441 0,00 0,34 0,79 0,80 1,20 1,70 |
Электродный потенциал металла относительно водородного электрода вычисляется также по уравнению Нернста
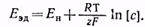
Следует, однако, помнить, что так же, как при вычислении мембранных потенциалов, в случае концентрированных растворов в уравнение Нернста вместо концентрации необходимо подставлять значение активности ионов в данном растворе.
Поскольку при выходе ионов металла в раствор сам металл заряжается отрицательно, то вследствие кулоновского притяжения избыточные ионы металла в растворе сосредоточиваются в тонком слое у поверхности металла, образуя двойной электрический слой (рис. а). Такие двойные слои возникают не только на границе раздела металл – жидкость, но и на границе раздела между любым твердым телом и жидкостью или двумя несмешивающимися жидкостями. Природа двойного слоя, помимо указанной, может быть обусловлена адсорбцией на поверхности ионов одного знака или ориентацией полярных молекул (например, молекул растворителя), в результате чего все молекулы оказываются обращенными одним и тем же концом к поверхности раздела (рис. 49,6). Адсорбироваться могут как катионы, так и анионы, но чаще адсорбируются анионы, так как они имеют меньших размеров гидратную оболочку.
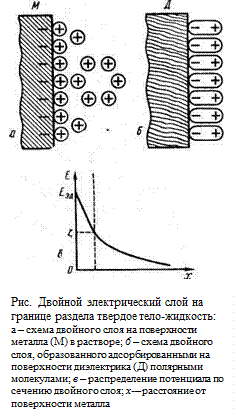 Ионы раствора, образующие внешнюю часть двойного электрического слоя, притягиваются к его внутренней части, находящейся внутри твердого тела. Силы притяжения убывают с расстоянием, и чем дальше от поверхности, тем менее эти силы могут противодействовать тепловому движению. Поэтому двойной слой имеет сложную структуру. У самой поверхности образуется его плотная часть толщиной d, примерно равной диаметру иона (слой Гельмгольца, который впервые ввел представление о двойном электрическом слое), и менее плотная, диффузная часть (слой Гуи). В этой части слоя плотность ионов убывает вследствие их диффузии в объем жидкости (см. рис.). Эффективная толщина двойного слоя имеет величину порядка нескольких ионных диаметров (0,1–0,5 нм). При движении частицы основная часть двойного слоя перемещается вместе с ней. Двойной электрический слой представляет собой своеобразный конденсатор. Поскольку расстояние между положительной и отрицательной обкладками его очень мало, то емкость конденсатора весьма значительна, достигая нескольких десятков мкФ на 1 см2, и внутри него действует большая напряженность поля (десятки МВ/м). Разность потенциалов между адсорбционным слоем, который может перемещаться вместе с частицей и окружающей средой, носит название электрокинетического, или z-потенциала (дзета-потенциала). Величина дзета-потенциала зависит от средней объемной плотности заряда в двойном слое, от его толщины и диэлектрической проницаемости среды, разделяющей поверхности слоя. Что касается знака дзета-потенциала, то он определяется соотношением между величинами диэлектрической проницаемости частицы и жидкости. Обычно из двух соприкасающихся тел положительным будет то, которое имеет большую диэлектрическую проницаемость. Например, стекло (e = 5) в воде (e = 81) имеет отрицательный дзета-потенциал, а в эфире (e = 4,3) приобретает положительный дзета-потенциал. Для частиц кварца, капель масла и пузырьков воздуха в воде дзета-потенциал имеет величину от 30 до 60 мВ.
Ионы раствора, образующие внешнюю часть двойного электрического слоя, притягиваются к его внутренней части, находящейся внутри твердого тела. Силы притяжения убывают с расстоянием, и чем дальше от поверхности, тем менее эти силы могут противодействовать тепловому движению. Поэтому двойной слой имеет сложную структуру. У самой поверхности образуется его плотная часть толщиной d, примерно равной диаметру иона (слой Гельмгольца, который впервые ввел представление о двойном электрическом слое), и менее плотная, диффузная часть (слой Гуи). В этой части слоя плотность ионов убывает вследствие их диффузии в объем жидкости (см. рис.). Эффективная толщина двойного слоя имеет величину порядка нескольких ионных диаметров (0,1–0,5 нм). При движении частицы основная часть двойного слоя перемещается вместе с ней. Двойной электрический слой представляет собой своеобразный конденсатор. Поскольку расстояние между положительной и отрицательной обкладками его очень мало, то емкость конденсатора весьма значительна, достигая нескольких десятков мкФ на 1 см2, и внутри него действует большая напряженность поля (десятки МВ/м). Разность потенциалов между адсорбционным слоем, который может перемещаться вместе с частицей и окружающей средой, носит название электрокинетического, или z-потенциала (дзета-потенциала). Величина дзета-потенциала зависит от средней объемной плотности заряда в двойном слое, от его толщины и диэлектрической проницаемости среды, разделяющей поверхности слоя. Что касается знака дзета-потенциала, то он определяется соотношением между величинами диэлектрической проницаемости частицы и жидкости. Обычно из двух соприкасающихся тел положительным будет то, которое имеет большую диэлектрическую проницаемость. Например, стекло (e = 5) в воде (e = 81) имеет отрицательный дзета-потенциал, а в эфире (e = 4,3) приобретает положительный дзета-потенциал. Для частиц кварца, капель масла и пузырьков воздуха в воде дзета-потенциал имеет величину от 30 до 60 мВ.
Строение двойного электрического слоя оказывает очень большое влияние на электрохимические явления на поверхности раздела двух веществ, в частности на поверхности клеточных мембран. Поэтому в биофизике разработаны специальные методы для измерения электроемкости двойного слоя, дзета-потенциала и других его характеристик.
 2014-02-13
2014-02-13 1027
1027








