Классификация основных процессов
Классификация основных процессов в технологии строительных материалов может быть проведена на основе различных признаков. Например, в зависимости от основных законов, определяющих скорость протекания процессов; по способу организации; в зависимости от изменения параметров процесса во времени; по направленности взаимодействующих потоков и др.
Так, в зависимости от закономерностей, характеризующих их протекание, процессы разделяют на пять основных групп.
Первая группа – механические процессы, основой которых является механическое воздействие на исходные материалы, описываемое законами механики твердых тел. К механическим процессам относятся измельчение твердых материалов, классификация (сортировка) сыпучих материалов, смешение и транспортировка твердых компонентов, формование изделий.
Вторая группа – гидромеханические процессы, скорость которых определяется законами гидродинамики – науки о движении жидкостей и газов. К ним относятся перемещение и перемешивание жидкостей и газов, разделение жидких неоднородных систем под действием сил тяжести (гравитационных сил) и центробежных (инерционных) сил (отстаивание, центрифугирование), а также движение твердых тел в жидкости или газе, псевдоожижение твердого зернистого материала.
Третья группа – тепловые процессы, скорость которых определяется законами теплопередачи – науки о способах распространения теплоты. В эту группу входят процессы нагревания, выпаривания, охлаждения и конденсации.
Четвертая группа – массообменные (диффузионные) процессы. Скорость этих процессов определяется скоростью перехода веществ из одной фазы в другую, т.е. законами массопередачи. К диффузионным процессам относятся абсорбция, ректификация, экстракция, кристаллизация, адсорбция и др.
В технологии строительных материалов тепловые и массообменные процессы протекают, как правило, одновременно. В связи с этим их нередко объединяют в одну группу. Типичным примером таких сопутствующих друг другу процессов является сушка.
Пятая группа – химические процессы, связанные с превращением веществ и изменением их химических свойств. Получение многих строительных материалов связано с различными химическими превращениями исходных компонентов. Таковы, например, реакции гидратации при твердении цемента, реакции декарбонизации при получении извести, реакции полимеризации и поликонденсации в технологии органических строительных материалов и др. Скорость этих процессов определяется закономерностями химической кинетики.
По способу организации основные процессы в технологии строительных материалов подразделяются на периодические, непрерывные и комбинированные.
Аппараты, в которых осуществляются периодические процессы, работают в циклическом режиме. Все стадии такого процесса протекают в одном месте (камере, аппарате), но в разное время. Примером может служить автоклавная обработка силикатного бетона – типичный химический процесс, осложненный массообменными (первоначальным увлажнением с последующим испарением влаги в конце процесса) и теплообменными процессами (нагревом и охлаждением материала).
Цикл автоклавной обработки состоит из следующих технологических операций: загрузка автоклава, подъем температуры с одновременным подъемом давления в автоклаве, изотермическая выдержка, охлаждение и выгрузка. Изделия во время автоклавирования находятся на месте и в разные временные периоды подвергаются различным температурным воздействиям. По окончании цикла автоклавирования все технологические операции повторяются.
Непрерывные процессы осуществляются в проточных аппаратах (установках) с непрерывной загрузкой исходных материалов и непрерывной выгрузкой продуктов, прошедших обработку. Все стадии такого процесса протекают в одно и то же время, но в разных местах аппарата. Характерным примером такого процесса может служить обжиг клинкера во вращающихся печах при производстве цемента.
Для более четкой характеристики периодических и непрерывных процессов используют следующие понятия и обозначения.
Продолжительность процесса (τ) – время, необходимое для завершения всех стадий процесса, начиная от момента загрузки исходных материалов и кончая выгрузкой готового продукта или полуфабриката.
Период процесса (t) – время, протекающее от начала загрузки исходных материалов данной партии до начала загрузки материалов следующей партии. Частное от деления продолжительности процесса на период процесса (τ/t) носит название степени непрерывности процесса (n). Для периодического процесса период процесса t ≥ τ, поэтому степень непрерывности n ≤ 1. Для непрерывного процесса период процесса t → 0 и степень непрерывности n → ∞.
Непрерывные процессы имеют значительные преимущества перед периодическими: возможность специализации аппаратуры для каждой операции (стадии) процесса, стабилизация процесса во времени, улучшение качества продукта, легкость регулирования и возможность автоматизации. Этими преимуществами объясняется неизменная тенденция перехода от периодических процессов к непрерывным.
Комбинированные процессы представляют собой либо непрерывный процесс, отдельные стадии которого проводятся периодически, либо такой периодический процесс, одна или несколько стадий которого проводятся непрерывно. Такие процессы также встречаются в технологии строительных материалов.
Различие между периодическими и непрерывными процессами касается только способа организации самого процесса и его аппаратурного оформления. Физико-химическая сущность процесса неизменна и не зависит от конструкции агрегата.
В зависимости от изменения параметров процесса во времени (скорость, давление, концентрация вещества) различают установившиеся (стационарные) процессы, значение каждого из параметров которых постоянны во времени, и неустановившиеся (нестационарные) процессы, значение параметров которых переменны во времени.
По направленности взаимодействующих потоков бывают прямоточные процессы, когда взаимодействующие вещества движутся в аппарате в одном направлении (например, пневмотранспорт) и противоточные процессы, когда движение взаимодействующих веществ осуществляется навстречу друг другу (например, при обжиге извести в шахтных печах).
При практических расчетах процессов и аппаратов обычно решаются следующие основные задачи:
1. Определение условий равновесного состояния системы;
2. Вычисление расходов исходных материалов и количества получаемого готового продукта или полуфабриката (составление материального баланса);
3. Определение необходимых расходов энергии для осуществления процесса (составление энергетического баланса);
4. Установление оптимальных режимов работы аппаратов и установление их основных размеров.
Очередность постановки этих задач и определяет содержание и последовательность инженерных расчетов. Рассмотрим содержание каждой задачи подробнее.
Первая задача. Начальным этапом расчета является расчет и анализ статики процесса, т.е. определение условий равновесия системы. Система, находящаяся в состоянии равновесия, не меняет своего состояния во времени. Для выведения такой системы из равновесия необходимо приложить к ней внешнюю силу. Определение направления протекания процесса в равновесных системах под действием внешней силы опирается на два основных положения термодинамики: принцип Ле Шателье – Брауна и правило фаз Гиббса.
Согласно первому принципу, направление сил, возникающих в системе, выведенной из состояния равновесия внешней силой, противоположно направлению этой силы. Рассматривая конкретные процессы на основе принципа Ле Шателье – Брауна, можно установить, какие параметры нужно изменять для изменения состояния системы в нужном для производства направлении.
Правило фаз Гиббса выражает зависимость между количеством компонентов системы k, фаз f и ее степеней свободы s. Степени свободы в термодинамике – независимые параметры состояния системы, находящейся в термодинамическом равновесии, которые можно изменять в определенных пределах так, чтобы сохранились все фазы, имевшиеся в системе, и не появились какие-либо новые фазы.
Согласно правилу фаз, соотношение между числом фаз f, числом компонентов k и числом термодинамических степеней свободы s имеет вид:
s + f = k + n,
где n – число внешних факторов, влияющих на положение равновесия в данной системе.
Правило фаз формулируется так: сумма числа степеней свободы системы и числа фаз равна сумме числа независимых компонентов и числа внешних факторов, влияющих на равновесие этой системы.
Применительно к процессам массопередачи внешними факторами, влияющими на равновесие системы, являются лишь температура и давление. Поэтому n = 2 и правило фаз принимает вид:
s = k - f + 2,
т.е. число степеней свободы равновесной термодинамической системы, на которую из внешних факторов влияют только температура и давление, равно числу независимых компонентов системы минус число фаз системы плюс два.
Правило фаз позволяет установить количество переменных, определяющих равновесие системы, которые могут быть выбраны произвольно. Из правила фаз следует, например, что для однокомпонентной системы (k = 1):
s = 3 - f,
т.е. такая система не может содержать больше трех равновесно существующих фаз. В качестве примера такой системы может служить вода.
Возможность одновременного существования всех трех фаз (твердой, жидкой, газообразной) в такой системе по правилу фаз определяется отсутствием степеней свободы (система является безвариантной):
s = k - f + 2 = 1 - 3 + 2 = 0.
Такая система может существовать только при строго определенных значениях температуры и давления (для воды t = 0,0075ºС и p = 4,579 мм рт. ст.). Изменение любого из этих условий приводит к исчезновению одной из фаз, и система становится двухфазной.
Наиболее интересной однокомпонентной системой является двухфазная система – жидкость и насыщенный пар. В этом случае
s = k - f + 2 = 1 - 2 + 2 = 1,
т.е. имеется одна степень свободы, и система является одновариантной. Следовательно, не нарушая фазового равновесия, можно произвольно менять либо температуру, либо давление. В таких системах строго однозначна зависимость между температурой и давлением насыщенного пара. Поэтому при изменении температуры пара одновременно будет соответственно меняться давление и, наоборот, при изменении давления соответственно меняется и температура. Для каждой жидкости можно, таким образом, построить кривую давления насыщенного пара.
Если система состоит из двух или большего числа компонентов, то ее положение и равновесие зависят не только от температуры и давления, но и от количественного состава фаз. Двухкомпонентная система, состоящая из двух фаз, по правилу фаз имеет две степени свободы:
s = 2 - 2 + 2 = 2,
что означает, что в таких системах можно без нарушения равновесия фаз менять одновременно два фактора – температуру и давление.
Для характеристики равновесного состояния этих систем один из факторов принимается постоянным, и тогда зависимость между другим фактором и составом фаз становится однозначной, т.е. при постоянном давлении каждой температуре, а при постоянной температуре каждому давлению соответствуют строго определенные составы фаз.
Вторая задача. Вычисление расходов исходных материалов и количества получаемого готового продукта или полуфабриката.
Эта задача решается на основе материального баланса. Материальный баланс основан на использовании закона сохранения массы. В общем виде для любой установки можно записать:
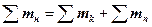 ,
,
где ∑mн – суммарная масса исходных продуктов; ∑mk – суммарная масса конечных продуктов;
∑mn – суммарная масса необратимых потерь.
Материальный баланс составляют для процесса в целом или для его отдельных стадий; для системы в целом или по одному из входящих в нее компонентов.
Пример. Для процесса сушки материальный баланс составляют как по всему влажному материалу, поступающему на сушку, так и по одному из его компонентов: массе абсолютно сухого вещества или массе влаги, содержащейся в высушиваемом материале.
Пусть m1 – масса влажного материала, поступившего на сушку, u1 – его влажность;
m2 – масса высушенного материала, u2 – его влажность; W – количество испарившейся влаги. Материальный баланс по всему количеству вещества запишется следующим образом:
m1 = m2 + W.
Материальный баланс по абсолютно сухому веществу, которое не меняется в процессе сушки, имеет вид:
mабс.сух. = m1 (1 – u1) = m2 (1 – u2).
Третья задача. Определение необходимых расходов энергии для осуществления процесса. Эта задача решается путем составления энергетического баланса.
Энергетический баланс составляется на основе закона сохранения энергии, согласно которому количество энергии, введенное в процесс, равно количеству выделившейся энергии. Частью энергетического баланса является тепловой баланс, который в общем виде выражается уравнением:
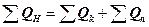 ,
,
где ∑QН – тепло, введенное в процесс; ∑Qк – отводимое тепло, которое складывается из тепла, удаляющегося с конечными продуктами и с отработанным теплоносителем;
∑Qn – потери тепла.
При этом вводимое тепло равно:
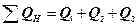 ,
,
где Q1 – количество теплоты, введенной в процесс с обрабатываемым материалом; Q2 – количество теплоты, подведенной теплоносителем; Q3 – тепловой эффект физических или химических превращений (если тепло поглощается, то перед Q3 ставим знак минус).
На основании теплового баланса находят расход водяного пара и других теплоносителей, а по данным энергетического баланса определяют общий расход энергии на осуществление процесса.
Четвертая задача. Установление оптимальных режимов работы аппаратов и установление их основных размеров.
При определении основных размеров площадь поперечного сечения непрерывно действующего аппарата находится из соотношения
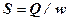 ,(1.1)
,(1.1)
где Q – объем среды, протекающей через аппарат в единицу времени, м3/c;
w – линейная скорость среды (заданная или принятая), м/c.
По величине S определяется один из основных размеров аппарата, например, для аппарата цилиндрической формы – его диаметр.
Рабочий объем периодически действующего аппарата вычисляют по формуле:
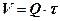 , (1.2)
, (1.2)
где Q – заданная производительность, м3/с; τ – период процесса, включающий его продолжительность, а также время, затрачиваемое на загрузку, выгрузку и другие вспомогательные операции, сек.
 2014-02-13
2014-02-13 3345
3345
