В качестве примеров химических реакций (ХР) можно привести следующие ХР:
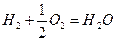 - ХР сгорания водорода;
- ХР сгорания водорода;
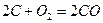 - ХР сгорания углерода;
- ХР сгорания углерода;
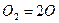 - ХР диссоциации кислорода;
- ХР диссоциации кислорода;
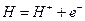 - - ХР ионизации водорода;
- - ХР ионизации водорода;
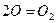 - ХР рекомбинации кислорода;
- ХР рекомбинации кислорода;
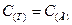 - ХР сублимации углерода;
- ХР сублимации углерода;
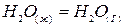 - ХР испарения воды;
- ХР испарения воды;
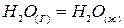 - ХР конденсации водяного пара,
- ХР конденсации водяного пара,
где (Т) – твердое вещество; (ж) – жидкое вещество; (Г) – газообразное вещество. Обозначение (Г) обычно отпускается, т.к. большинство рассматриваемых реагентов является газообразными веществами.
При химических реакциях вещества реагируют друг с другом в строго определенных отношениях, характеризуемых стехиометрическими коэффициентами компонентов реакции - 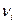 , где i =1, 2, 3,… и т.д.
, где i =1, 2, 3,… и т.д.
Первая форма записи уравнения произвольной ХР:
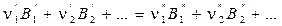
или 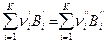 ,
,
где 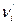 - стехиометрический коэффициент i -го исходного вещества;
- стехиометрический коэффициент i -го исходного вещества; 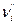 - стехиометрический коэффициент i -го продукта реакции;
- стехиометрический коэффициент i -го продукта реакции; 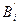 - символ i -го исходного вещества;
- символ i -го исходного вещества; 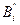 - символ i -го продукта реакции.
- символ i -го продукта реакции.
Вторая форма записи уравнения произвольной ХР может быть получена если все слагаемые уравнения ХР перенести в сторону продуктов ХР:
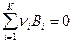 ,
,
где 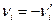 и
и 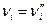 , т.е. стехиометрические коэффициенты левой части уравнения ХР считаются отрицательными, т.к. они убывают в ходе прямой ХР, а коэффициенты правой части уравнения ХР считаются положительными. В этой форме записи уравнение ХР может быть представлена в виде:
, т.е. стехиометрические коэффициенты левой части уравнения ХР считаются отрицательными, т.к. они убывают в ходе прямой ХР, а коэффициенты правой части уравнения ХР считаются положительными. В этой форме записи уравнение ХР может быть представлена в виде:
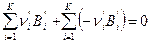
Например, для ХР сгорания водорода:
2Н2 + О2=2Н2О,
имеем для первой формы записи уравнения ХР:
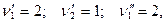
и для второй формы записи уравнения ХР:
2Н2О – 2Н2 – О2 =0
имеем: 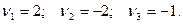
При подсчете чисел молей принято не принимать во внимание жидкие и твердые тела.
Например, для ХР:
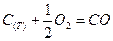 , имеем
, имеем 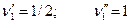 .
.
 2015-01-21
2015-01-21 1124
1124








