Al3+, Sn2+, Cr3+, Zn2+
В состав четвертой аналитической группы входят катионы р-элементов главной подгруппы III и IV групп (Al3+, Sn2+) и d-элементов побочных подгрупп II и VI групп (Zn2+, Сr3+) периодической системы Д. И. Менделеева. Их электронные формулы, радиусы (нм) и ионные потенциалы:
| Al3+ | 2s22p6 | 0,057 | 0,525 | Cr3+ | 3s23p63d3 | 0,063 | 0,470 |
| Sn2+ | 4s24p64d105s2 | 0,104 | 0,192 | Zn2+ | 3s23p63d10 | 0,083 | 0,243 |
Высокая поляризующая способность ионов обусловлена значительной величиной ионного потенциала (Al3+, Сr3+) и строением внешнего электронного слоя (18 и 18+2 электрона) – Zn2+ и Sn2+ и определяет появление малорастворимых соединений (гидроксиды, фосфаты и др.) и разнообразие химических свойств (таблица 4). Для них характерны реакции осаждения, комплексообразования, окисления-восстановления. Ионы олова (II) и хрома (III) являются восстановителями (E° Sn4+/Sn2+ = – 0,14 В, Е° СrO 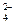 /Cr(OH)3 = – 0,13 В). Водные растворы солей всех катионов, кроме Сr3+, бесцветны. Катион хрома (III) имеет недостроенный d-подуровень, растворы его солей окрашены в сине-фиолетовый цвет.
/Cr(OH)3 = – 0,13 В). Водные растворы солей всех катионов, кроме Сr3+, бесцветны. Катион хрома (III) имеет недостроенный d-подуровень, растворы его солей окрашены в сине-фиолетовый цвет.
Таблица 4
 2015-01-30
2015-01-30 2561
2561








