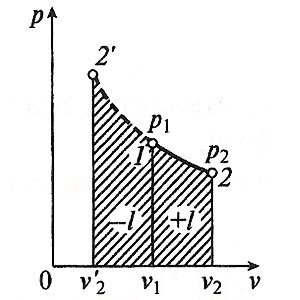
Адиабатный процесс в p, v-, T, s- и i, s-координатах (диаграммах)
Адиабатным называется процесс изменения состояния газа, который происзодит без теплообмена с окружающей средой. Так как d q = 0, то уравнение первого закона термодинамики для адиабатного процесса будет иметь вид:
d u + p d v = 0
или
Δ u + l = 0,
следовательно
Δ u = - l.
В адиабатном процессе работа расширения совершается только за счет расходования внутренней энергии газа, а при сжатии, происходящем за счет действия внешних сил, вся совершаемая ими работа идет на увеличение внутренней энергии газа.
Обозначим теплоемкость в адиабатном процессе через c ад, и условие d q = 0 выразим следующим образом:
d q = c адd T = 0.
Это условие говорит о том, что теплоемкость в адиабатном процессе равна нулю (c ад = 0).
Известно, что
сp/cv = k
и уравнение кривой адиабатного процесса (адиабаты) в p, v -диаграмме имеет вид:
pvk = const.
В этом выражении k носит название показателя адиабаты (так же ее называют коэффициентом Пуассона).
Значения показателя адиабаты k для некоторых газов:
k воздуха = 1,4
k перегретого пара = 1,3
k выхлопных газов ДВС = 1,33
k насыщенного влажного пара = 1,135
Из предыдущих формул следует:
l = — Δ u = cv (T1 – T2);
i1 – i2 = cp (T1 – T2).
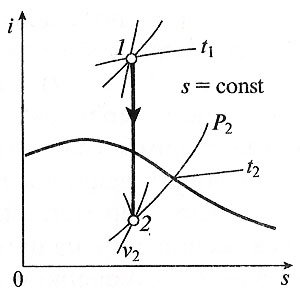
Техническая работа адиабатного процесса (l техн) равна разности энтальпий начала и конца процесса (i1 – i2).
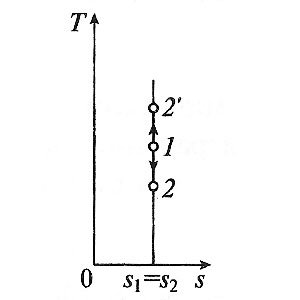
Адиабатный процесс, происходящий без внутреннего трения в рабочем теле, называется изоэнтропийным. В T, s -диаграмме он изображается вертикальной линией.
Обычно реальные адиабатные процессы протекают при наличии внутреннего трения в рабочем теле, в результате чего всегда выделяется теплота, которая сообщается самому рабочему телу. В таком случае d s > 0, и процесс называется реальным адиабатным процессом.
 2015-01-30
2015-01-30 4299
4299
