В своих опытах Резерфорд пропускал пучок альфа-частиц сквозь тонкую золотую фольгу. Золото было выбрано за пластичность, которая позволила создать очень тонкую фольгу, толщиной едва ли не в один слой молекул. За фольгой располагался специальный экран, подсвечивавшийся при бомбардировке попадающими на него альфа частицами. По теории Томсона альфа-частицы должны были беспрепятственно проходить сквозь фольгу, совсем немного отклоняясь в стороны. Однако, оказалось, что часть частиц так и вела себя, а совсем небольшая часть отскакивала назад, как будто ударившись во что-то.
То есть было установлено, что внутри атома существует нечто твердое и небольшое, от чего и отскакивали альфа-частицы. Тогда-то Резерфорд и предложил планетарную модель строения атома. Планетарная модель атома по Резерфорду объясняла результаты проведения как его экспериментов, так и опытов его коллег. До сего дня не предложено лучшей модели, хотя некоторые аспекты этой теории все равно не согласуются с практикой в некоторых очень узких областях науки. Но в основном, планетарная модель атома самая пригодная из всех. В чем же состоит эта модель?
Планетарная модель строения атома
Как следует из названия, атом сравнивается с планетой. В данном случае планету представляет из себя ядро атома. А вокруг ядра на довольно большом расстоянии вращаются электроны, как и вокруг планеты вращаются спутники. Только скорость вращения электронов в сотни тысяч раз превосходит скорость вращения самого быстрого спутника. Поэтому при своем вращении электрон создает как бы облако над поверхностью ядра. И существующие заряды электронов отталкивают такие же заряды, образованные другими электронами вокруг других ядер. Поэтому атомы не «слипаются», а располагаются на некотором расстоянии друг от друга.
И когда мы говорим о столкновении частиц, имеется в виду, что они подходят друг к другу на достаточно большое расстояние и отталкиваютсяполями своих зарядов. Непосредственного контакта не происходит. Частицы в веществе вообще расположены очень далеко друг от друга. Если бы каким-либо способом удалось схлопнуть вместе частицы какого-либо тела, оно бы уменьшилось в миллиарды раз. Земля стала бы меньше яблока размером. Так что основной объем любого вещества, как ни странно это звучит, занимает пустота, в которой расположены заряженные частицы, удерживающиеся на расстоянии электронными силами взаимодействия.
31. Атомные спектры. Сериальные ф-лы. Исследования спектров излучения разреженных газов (т.е. спектров излучения отдельных атомов) показали, что каждому газу присущ вполне определенный линейчатый спектр, состоящий из отдельных спектральных линий или групп близко расположенных линий. Самым изученным явл-ся спектр наиболее простого атома – атома водорода. Бальмер (1825-1898) подобрал эмпирическую ф-лу описывающую все известные в то время спектральные линии атома водорода и видимой области спектра: 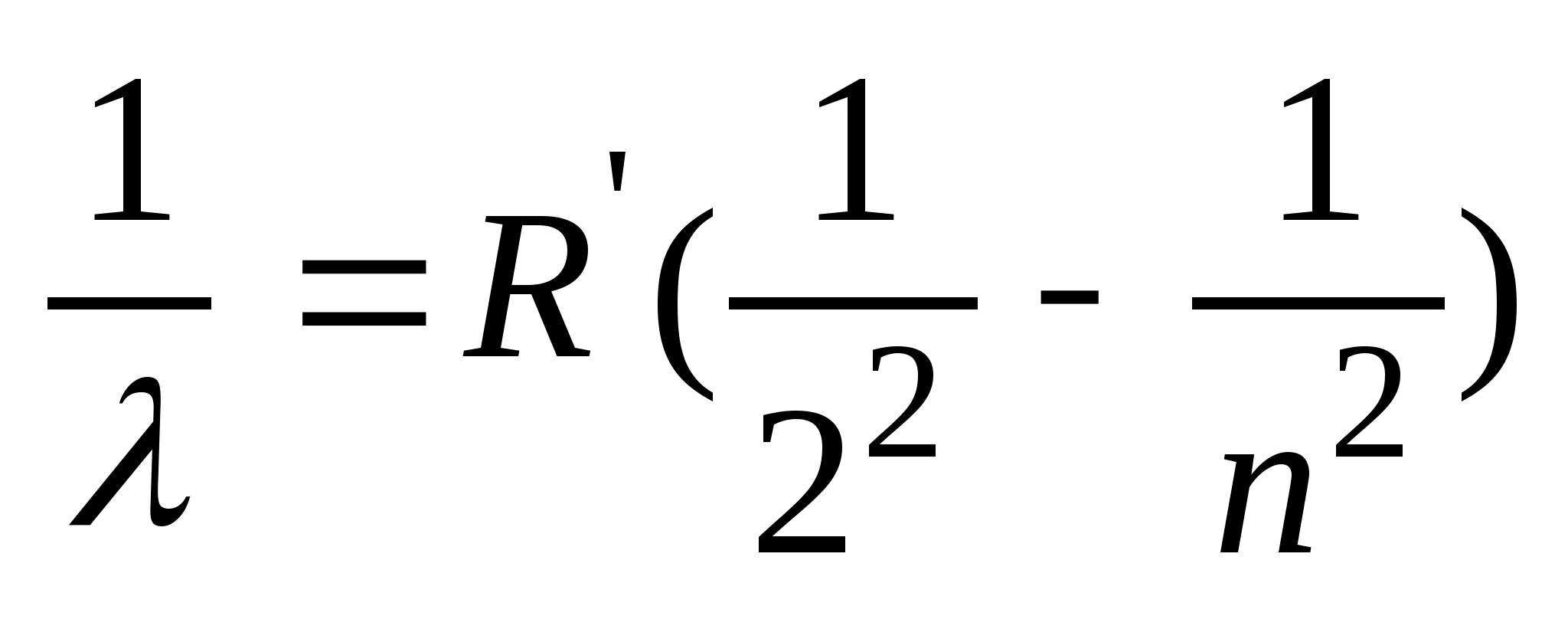 ,(n = 3, 4, …) где
,(n = 3, 4, …) где 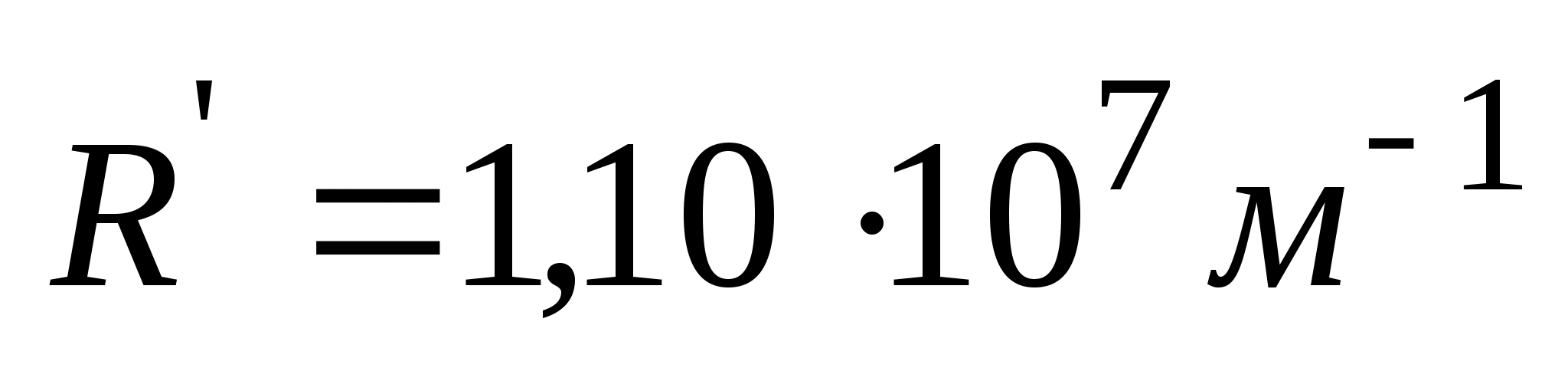 -- постоянная Ридберга. Так как
-- постоянная Ридберга. Так как 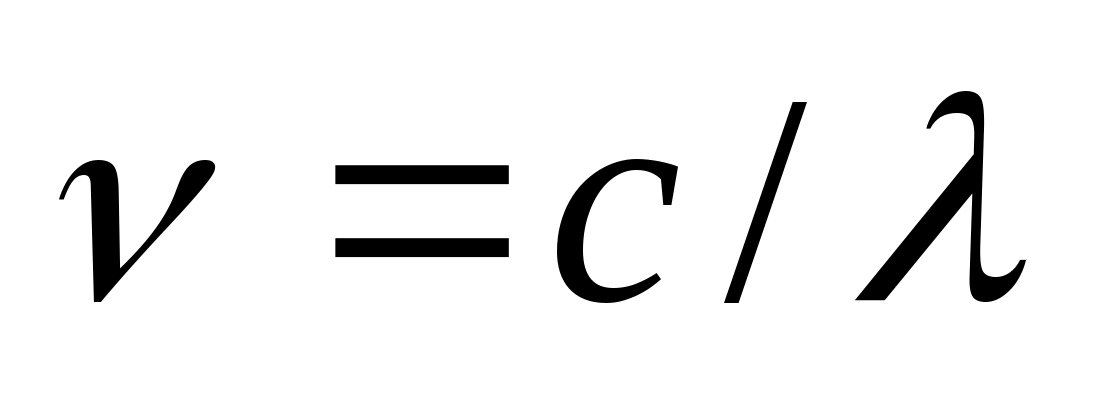 , то ф-ла может быть переписана для частот:
, то ф-ла может быть переписана для частот: 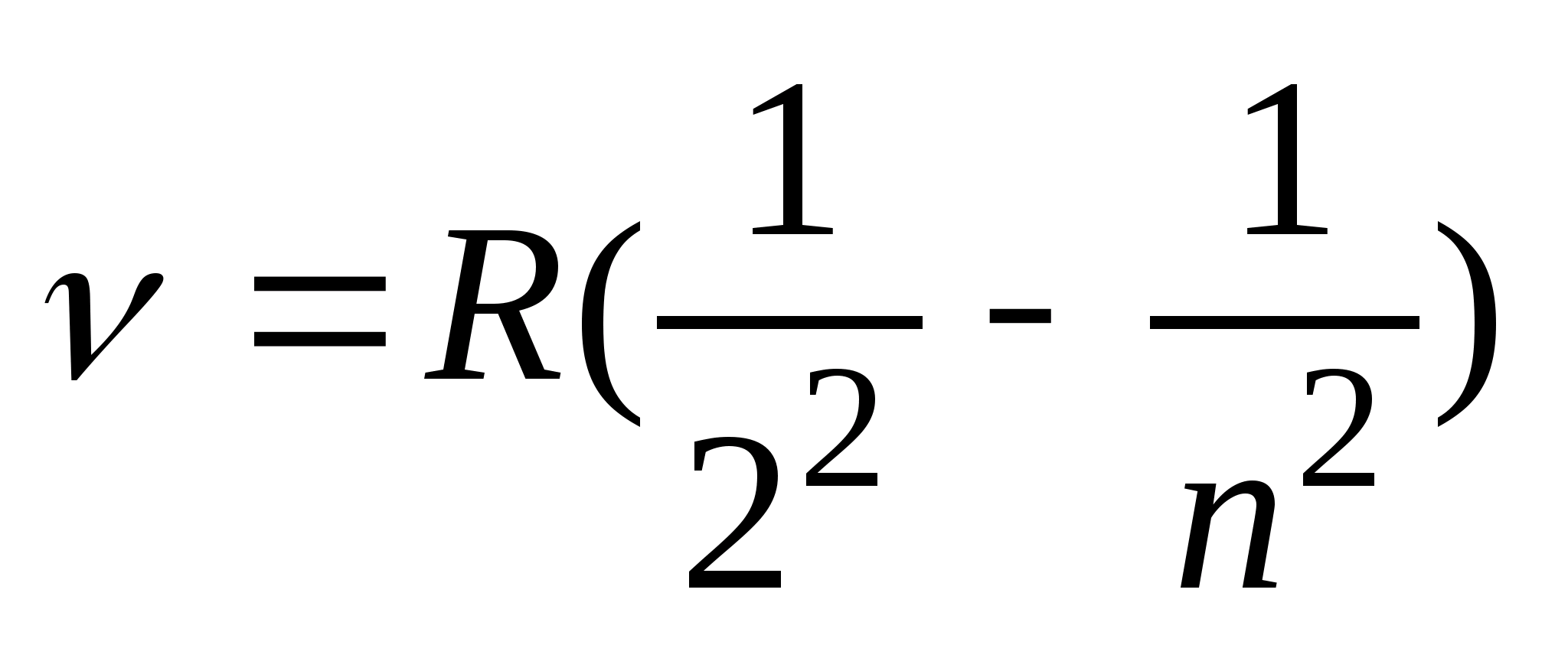 , (n = 3, 4, …), где
, (n = 3, 4, …), где 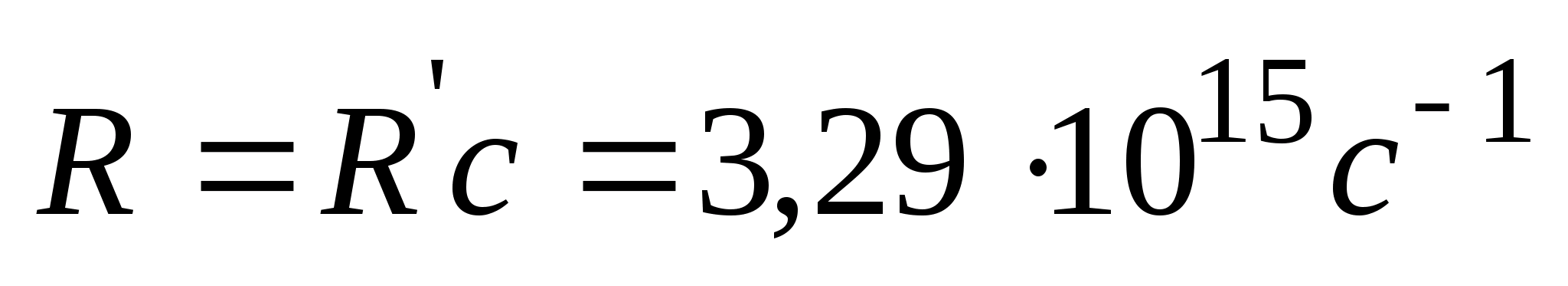 -- так же постоянная Ридберга. Из полученных выражений вытекает, что спектральные линии отличающиеся различными значениями n, образуют группу или серию линий, называемую серией Бальмера. С увеличением n линии серии сближаются; значение n =
-- так же постоянная Ридберга. Из полученных выражений вытекает, что спектральные линии отличающиеся различными значениями n, образуют группу или серию линий, называемую серией Бальмера. С увеличением n линии серии сближаются; значение n = 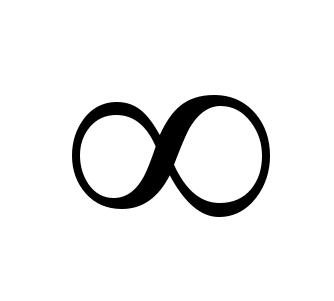 определяет границу серии, к которой со стороны больших частот примыкает сплошной спектр. В дальнейшем в спектре атома водорода было обнаружено еще несколько серий. В ультрафиолетовой области спектра находится серия Лаймана:
определяет границу серии, к которой со стороны больших частот примыкает сплошной спектр. В дальнейшем в спектре атома водорода было обнаружено еще несколько серий. В ультрафиолетовой области спектра находится серия Лаймана: 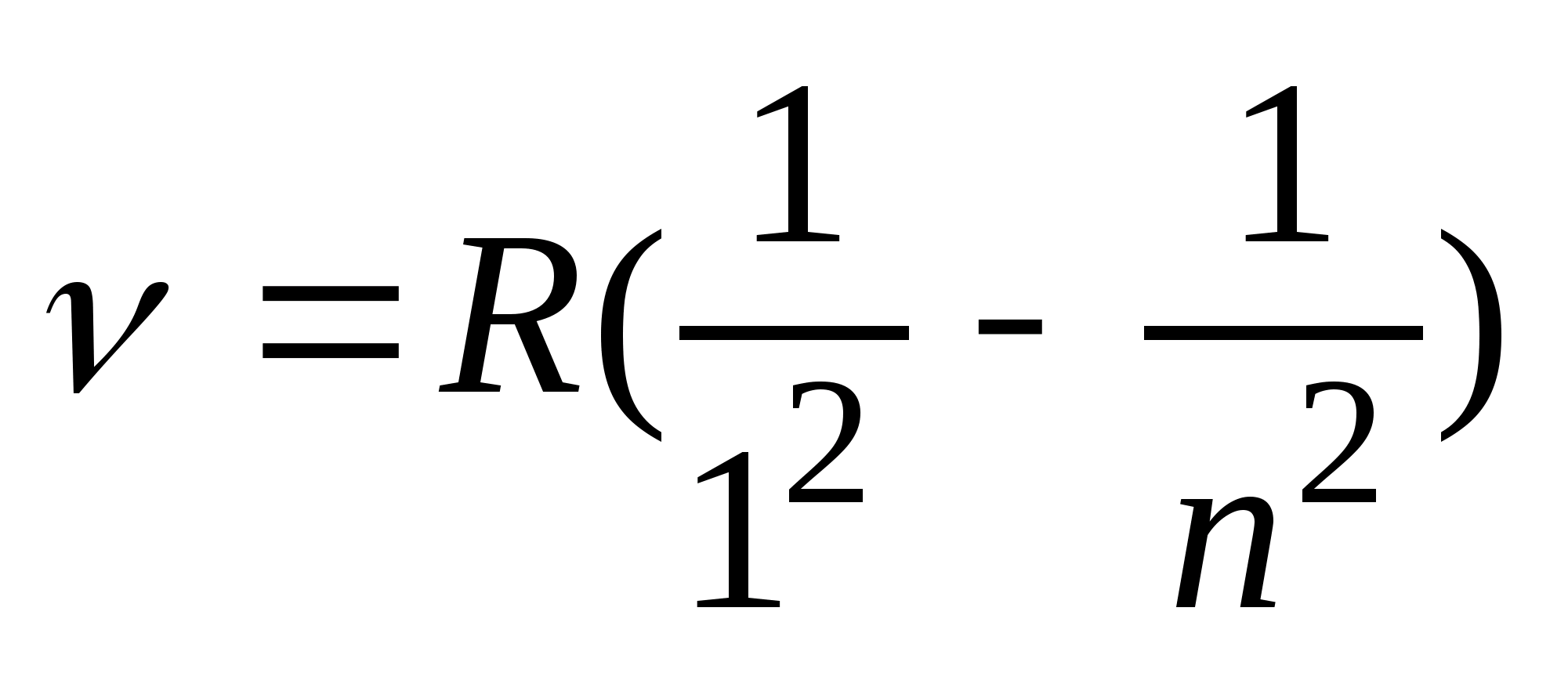 , (n = 2, 3, 4, …). В инфракрасной области были обнаружены: серия Пашена:
, (n = 2, 3, 4, …). В инфракрасной области были обнаружены: серия Пашена: 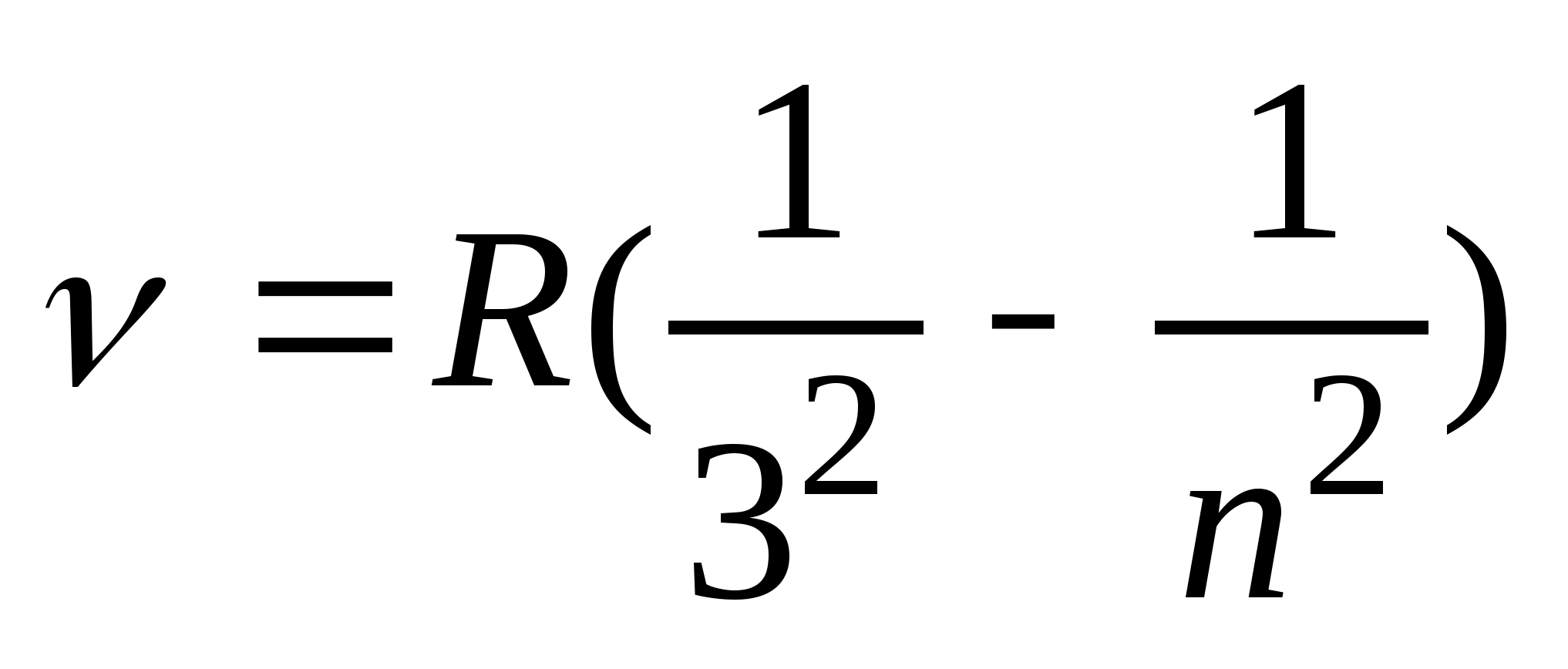 , (n = 4, 5, 6, …), серия Брэкета:
, (n = 4, 5, 6, …), серия Брэкета: 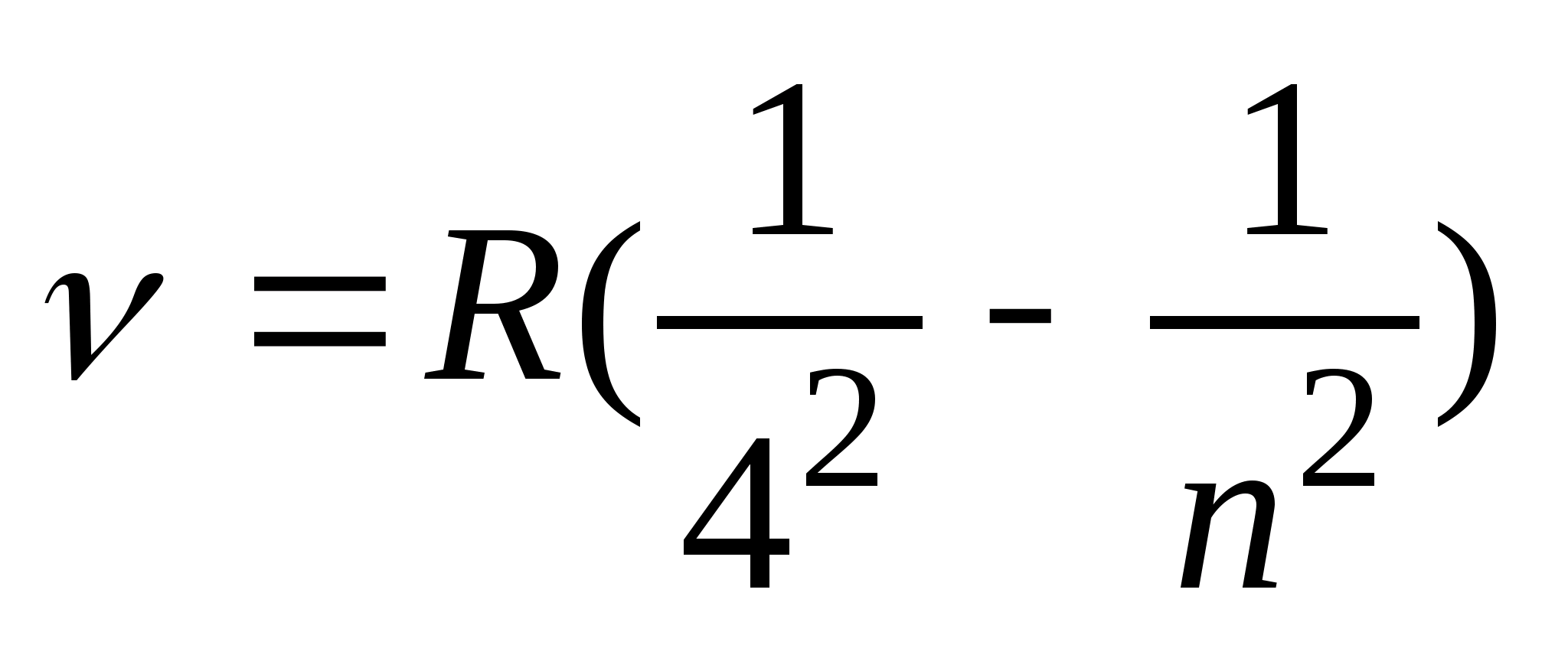 , (n = 5, 6, 7, …), серия Пфунда:
, (n = 5, 6, 7, …), серия Пфунда: 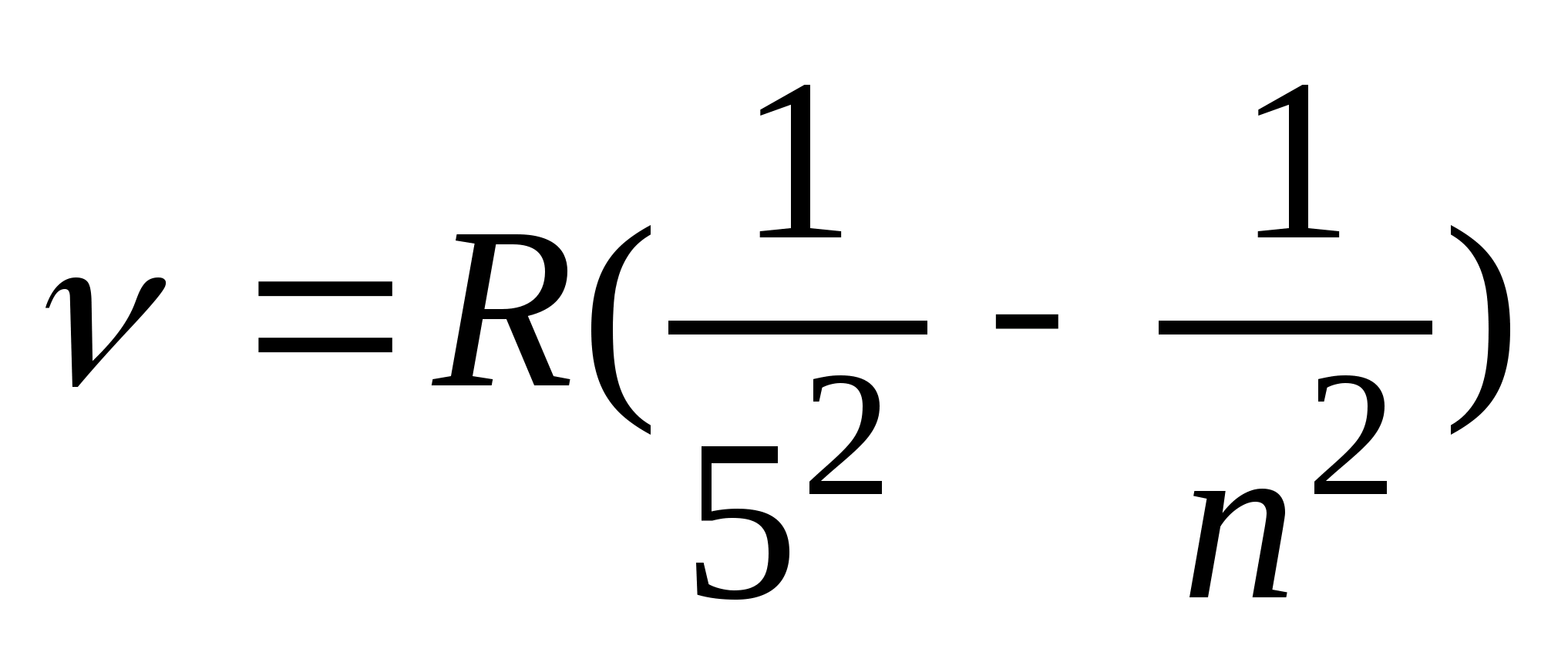 , (n = 6, 7, 8, …), серия Хэмфи:
, (n = 6, 7, 8, …), серия Хэмфи: 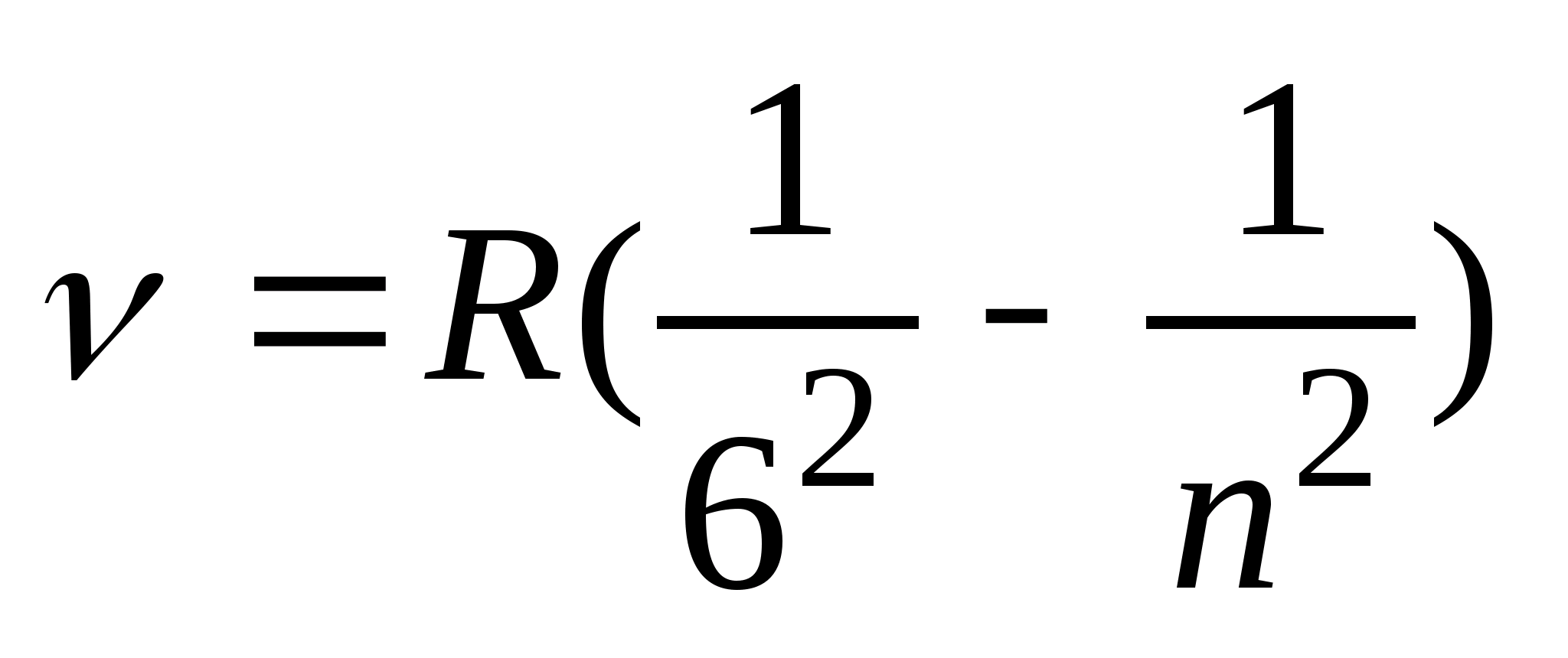 , (n = 7, 8, 9, …).
, (n = 7, 8, 9, …).
Все приведенные выше серии в спектре атома водорода могут быть описаны одной ф-лой, называемой обобщенной ф-лой Бальмера: 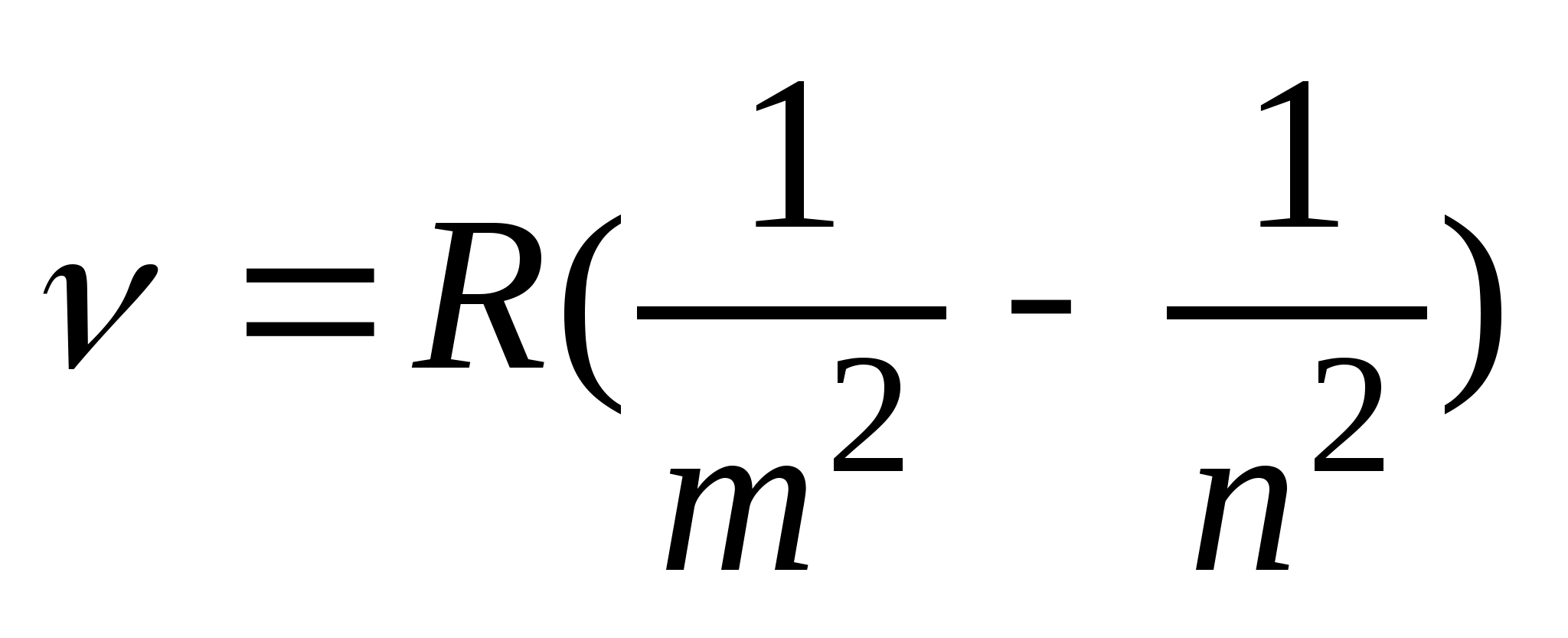 , где m – имеет в каждой данной серии постоянное значение, m = 1, 2, 3, 4, 5, 6 (определяет серию), n – принимает целочисленные значения, начиная с m+1 (определяет отдельные линии этой серии).
, где m – имеет в каждой данной серии постоянное значение, m = 1, 2, 3, 4, 5, 6 (определяет серию), n – принимает целочисленные значения, начиная с m+1 (определяет отдельные линии этой серии).
32. Постулаты Бора. Первая попытка построить качественно новую – квантовую -- теорию атома была предпринята Бором. Он поставил перед собой цель связать в единое целое эмпирические закономерности линейчатых спектров, ядерную модель атома Резерфорда (Согласно этой модели, вокруг положительного ядра, имеющего заряд Ze (Z – порядковый номер эл-та в системе Менделеева, е -- элементарный заряд), размер 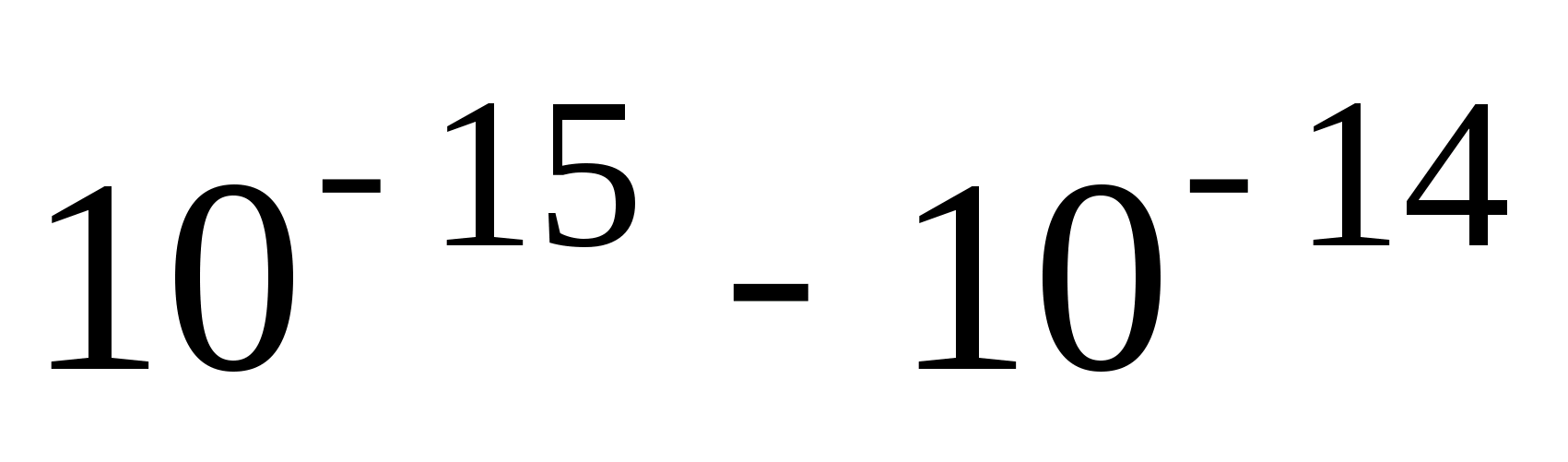 м и массу, практически равную массе атома, в области с линейными размерами порядка
м и массу, практически равную массе атома, в области с линейными размерами порядка 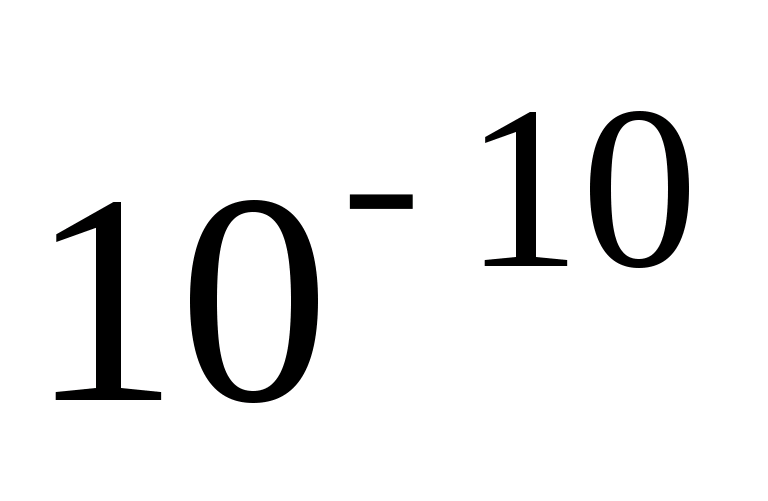 м по замкнутым орбитам движутся электроны, образую электронную оболочку атома. Так как атомы нейтральны, то заряд ядра равен суммарному заряду электронов, т.е. вокруг ядра должно вращаться Z электронов) и квантовый характер излучения и поглощения света. Два постулата: Первый постулат Бора (постулат стационарных состояний): в атоме существуют стационарные состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн. В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные квантовые значения момента импульса, удовлетворяющие условию
м по замкнутым орбитам движутся электроны, образую электронную оболочку атома. Так как атомы нейтральны, то заряд ядра равен суммарному заряду электронов, т.е. вокруг ядра должно вращаться Z электронов) и квантовый характер излучения и поглощения света. Два постулата: Первый постулат Бора (постулат стационарных состояний): в атоме существуют стационарные состояния, в которых он не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, по которым движутся электроны. Движение электронов по стационарным орбитам не сопровождается излучением электромагнитных волн. В стационарном состоянии атома электрон, двигаясь по круговой орбите, должен иметь дискретные квантовые значения момента импульса, удовлетворяющие условию 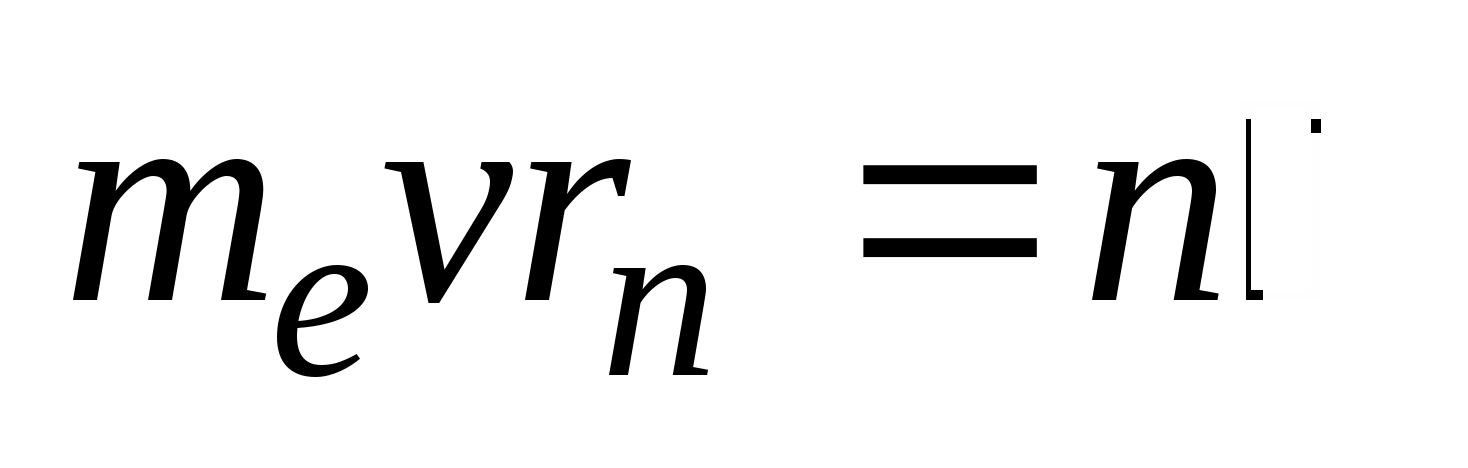 (n=1,2,3,…), где
(n=1,2,3,…), где 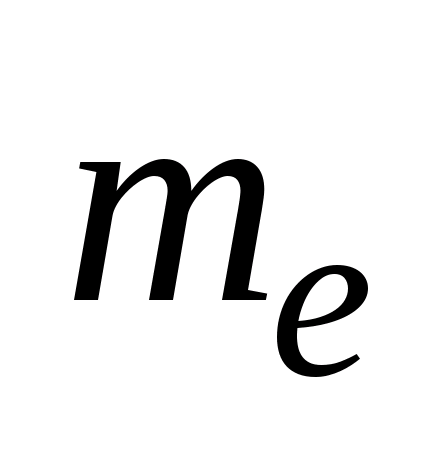 -- масса эл-трона, v – его скорость по n-ой орбите радиуса
-- масса эл-трона, v – его скорость по n-ой орбите радиуса 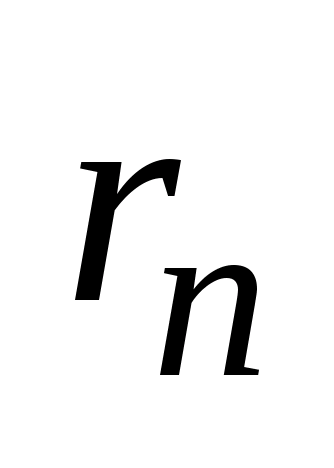 ,
, 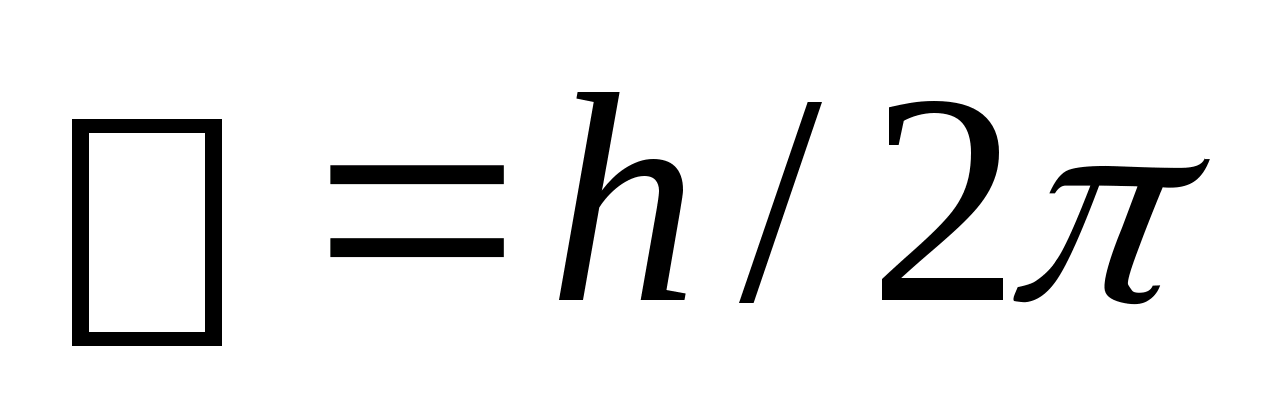 . Второй постулат (правило частот): при переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией
. Второй постулат (правило частот): при переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией 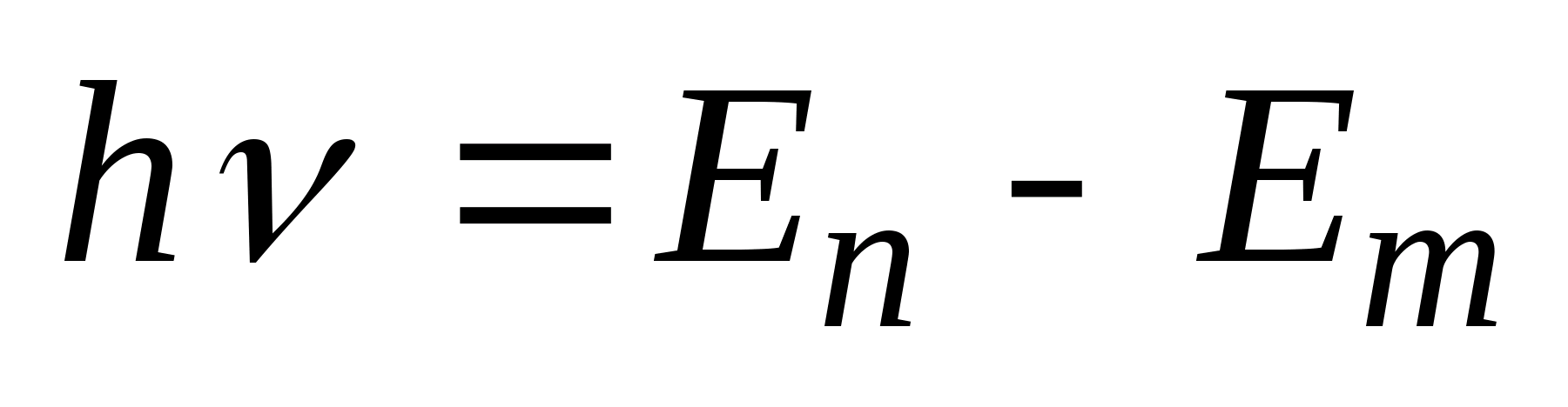 , равной разности энергий соответствующих стационарных состояний (
, равной разности энергий соответствующих стационарных состояний (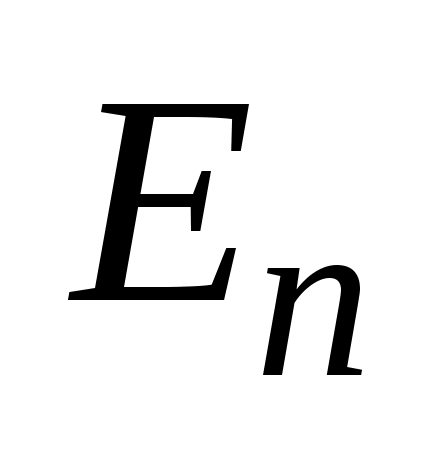 и
и 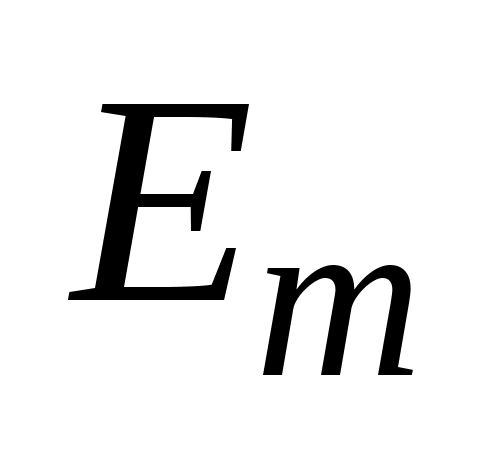 -- соответственно энергии стационарных состояний атома до и после излучения (поглощения)). При
-- соответственно энергии стационарных состояний атома до и после излучения (поглощения)). При 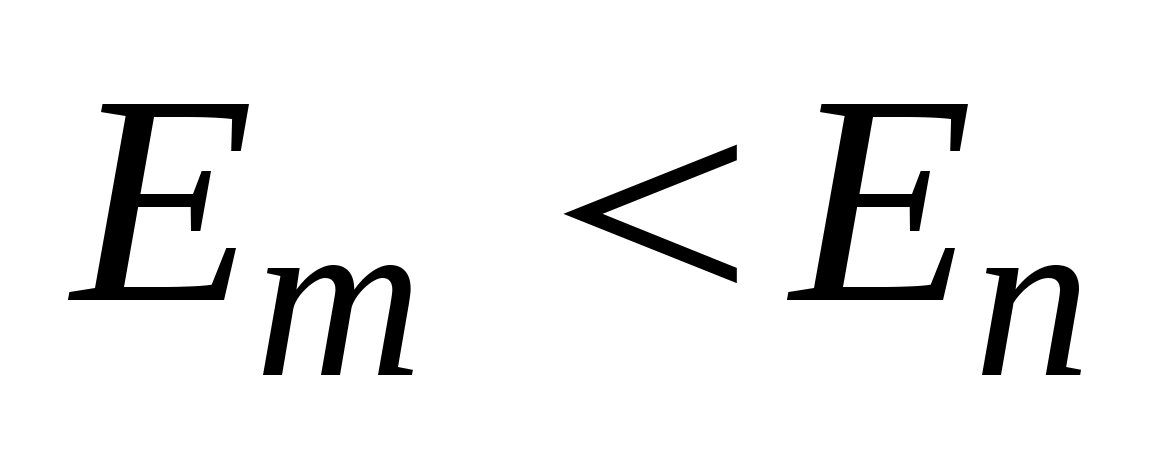 происходит излучение фотона (переход атома из состояния с большей энергией в состояние с меньшей, т.е. переход электрона с более удаленной от ядра орбиты на близлежащую), при
происходит излучение фотона (переход атома из состояния с большей энергией в состояние с меньшей, т.е. переход электрона с более удаленной от ядра орбиты на близлежащую), при 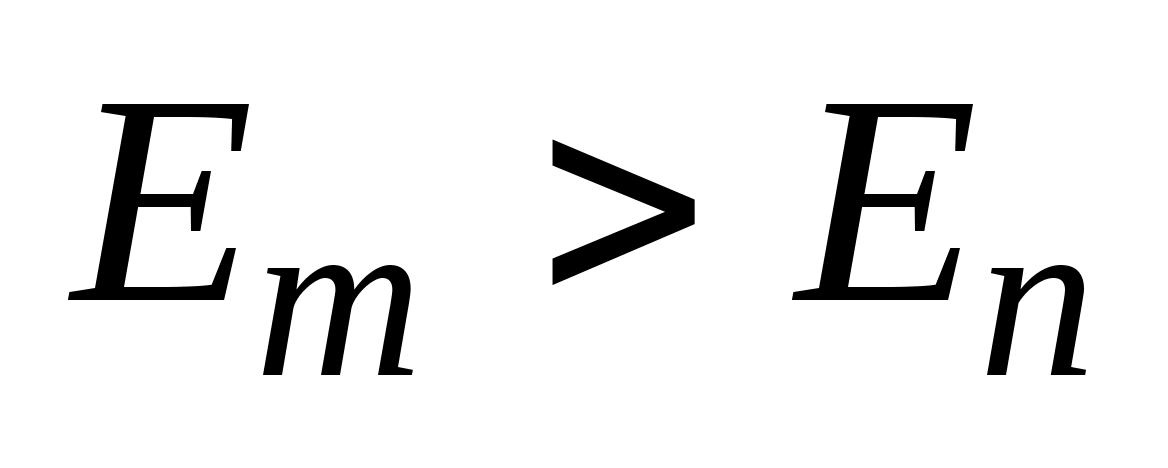 -- его поглощение (переход атома в состояние с большей энергией, т.е. переход электрона на более удаленную от ядра орбиту). Набор всевозможных дискретных частот
-- его поглощение (переход атома в состояние с большей энергией, т.е. переход электрона на более удаленную от ядра орбиту). Набор всевозможных дискретных частот 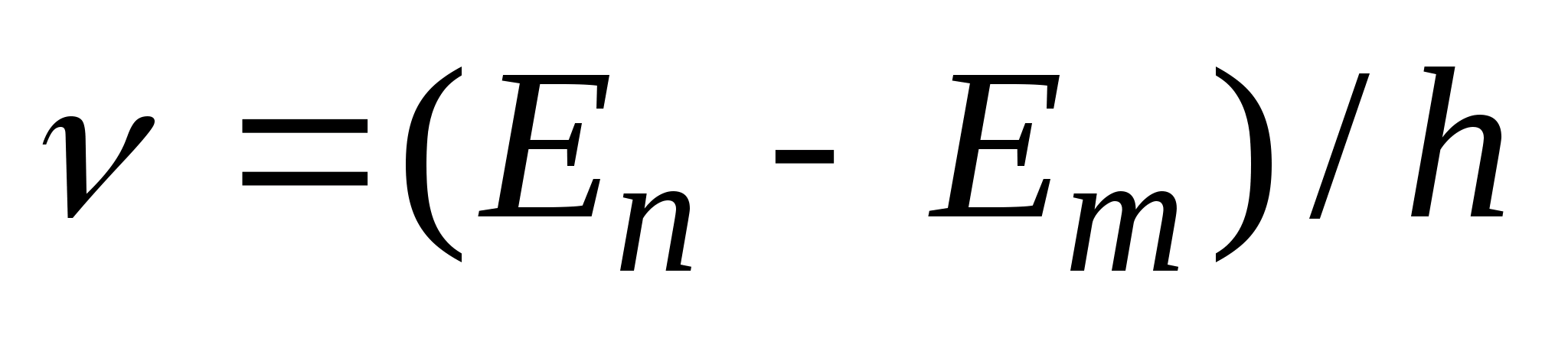 квантовых переходов и определяет линейчатый спектр атома.
квантовых переходов и определяет линейчатый спектр атома.
Опыт Франка Герца. Изучая методом задерживающего потенциала столкновения электронов с атомами газов, экспериментально было доказано, что значения энергии атомов дискретны.
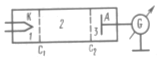
Принципиальная схема их установки приведена на рис. Вакуумная трубка, заполненная парами ртути (давление приблизительно равно 13 Па), содержала катод (К), две сетки (С1 и С2) и анод (А). Электроны, эмитируемые катодом, ускорялись разностью потенциалов, приложенной между катодом и сеткой С1. Между сеткой С2 и анодом приложен небольшой (примерно 0.5 В) задерживающий потенциал. Электроны, ускоренные в области 1, попадают в область 2 между сетками, где испытывают соударения с атомами паров ртути. Электроны, которые после соударений имеют достаточную энергию для преодоления задерживающего потенциала в области 3, достигают анода. При неупругих соударениях электронов с атомами ртути последние могут возбуждаться. Согласно боровской теории, каждый из атомов ртути может получить лишь вполне определенную энергию, переходя при этом в одно из возбужденных состояний.
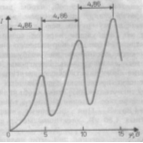
Поэтому, если в атомах действительно сущ-вуют стационарные состояния, то электроны, сталкиваясь с атомами ртути, должны терять энергию дискретно, определенными порциями, равными разности энергий соответствующих стационарных состояний атома. Из опыта следует, что при увеличении ускоряющего потенциала вплоть до 5 В анодный ток возрастает монотонно, его значение проходит через максимум, затем резко уменьшается и возрастает вновь.
33. Бо́ровская моде́ль а́тома (Моде́ль Бо́ра) — полуклассическая модель атома, предложенная Нильсом Бором в 1913 г. За основу он взял планетарную модель атома, выдвинутую Резерфордом. Однако, с точки зрения классической электродинамики, электрон в модели Резерфорда, двигаясь вокруг ядра, должен был бы излучатьэнергию непрерывно и очень быстро и, потеряв её, упасть на ядро. Чтобы преодолеть эту проблему, Бор ввёл допущение, суть которого заключается в том, что электроны в атоме могут двигаться только по определённым (стационарным) орбитам, находясь на которых они не излучают, а излучение или поглощение происходит только в момент перехода с одной орбиты на другую. Причём, стационарными являются лишь те орбиты, при движении по которым момент количества движения электрона равен целому числу постоянных Планка[1]: 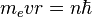 .
.
Используя это допущение и законы классической механики, а именно равенство силы притяжения электрона со стороны ядра и центробежной силы, действующей на вращающийся электрон, он получил следующие значения для радиуса стационарной орбиты 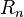 и энергии
и энергии 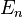 находящегося на этой орбите электрона:
находящегося на этой орбите электрона:
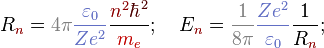
Здесь 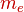 — масса электрона,
— масса электрона, 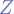 — количество протонов в ядре,
— количество протонов в ядре, 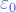 — электрическая постоянная,
— электрическая постоянная,  — заряд электрона.
— заряд электрона.
Именно такое выражение для энергии можно получить, применяя уравнение Шрёдингера, решая задачу о движении электрона в центральном кулоновском поле.
Радиус первой орбиты в атоме водорода R0=5,2917720859(36)·10−11 м[2], ныне называется боровским радиусом, либо атомной единицей длины и широко используется в современной физике. Энергия первой орбиты 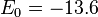 эВ представляет собой энергию ионизации атома водорода.
эВ представляет собой энергию ионизации атома водорода.
 2015-01-30
2015-01-30 2540
2540
