Еще в античные времена возникла идея о том, что Вселенная состоит из маленьких неделимых частиц — атомов. Это представление о строении вещества сохранилось до конца XIX столетия, когда к началу XX века достоверно было установлено, что в состав каждого атома входят электроны. Приоритет в открытии электрона принадлежит английскому физику Дж. Томсону. Вместе с тем тогда же было известно, что атом электрически нейтрален. Следовательно, отрицательный заряд электронов должен компенсироваться положительным зарядом неизвестных частиц, входящих в заряд атома.
В 90-х годах XIX века получила широкое распространение модель атома Дж. Томсона в виде однородной, положительной сферической среды, в которой, как изюминки в булке, рассредоточены отрицательно заряженные электроны. Атомная модель Дж. Томсона подобна кексу. Однако вскоре автор «кексовой» модели высказал предположение о нестатическом положении электронов в атоме.
Наиболее реальной представлялась ядерная или планетарная модель атома Э. Резерфорда, предложенная английским физиком в 1911г. Планетарная модель явилась результатом выполненных Э. Резерфордом и его сотрудниками экспериментов по рассеянию α-частиц. Опыты состояли в следующем. Пучок положительно заряженных α-частиц направляется на тонкий, в виде фольги, золотой лист. За фольгой находился экран, покрытый сцинтиллятором — веществом, которое испускает свет в той точке, в которую ударялась α-частица. Исходя из модели Дж. Томсона, следовало ожидать, что α-частицы не будут отклоняться на большие углы, так как электроны гораздо легче α-частиц. И, действительно, опыты показали, что большинство α-частиц свободно проходили сквозь лист фольги, как если бы он представлял собой в основном пустое пространство. И все же часть α-частиц отклонялась на небольшие углы, что являлось, как можно было предположить, следствием взаимодействия с положительным зарядом атома. Но неожиданным и ошеломляющим оказалось то, что небольшое количество α-частиц рассеивалось на большие углы, достигающие 180°. Такое могло происходить только в том случае, если положительно заряженные α-частицы испытали отталкивание массивного положительного заряда, сконцентрированного в малой области пространства.
По модели Э. Резерфорда атом состоит из массивного, положительно заряженного ядра, в котором сосредоточено 99,94 % массы атома. Величина положительного заряда оценивается произведением ze, где z — порядковый атомный номер химического элемента в таблице Д. Менделеева; е — элементарный заряд. Вокруг ядра внутри сферы с наружным диаметром ~10-10 м по замкнутым эллиптическим орбитам вращается z электронов, образуя электронную оболочку атома. Электроны не могут покоиться в атоме, так как в этом случае они упали бы на ядро под действием кулоновского притяжения. По оценкам Э. Резерфорда, размеры ядра должны быть порядка 10-15—10-14 м. Сравнивая размеры ядра и атома, приходим к выводу о том, что электроны должны находиться от ядра на расстоянии в (10—100) • 103 больше, чем размер ядра. И отсюда второй вывод: основную часть атома составляет пустое пространство.
Недостаток модели Э. Резерфорда состоит в невозможности объяснить факт исключительной устойчивости атома: во-первых, при столкновениях с другими атомами; во-вторых, по законам классической физики вращение электронов вокруг ядра не может быть устойчивым, так как оно должно сопровождаться электромагнитным излучением, как всякое ускоренное движение заряженных частиц. А по законам классической физики электроны, двигаясь по окружности, обладают центростремительным ускорением. Центростремительная, сила, удерживающая электрон на орбите радиусом г, представляет кулоновскую силу притяжения электрона к ядру:
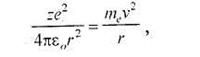
где εо = 8,85 • 10-12 Ф/м — электрическая постоянная; mе — масса электрона, кг; v — скорость электрона на орбите, м/с. На создание электромагнитного поля расходуется энергия. Энергия электрона должна постепенно убывать, а вместе с ней и скорость вращения электрона вокруг ядра. Электрон в конце концов должен упасть на ядро. Однако атомы — достаточно устойчивые образования и могут существовать миллиарды лет. В-третьих, по модели Э. Резерфорда спектр излучения атома должен быть сплошным. Опыты же показали, что спектр излучения конкретного атома является дискретным.
 2015-05-13
2015-05-13 4520
4520
