Стадия микрофильтрации.
Микрофильтрация – это баромембранный процесс разделения, в котором мембраны не пропускают частицы и растворенные макромолекулы размером свыше 0,1 мкм. МФ присущ ситовой или экранный механизм разделения, соотношение размеров частиц и размера пор (практический, без учета гидаратации) являются величинами одного порядка. Размеры пор в микрофильтрации варьируются от 10 до 0,05мкм. В данном процессе вся толщина мембраны дает вклад в сопротивление транспорту, особенно при использовании симметричных пористых мембран. Микрофильтрация всегда протекает с образованием осадка на мембране.
Стадия ультрафильтрации.
Относительно ультрафильтрации до недавнего времени существовало мнение, что лишь соотношение размеров молекулы растворенного вещества и пор в мембране определяет, селективна (избирательна) или неселективна мембрана по отношению к данному веществу. Но при УФ на ситовой механизм накладывается явление гидратации. Для УФ мембран сопротивление локализуется в верхнем слое, а нижний слой выполняет лишь функцию подложки. Поры здесь меньшего размера, по сравнению с МФ, гидратация более выражена, на поверхности мембраны имеется заряд.
Стадия обратного осмоса.
Обратный осмос заключается в фильтровании растворов под давлением, превышающим осмотическое, через полупроницаемые мембраны, пропускающие растворитель и задерживающие молекулы либо ионы растворенных веществ. В основе описываемого метода лежит явление осмоса — самопроизвольного перехода растворителя через полупроницаемую перегородку в раствор (рис. 10.1.- а). Давление, при котором наступает равновесие (рис. 10.1.-б), называется осмотическим. Если со стороны раствора приложить давление, превышающее осмотическое (рис. 10.1.-в), то перенос растворителя будет происходить в обратном направлении, что нашло отражение в названии процесса «обратный осмос».
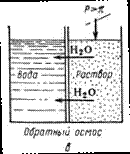
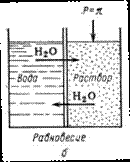
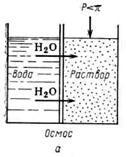
Рис. 10.1. Схема осуществления процесса обратного осмоса.
Из данной схемы следует, что движущей силой обратного осмоса является разница между приложенным гидростатическим давлением и осмотическим давлением раствора. Движущей силой процесса является разность давлений:
∆Р=Р-(п3-п2), (10.1.)
где Р – избыточное давление над исходным раствором;
п2 и п3 – осмотическое давление соответственно исходного раствора у поверхности мембраны и раствора, прошедшего через мембрану (пермеата).
Осмотические давления растворов могут достигать десятков мегапаскалей. Рабочее давление в обратноосмотических установках должно быть значительно больше, поскольку их производительность определяется движущей силой процесса — разностью между рабочим давлением и осмотическим.
Несмотря на сравнительно высокие рабочие давления, обратный осмос оказывается энергетически выгоднее большинства других массообменных процессов и даже многокорпусного выпаривания. Обратноосмотический процесс протекает без фазовых превращений, что также позволяет снизить затраты энергии на разделение до минимальной термодинамической энергии.
Многочисленными исследованиями было установлено, что эффект разделения в обратном осмосе обусловлен не простым механическим просеиванием молекул в зависимости от их размеров через поры в мембране, а может быть объяснён лишь с учетом сложных физико-химических взаимодействий между молекулами растворителя и растворённого вещества с мембраной.
Для обеспечения качественной и стабильной работы обратноосмотических мембран в течении длительного периода эксплуатации необходимо обеспечить высокий уровень предварительной очистки, т.к. образование аморфного осадка - геля на поверхности полупроницаемой мембраны резко ухудшает условия её работы.
Помимо качественной предварительной очистки необходимо своевременно проводить химическую очистку мембран, для удаления загрязнений с поверхности, образующихся в процессе эксплуатации.
 2015-01-21
2015-01-21 2059
2059








