Из закона Рауля вытекают два следствия: растворы кипят при более высоких и замерзают при более низких температурах, чем чистый растворитель. Причем величины повышения температуры кипения Δ t кип и понижения температуры замерзания Δ t зам разбавленных растворов неэлектролитов пропорциональны моляльной концентрации растворенного вещества:
| Δ t кип = Е ∙ Сm, | (7.11) | |
| Δ t зам = К ∙ Сm, | (7.12) |
где Е – эбуллиоскопическая постоянная;
К – криоскопическая постоянная;
Сm – моляльная концентрация, то есть число молей растворенного вещества на 1 кг растворителя.
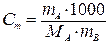 , , | (7.13) |
где mА – масса растворенного вещества, г;
МА – молярная масса растворенного вещества, г/моль;
mB – масса растворителя, г;
1000 – переводной коэффициент от граммов к килограммам.
Е и К – величины, постоянные для каждого растворителя, определяются только его природой и не зависят от свойств растворенного вещества. Физический смысл постоянных Е и К выявляется при условии, что Сm = 1 моль/кг. Тогда из (7.11) и (7.12) следует что Δ t кип = Е и Δ t зам = К. Следовательно, Е – это повышение температуры кипения, К – понижение температуры замерзания одномоляльного раствора. Для водных растворов Е = 0,52 ˚ С∙кг/моль, а К = 1,86 ˚С∙кг/моль.
Уравнения (7.11) и (7.12) можно применить для определения молярных масс веществ, подставив вместо Сm соответствующие выражения, тогда:
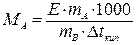 , , | (7.14) | |
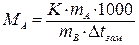 . . | (7.15) |
Пример 7. При какой температуре будет кипеть и замерзать 10 %-ный раствор уксусной кислоты (СН3СООН)?
 2015-02-27
2015-02-27 1410
1410








