Тиамина бромид количественно определяют в водной среде способом, основанным на нейтрализации гидробромида и последующим аргентометрическим титрованием суммы бромид-ионов:
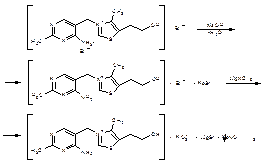
Окисление кислоты аскорбиновой иодом до дегидроаскорбиновой кислоты лежит в основе иодометрического определения. Титруют 0,1 М раствором иода без индикатора до образования стойкого желтого окрашивания или используют крахмал, который добавляют в конце титрования.

Для испытания подлинности кислоты аскорбиновой после добавления карбоната натрия в водном растворе происходит образование ионизированной формы кислоты аскорбиновой. К полученной натриевой соли прибавляют сульфат железа (II). Появляется темно-фиолетовое окрашивание, обусловленное образованием аскорбината железа, исчезающее после добавления разведенной серной кислоты:
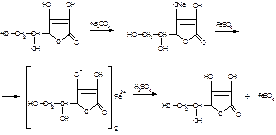
При взаимодействии кислоты аскорбиновой с раствором нитрата серебра его катион восстанавливается до металлического серебра (реакция образования «серебряного зеркала»):
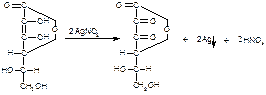
Восстановительными свойствами кислоты аскорбиновой обусловлено превращение окрашенного в синий цвет раствора 2,6-дихлорфенолиндофенола в бесцветное лейкооснование:

Аналогичную реакцию кислота аскорбиновая дает с раствором метиленового синего. Растворы иода и перманганата калия обесцвечиваются, нитраты превращаются в нитриты, арсенаты в арсениты, фосфорномолибденовая кислота образует окрашенный в синий цвет продукт реакции также вследствие проявления восстановительных свойств кислотой аскорбиновой.
Восстановление сульфата меди (II) до меди (I) происходит при прибавлении к раствору кислоты аскорбиновой растворов сульфата меди и тиоцианата аммония. При этом выпадает белый осадок тиоцианата меди (I):
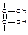 | 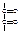 |
+ 2CuSO4 + 2NH4NCS 2CuNCS + + (NH4)2SO4 + H2SO4
Количественно по ФС определяют кислоту аскорбиновую, используя в качестве титранта-окислителя 0,1 М раствор иодата калия в присутствии иодида калия:
KIO3 + 5KI + 6HCl ¾ 3I2 + 6KCl + 3H2O
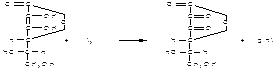
Избыток иода окрашивает крахмал в синий цвет.
Цериметрическое определение основано на том же процессе окисления кислоты аскорбиновой (в среде серной кислоты) 0,1 М раствором сульфата церия (IV), который восстанавливается до иона церия (III). Индикатором служит комплексное соединение железа (II) с о -фенантролином. Оно имеет интенсивно-красное окрашивание. В эквивалентной точке избыток сульфата церия (IV) окисляет ион железа до трехзарядного и происходит образование комплексного соединения голубого цвета:
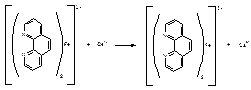
Широко применяют фотоколориметрические способы, основанные на цветных реакциях с 2,6-дихлорфенолиндофенолом, фосфорномолибденовой кислотой и другими реактивами.
Кислотные свойства кислоты аскорбиновой лежат в основе определения кислоты аскорбиновой методом кислотно-основного титрования
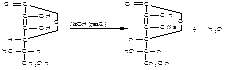
Идентифицируют тиамин по окислению в щелочной среде. Эта реакция известна под названием тиохромной пробы:
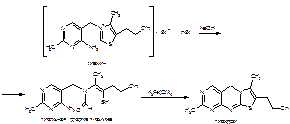
Тиохром из водных растворов извлекают бутиловым или изоамиловым спиртом. Полученные спиртовые растворы при ультрафиолетовом облучении (365 нм) имеют характерную синюю флуоресценцию, исчезающую при подкислении и вновь возникающую при подщелачивании. Реакцию образования тиохрома используют для количественного флуориметрического определения тиамина.
Тиамина бромид дает характерные реакции на бромиды по образованию свободного брома под действием хлорамина в солянокислой среде (желто-бурое окрашивание хлороформного слоя). При действии на соли тиамина реактивом Несслера появляется желтое окрашивание, которое вследствие восстановления до металлической ртути переходит в черное. При добавлении двух капель 15%-ного раствора гидроксида натрия к 0,1%-ному раствору соли тиамина появляется желтое окрашивание. При сплавлении с кристаллическими едкими щелочами тиамин разрушается с образованием сульфидов, которые легко обнаружить с помощью раствора нитропруссида натрия (красно-фиолетовое окрашивание).
Как и другие третичные амины, тиамин при нагревании на водяной бане с уксусным ангидридом и кристаллами лимонной кислоты приобретает красное окрашивание. При пиролизе тиамина вследствие наличия в его молекуле первичной аминогруппы происходит конденсация:
2R-NH2 ¾® R-NH-R + NH3
Для количественного определения тиамина бромида используют гравиметрическое определение которое состоит в нагревании смеси водного раствора навески, концентрированной хлороводородной кислоты и 10%-ного раствора кремневольфрамовой кислоты. Образовавшийся осадок отделяют, промывают на фильтре горячей разбавленной хлороводородной кислотой, затем водой и ацетоном. Все операции выполняют на предварительно высушенной до постоянной массы воронке, которую вместе с осадком сушат, охлаждают в эксикаторе и взвешивают. Масса осадка, умноженная на коэффициент 0,25, соответствует количеству тиамина бромида.
• Вопрос 4 Ф/гнозия 4. В фармакогностическом анализе лекарственное сырье стандартизуют по содержанию витаминов - аскорбиновой кислоты, каротиноидов, филлохинона (вит. K1).
• Какие методы используют для обнаружения витаминов в сырье и их количественной оценки? На каких физико-химических свойствах указанных витаминов они основаны?
• Дайте характеристику их растительным источникам. Назовите латинские названия растений, сырья, семейств, укажите химический состав и применение.
Ответ: Витамин С — кислота аскорбиновая. Водорастворим. Суточная потребность 50-100 мг. Участвует в окислительно-восстановительных реакциях, повышает сопротивляемость организма к экстремальным воздействиям. Недостаток вызывает цингу (рыхлость десен, выпадение зубов, кровоизлияния). Накапливается в плодах шиповника, черной смородины и др.
Качественное и количественное определение содержания аскорбиновой кислоты в лекарственном растительном сырье связано с использованием 2,6-дихлорфенолиндофенолята натрия. Для количественного определения навеску сырья экстрагируют горячей водой и аликвоту экстракта титруют раствором реактива (синего цвета) до неисчезающей синеватой окраски (в ходе титрования кислота аскорбиновая окисляется, а реактив восстанавливается до бесцветной формы). Для качественного определения часть водного экстракта хроматографируют на пластинках «Силуфол» или «Сорбфил», высушивают и обрабатывают указанным реактивом (нанеся одновременно раствор свидетеля — чистой аскорбиновой кислоты) — пятна кислоты аскорбиновой выглядят бесцветными на синем фоне. Сырье, содержащее аскорбиновую кислоту Fructus Rosae — плоды шиповника (Rosae fructus — шиповника плод)Собранные в период полного созревания и высушенные плоды дикорастущих и культивируемых кустарников различных видов шиповника (розы) Rosa L. из сем. розоцветных (Rosaceae); используют в качестве лекарственного средства и лекарственного сырья.В медицине используются представители:секц. Rugosae Chrshan.: шиповник морщинистый (Rosa rugosa Thunb.);секц. Cinnamomeae DC: шиповник майский (ш. коричный) — Rosa majalis Herrm. (R. cinnamomea L), ш. иглистый (R. acicularis Lindl.), ш. даурский (R. davurica Pall.), ш. Беггера (R. beg geriana Schrenk), ш. Федченко (R. fedtschenkoana Regel), ш. кокандский ( R. kokanica (Regel) Regel ex Juz.);секц. Caninae DC: ш. собачий (R. canina L.), ш. щитконосный (R. corymbif era Borkh.), ш. мелкоцветковый (R. micrantha Borrer ex Smith), ш. песколюбивый (R. psammophila Chrshan.), ш.войлочный (R. tomentosa Smith), ш. зангезурский (R. zangezura P. Jarocs) и некоторые другие виды
Химический состав. Плоды шиповника содержат кислоту аскорбиновую (от 0,2-1 % у низковитаминных видов и до 4-5 % у высоковитаминных), каротиноиды (р-каротин и др.) до 10 мг%, токоферолы (витамин Е), флавоноиды (флавонолы — рутин, кемпферол; катехины; лейкоантоцианидины; антоцианы), гидролизуемые и конденсированные дубильные вещества, органические кислоты — лимонная и яблочная (2-4 %), жирное масло, пектиновые вещества (до 14%), сахара (до 24 %), около 0,9 % свободных аминокислот (в основном аспарагиновой). Использование. Для приготовления настоев, сиропов, микстуры Траскова, витаминных и поливитаминных сборов, применяемых при гипо- и авитаминозе С и различных заболеваниях, сопровождающихся повышенной потребностью в кислоте аскорбиновой. Для получения богатых кароти-ноидами препаратов «Масло шиповника» и «Каротолин», применяемых как ранозаживляющие средства, а кроме того, для получения препарата «Холосас», содержащего органические кислоты, используемого как желчегонное средство.Входит в состав ряда БАДов. Имеется также НД на «Плоды шиповника свежие» (ТУ 64-4-26-86). Витамины К — филлохинон и др. Жирорастворимы. Участвуют в свертывании крови, индуцируя образование протромбина. Содержатся во всех растениях, но в повышенных концентрациях накапливаются только в некоторых — в листьях крапивы, траве пастушьей сумки, кукурузных рыльцах и др. Недостаток вызывает замедление свертывания крови и кровоизлияния.Витамин С, а также каротиноиды термостабильны, но в свежесобранном сырье постепенно разлагаются ферментами. Для инактивации последних (то есть ферментов) и максимального сохранения первых (витаминов) сырье следует сушить при повышенных температурах — 70-90 °С. Сырье, содержащее филлохиноны (витамины группы К)
Folia Urticae (Folia Urticae dioicae) — листья крапивы двудомной (Urticae folium —крапивы двудомной лист)Собранные во время цветения и высушенные листья дикорастущего многолетнего травянистого растения крапивы двудомной (Urtica dioica L.) из сем. крапивных (Urticaceae); используют в качестве лекарственного средства и лекарственного сырья.
Недопустимыми к заготовке видами считаются крапива жгучая и крапива коноплевая.
Крапива жгучая (U. urens L.) — сорное и рудеральное однолетнее, однодомное растение высотой 40-50 см. Листья эллиптические или яйце-видные длиной 4-5 см, с округло-клиновидным основанием.
Крапива коноплевая (U. cannabina L.) — многолетнее травянистое растение высотой 50-150 см. Листья глубоко 3-5-рассеченные с перисто-зубчатыми надрезами.
Химический состав. Листья крапивы содержат витамин К1 (200 мг%), хлорофиллы А и В, кислоту аскорбиновую (270 мг%), каротиноиды (50 мг%), флавоноиды, дубильные вещества.
Использование. Для приготовления настоя или жидкого экстракта, которые применяют в качестве кровоостанавливающего средства при маточных, легочных, печеночных, почечных и других кровотечениях. Препараты крапивы усиливают сократительную деятельность матки и повышают свертываемость крови, поэтому эффективны при климактерических кровотечениях. Листья входят в состав витаминных, желудочных и слабительных сборов и ряда БАДов.
Каротиноиды — жирорастворимые растительные пигменты желтого, оранжевого или красного цвета, предшественники витамина А (провитамины А).
Наиболее важными источниками провитамина А являются корнеплоды моркови, томаты, листовая зелень (салат, шпинат, зеленый лук, петрушка, крапива), плоды облепихи, рябины обыкновенной, цветки ноготков, смородины, шиповника, абрикоса, черники, ежевики, крыжовника, тыквы. Накоплению каротиноидов в растениях способствуют хорошее освещение, дефицит влаги, характер почв. Низкая температура и повышенная влажность снижают накопление каротиноидов.
Каротиноиды — кристаллические вещества желтого или оранжевого цвета, нерастворимые в воде, плохо — в спирте; хорошо растворимые в неполярных органических растворителях (хлороформ, петролейный эфир, бензин и др.), жирных маслах. Растворы имеют окраску от желтой до оранжевой и оранжево-красной с желтовато-зеленой флуоресценцией.
Каротиноиды в силу своей химической природы (длинная алифатическая цепочка и большое количество ненасыщенных связей) легко окисляются кислородом воздуха, разрушаются на свету. Кислая среда ускоряет окисление. Кроме того, легко разрушаются при сушке и хранении лекарственного сырья. Лекарственное сырье, содержащее каротиноиды, рекомендуется сушить непосредственно после сбора, в тепловых сушилках при температуре 60-70 °С; хранить в прохладных темных помещениях, защищенных от прямого солнечного света, по общему списку 1-2 года.
Для качественного обнаружения каротиноидов можно использовать химические реакции и хроматографию на силикагеле. Каротиноиды извлекают из сырья хлороформом и к хлороформному извлечению прибавляют кислоту серную концентрированную (синее окрашивание, переходящее в слой кислоты серной) или кислоту азотную концентрированную (синее окрашивание, переходящее в зеленое и грязно-желтое). Хромато-граммы проявляют 10 %-ным эта-нольным раствором кислоты фосфор-номолибденовой, нагревают в сушильном шкафу при температуре 60-80 °С несколько минут. На желто-зеленом фоне появляются синие пятна каротиноидов.
Для количественного определения каротиноидов в лекарственном сырье используют фотоколориметрический или спектрофотометрический методы. В качестве стандарта применяют раствор калия бихромата. Из сырья каротиноиды извлекают абсолютным спиртом, петролейным эфиром (ткип 40-70 °С). Извлечения высушивают над безводным натрия сульфатом перед определением оптической плотности.
 2015-02-27
2015-02-27 4379
4379








