Изменение энтропии сложного процесса, состоящего из нескольких стадий, равняется сумме изменений энтропий каждой отдельной стадии этого процесса:
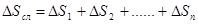 . (4.8)
. (4.8)
Например, изменение энтропии при обратимом превращении 10,0 г льда, находящегося при -10 °С, в пар при 120 °С, если
С(Н2О, ТВ) = 2,03 Дж г-1 К-1; DНпл. льда = 331,89 Дж г-1;
С(Н2О, Ж) = 4,18 Дж г-1 К-1; DНисп. Н2О = 2253,4 Дж г-1.
С(Н2О, Г) = 1,93 Дж г-1 К-1;
Вычисляют следующим образом.
Данный процесс представим из пяти стадий:
Данный процесс представим из пяти стадий:
1. Нагревание льда от -10 °С до 0 °С, Δ S 1.
2. Плавление льда, Δ S 2.
3. Нагревание жидкой воды от 0°С до 100 °С, Δ S 3.
4. Испарение воды, Δ S 4.
5. Нагревание пара от 100 °С до 120 °С, Δ S 5.
Изменение энтропии в 1, 3, 5 стадиях рассчитывают по уравнению
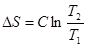 .
.
В стадиях 2, 4 – по уравнению 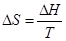 .
.
Общее изменение энтропии составит: 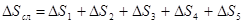 .
.
 2015-02-04
2015-02-04 393
393








