Процесс без обмена теплотой с окружающей средой называется адиабатическим. Он может происходить, если газ (или другое тело) окружен абсолютно не проводящей тепло оболочкой или процесс происходит очень быстро, так что газ не успевает обменяться теплом с другими телами.
При таких процессах первое начало термодинамики упрощается:
δQ = 0; dU = – δА. (32).
Это означает, что если над газом производить работу ( δ А < 0), то dU > 0. Внутренняя энергия газа возрастает, он нагревается. Если же газ расширяется, то он сам производит работу δ А > 0 за счет собственной внутренней энергии и dU < 0. В результате он охлаждается.
Согласно (25): dU =ν · CV · dT. Дляδ А используем соотношение (20). Тогда выражение (32) для адиабатического процесса можно записать так:
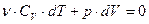 (33).
(33).
Подставим сюда р из уравнения Клапейрона-Менделеева (4) иполучим:
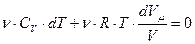 ;
; 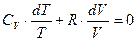 (34).
(34).
Проинтегрируем последнее выражение для пределов изменения переменных от T 1 до T 2 и от V 1 до V 2 и введя обозначение 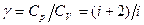 (35). получим:
(35). получим: 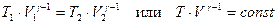 (36),
(36),
а используя Т = p·V/(ν·R), получаем 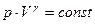 (37).
(37).
Соотношения (36-37) носят название уравнений Пуассона или адиабаты. γ – показатель адиабаты.
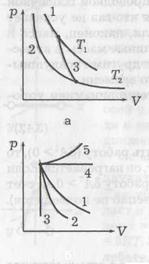 Поскольку γ > 1, давление в (37) обратно пропорционально не V, как было при изотермическом процессе, а Vγ, т. е. давление убывает с увеличением объема быстрее. На рисунке a кривые 1 и 2 – изотермы (Т 2 < T 1), а кривая 3 – адиабата.
Поскольку γ > 1, давление в (37) обратно пропорционально не V, как было при изотермическом процессе, а Vγ, т. е. давление убывает с увеличением объема быстрее. На рисунке a кривые 1 и 2 – изотермы (Т 2 < T 1), а кривая 3 – адиабата.
При любых других процессах (неизотермических и неадиабатических) всегда можно связь между р и V написать в виде (37), но γ уже не будет равна Ср/СV.
В этих случаях процесс называется политропическим, а γ – показателем политропы.
Можно сказать, что для изотермического (T =const) процесса γ = 1, для изобарического (р = const) γ = 0, для изохорического (V = const) γ = ∞. На рисунке б показаны различные процессы расширения газа: 1 – изотерма, 2 – адиабата, 3 – изохора, 4 – изобара, 5 – политропа. Процессы 2, 3 идут с охлаждением, а 4, 5 – с нагреванием газа.
 2015-02-04
2015-02-04 1006
1006








