Давление пара, при котором в условиях определенной температуры наступает динамическое равновесие, характеризующееся равенством скоростей испарения и конденсации жидкости, называется давлением насыщенного пара.
В 1886 году Рауль установил, что
относительное понижение давления пара растворителя над раствором равно мольной доле растворенного вещества, т.е. отношению количества молей растворенного вещества к суммарному количеству молей растворенного вещества и растворителя (I закон Рауля):
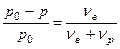 ,
,
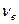 – число молей растворенного вещества
– число молей растворенного вещества
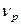 – число молей растворителя
– число молей растворителя
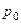 – давление насыщенного пара над чистым растворителем
– давление насыщенного пара над чистым растворителем
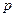 – давление насыщенного пара над раствором.
– давление насыщенного пара над раствором.
Закон Рауля, как и закон Вант-Гоффа, справедлив только для идеальных растворов, причем имеется в виду, что растворяемое вещество значительно менее летуче, чем растворитель (температура кипения его по меньшей мере на 150–200° должна быть ниже, чем температура кипения растворителя).
 2015-02-04
2015-02-04 843
843








