Энтропия S системы может быть определена интегрированием (9.36) с точностью до постоянной S0: 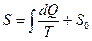 . Значение S0 не может быть установлено на основе первого и второго начал термодинамики. Эту задачу решает теорема Нернста (1906 г.), которую называют также третьим началом термодинамики. Существует несколько формулировок теоремы, которые эквивалентны между собой. Приведём две из них.
. Значение S0 не может быть установлено на основе первого и второго начал термодинамики. Эту задачу решает теорема Нернста (1906 г.), которую называют также третьим началом термодинамики. Существует несколько формулировок теоремы, которые эквивалентны между собой. Приведём две из них.
1. Формулировка Нернста. Все процессы при абсолютном нуле (Т=0), при которых система переходи из одного равновесного состояния в другое, происходят без изменения энтропии:
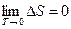 .
.
2. Формулировка Планка. При Т=0 система находится в основном состоянии, для которого термодинамическая вероятность Р=1, и следовательно, S=0, т.е. при стремлении абсолютной температуры тел к нулю энтропия тел обращается в нуль:
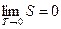 .
.
Абсолютному нулю соответствует единственно возможное состояние системы, в которое она переходит независимо от того, в каких состояниях она находилась при более высоких температурах.
Из теоремы Нернста следует, что невозможен такой термодинамический процесс, который приводил бы к охлаждению системы до температуры Т=0 (принцип невозможности достижения температуры абсолютного нуля).
 2015-02-04
2015-02-04 417
417








