1. Оксидоредуктазы. Катализируют окислительно-восстановительные реакции. Общая схема их действий может быть представлена следующим образом:

 A∙2H + B А + B ∙2H
A∙2H + B А + B ∙2H
 донор акцептор донор акцептор
донор акцептор донор акцептор
(red) (ox) (ox) (red)
«red» – восстановленный;
«ox» – окисленный.
Окисление протекает как процесс отнятия атомов H (электронов) от субстрата (А), а восстановление – как присоединение атомов H (электронов) к акцептору (В).
Характерной особенностью деятельности оксидоредуктаз в живой клетке является их способность образовывать цепи о-в (ox- red) ферментов, в которых осуществляется многоступенчатый перенос атомов водорода или электронов от первичного субстрата к конечному акцептору, которым является, как правило, кислород, так что в результате образуется вода.
Различают следующие основные группы оксидоредуктаз:
– анаэробные дегидрогеназы (ускоряют перенос атомов водорода на промежуточный акцептор, но не на кислород; в тех случаях, когда донор водорода точно не установлен, используют термин редуктаза);
– аэробные дегидрогеназы (ускоряют перенос атомов водорода непосредственно на кислород – оксидазы);
– реакции прямого присоединения молекулярного кислорода к субстрату катализируются оксигеназами.
Оксидоредуктазы подразделяются на 17 подклассов в зависимости от природы доноров атомов водорода, т.е. окисляемых субстратов.
Если акцепторами атомов водорода служат окисленные коферменты НАД+, НАДФ+ и ФАД, то различают, в зависимости от природы субстратов – доноров атомов водорода, следующие подклассы анаэробных дегидрогеназ:
1.1. \ 1.2.\ // O 1.3. – CH2 – CH2 –
CH – OH C = O или – C
/ / \ Н
1.4. – CH – NH2 1.5. – C = NH.
| |
– Если акцептором атомов водорода в группе аэробных дегидрогеназ служит молекулярный кислород, то такие ферменты называют оксидазами подкласс 1.1.3. Общая схема их действия следующая:

 A∙2H + O2 A + H2O2
A∙2H + O2 A + H2O2
донор акцептор донор акцептор
(red) (ox) (ox) (red)
– Если донором атомов водорода служат восстановленные коферменты НАДФН, НАДН, то ферменты из группы анаэробных дегидрогеназ относятся к подклассу 1.6.
– Если акцептором атомов водорода в группе аэробных дегидрогеназ служит пероксид водорода, то такие ферменты называют пероксидазами относятся к подклассу 1.11. Общая схема их действия может быть представлена следующим образом:


 A ∙ 2H + H2O2 A + 2H2O
A ∙ 2H + H2O2 A + 2H2O
донор акцептор донор акцептор
(red) (ox) (ox) (red)
– Оксидоредуктазы, катализирующие реакции прямого включения двух атомов кислорода в окисляемый субстрат (донор атомов водорода), т.е. диоксигеназы относятся к подклассу 1.13. Общая схема их действия может быть представлена следующим образом:

A ∙ 2H + O2 → A(OH)2
Оксидоредуктазы, катализирующие включение одного атома кислорода в два окисляемых субстрата, т.е. монооксигеназы (или гидроксилазы) относятся к подклассу 1.14. Общая схема их действия может быть представлена следующим образом:

 A ∙ 2H + O2 + НАДН…Н+ A–OH + НАД+ + H2O
A ∙ 2H + O2 + НАДН…Н+ A–OH + НАД+ + H2O
донор акцептор донор донор донор акцептор
(red) (ox) (red) (ox) (ox) (red)
2. Трансферазы. Катализируют перенос группы с одной молекулы на другую. Общая схема их действия может быть представлена следующим образом:


 А – В + С А + С – В
А – В + С А + С – В
Деление на подклассы в классе трансфераз основано на химической природе переносимых групп:
2.1. Переносят одноуглеродные остатки (С1 – фрагменты): // О
– СН3 (метил), – СН2ОН (гидроксиметил), – СОО– (карбоксил), – С
(формил). \ Н
2.2. Переносят С2 и С3 – фрагменты (альдегидные или кетонные остатки):
CH2OH гидроксиацетил CH2OH дигидроксипропионил
| (гликоальдегидная | (группа дигидрокси-
C=O группа) C=O ацетона)
| |
CHOH
|
2.3. Ацилтрансферазы (донор – ацил – КоА) – переносят остатки карбоновых кислот: CH3CO – (ацетил) и др.
2.4. Гликозилтрансферазы – переносят гликозильные остатки моносахаридов (гексоз и пентоз).
2.5. Алкил- и арилтрансферазы – переносят алкильные (кроме – СН3) и арильные группы.
2.6. Аминотрансферазы (трансаминазы) – переносят аминогруппу (– NH2).
2.7. Фосфотрансферазы (киназы) – переносят фосфорсодержщие группы.
3. Гидролазы. Катализируют реакции расщепления органических соединений при участии воды (гидролиз). Общая схема их действия может быть представлена следующим образом:


 А – В + HOH А –H + B – OH
А – В + HOH А –H + B – OH
Деление на подклассы в классе гидролаз основано на природе связи, подвергающейся гидролизу:
3.1. Эстеразы – гидролизуют сложноэфирные связи в эфирах карбоновых кислот и эфирах фосфорной кислоты (фосфатазы):
R – CO – O – R′ и OH
R – O – P = O
OH
3.2. Гликозидазы – гидролизуют гликозидные связи (например, в углеводах связи между остатками олиго- и полисахаридах):
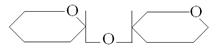
3.3. Гидролизуют простые эфирные связи: R – O – R′.
3.4. Пепетидгидролазы (пептидазы) – гидролизуют пептидные связи:
– CO – NH –.
3.5. Амидазы – гидролизуют амидные связи, отличные от пептидных:
O O
– C, – C
NH2 NHR′.
4. Лиазы (синтазы). Катализируют расщепление или образование химических соединений, при этом образуются или исчезают двойные связи без участия окислителя или воды. Общая схема их действия может быть представлена следующим образом:


 А + В А – В
А + В А – В
Деление на подклассы в классе лиаз основано на природе образуемой или расщепляемой связи:
4.1. С – С – лиазы – образуют или расщепляют связи углерод – углерод:
декарбоксилазы R – C – COOH, альдегид-лиазы H2NCHCOOH.
|| |
O CH2OH
4.2. С – О-лиазы – образуют или расщепляют связи углерод – кислород (гидролиазы: гидратазы и дегидратазы).
4.3. C – N-лиазы – образуют и расщепляют связи углерод – азот (аммиак-лиазы).
5. Изомеразы. Катализируют превращения в пределах одной молекулы без изменения общей формулы. Общая схема их действия может быть представлена следующим образом:


 АВ ВА
АВ ВА
Деление на подклассы в классе изомераз основано на типе изомеризации:
5.1. Рацемазы или эпимеразы – катализируют изменение пространственного расположения атомных группировок, связанных с асимметрическим атомом углерода (оптическая стереометрия).
5.2. цис-транс-Изомеразы – катализируют превращение одного из геометрических изомеров.
5.3. Внутримолекулярные оксидоредуктазы – катализируют:
 – взаимопревращения альдоз и кетоз:
– взаимопревращения альдоз и кетоз:


 O CHOH CH2OH
O CHOH CH2OH




 C || |
C || |
 | H C – OH C = O
| H C – OH C = O
CHOH | |
|
– взаимопревращение кетонных и енольных групп (кето-енольная таутомерия):
 CH3 CH2
CH3 CH2
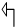
 | ||
| ||
 C = O C – OH
C = O C – OH
| |
– перемещение С = С связей.
5.4. Внутримолекулярные трансферазы (мутазы) – катализируют перенос группы внутри молекулы (фосфатной, ацильной групп).
 6. Лигазы (синтетазы). Катализируют энергозависимые реакции синтеза, их действие сопряжено с гидролизом АТФ (аденозинтрифосфорная кислота). Общая схема их действия может быть представлена следующим образом:
6. Лигазы (синтетазы). Катализируют энергозависимые реакции синтеза, их действие сопряжено с гидролизом АТФ (аденозинтрифосфорная кислота). Общая схема их действия может быть представлена следующим образом:
• A + B + АТФ → A – B + АМФ + H3PO4;
• A + B + АТФ → А – В + АМФ + H4P2O7
Деление на подклассы в классе синтетаз основано на типе образующейся связи:
6.1. Образуют С–О–связи; O
||
6.2. Образуют С–S–связи: – C – SKoA;
6.3. Образуют C–N–связи: – C – NH2 , – C – NHR.
|| ||
O O
6.4. Образуют С–С-связи (карбоксилазы).
 2015-02-04
2015-02-04 1490
1490








