Реактивы и материалы: бензол; серная кислота (d = 1,84 г/см3). Оборудование: водяная баня.
В пробирку помещают 3 капли бензола и 5 капель концентрированной серной кислоты. Содержимое пробирки нагревают в кипящей водяной бане при постоянном взбалтывании реакционной смеси. После получения однородного раствора выливают сульфомассу в пробирку с 10 каплями холодной воды.
Если сульфирование закончено полностью, образуется прозрачный раствор, так как сульфокислоты растворимы в воде.
Химизм процесса:
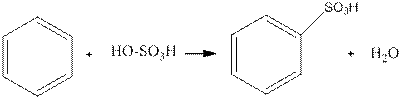
Легкость сульфирования при действии серной кислоты так же характерна для ароматических соединений, как способность к нитрованию. Реакция сульфирования, вотличие от реакций галогенирования и нитрования, обратима.
Сульфирующими агентами являются S03 и бисульфониевый ион HSO3+, образующиеся в результате реакции молекул серной кислоты между собой:
2H2SO4 → SO3 + H3O+ + HSO4-
Это сильные электрофильные реагенты с недостатком электронов у атома серы (смещение электронной плотности к кислороду). При взаимодействии с ароматическим ядром образуется промежуточный карбониевый бензол сульфокислота H-Ar+-SO3-, отщепляющий с одинаковыми скоростями SO3- или Н+. Чтобы полностью использовать серную кислоту, реакцию сульфирования ведут в избытке бензола при нагревании.
 2015-02-14
2015-02-14 5361
5361








