Все сказанное о равновесии между жидкостью и газом справедливо и для системы твердое тело — газ. Каждой температуре соответствует определенное значение давления, при котором устанавливается подвижное равновесие между твердым телом и газом. Для многих тел, таких, например, как твердые металлы, это давление при обычных температурах настолько мало, что не может быть обнаружено самыми чувствительными приборами.
Переход кристаллического тела в жидкое состояние происходит при определенной для каждого вещества температуре и требует затраты некоторого количества тепла, называемого теплотой плавления.
Если веществу, первоначально находившемуся в кристаллическом состоянии, сообщать каждую секунду одно и то же количество тепла, то изменение температуры тела со временем будет таким, как показано на рис. 45. Вначале температура тела все время растет. По достижении температуры плавления Тпл (точка 1 на рис. 45), несмотря на то, что к телу по-прежнему продолжает подводиться тепло, температура его перестает изменяться. Одновременно начинается процесс плавления твердого тела, в ходе которого все новые и новые порции вещества превращаются в жидкость. После того как процесс плавления будет закончен и все вещество полностью перейдет в жидкое состояние (точка 2на рис. 45), температура снова начнет повышаться.
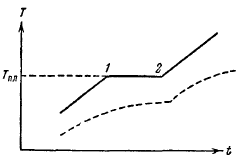
Рис. 45. Кривые плавления для кристаллического и аморфного тел
Кривая нагревания аморфного тела выглядит иначе (см. пунктирную кривую на рис. 45). При равномерном подводе тепла температура аморфного тела непрерывно растет. Для аморфных тел нет определенной температуры перехода в жидкое состояние. Этот переход совершается непрерывно, а не скачком. Можно лишь указать интервал температур, в пределах которого происходит размягчение тела. Это объясняется тем, что жидкости и аморфные тела отличаются лишь степенью подвижности молекул, — аморфные тела, как уже отмечалось, представляют собой сильно переохлажденные жидкости.
Температура плавления зависит от давления. Таким образом, переход из кристаллического в жидкое состояние происходит при вполне определенных условиях, характеризуемых значениями давления и температуры. Совокупности этих значений соответствует кривая на диаграмме (р,Т), которую принято называть кривой плавления. Кривая плавления идет очень круто. Для того, например, чтобы изменить на 1° температуру таяния льда, необходимо изменить давление на 132 ат.
Обратный плавлению процесс кристаллизации протекает следующим образом. При охлаждении жидкости до температуры, при которой твердая и жидкая фазы могут находиться в равновесии при данном давлении (т. е. до той же температуры, при которой происходило плавление), начинается одновременный рост кристалликов вокруг так называемых зародышей или центров кристаллизации. Разрастаясь все более, отдельные кристаллики в конце концов смыкаются друг с другом, образуя поликристаллическое твердое тело.
Центрами кристаллизации могут служить взвешенные в жидкости твердые частицы. Тщательно очищенную от таких частиц жидкость можно охладить ниже температуры кристаллизации без того, чтобы началось образование кристалликов. Состояние такой переохлажденной жидкости является метастабильным. Обычно достаточно попасть в такую жидкость пылинке, для того чтобы она распалась на жидкость и кристаллы, находящиеся при равновесной температуре. Однако в некоторых случаях при больших переохлаждениях подвижность молекул жидкости оказывается столь незначительной, что метастабильное состояние может сохраняться очень долго. Жидкость в таких случаях обладает весьма малой текучестью и представляет собой аморфное твердое тело.
Процесс кристаллизации сопровождается выделением такого же количества тепла, какое поглощается при плавлении.
 2015-02-15
2015-02-15 1698
1698
