Задача 1. Как изменится скорость химической реакции А(газ) + 2В(газ) ® С(газ) при повышении концентрации вещества А в 2 раза, давления в 2 раза.
Согласно закону действующих масс, скорость реакции можно выразить по формуле V1 = k[A].[B]2
а) если повысить концентрацию А в 2 раза, то скорость будет равна V2 = k[2A].[B]2 = 2V1. Скорость увеличится в 2 раза;
б) если повысить давление, то для газообразных веществ это равносильно повышению концентрации каждого из реагирующих веществ в 2 раза: V3 = k[2A].[2B]2 = 8k[A].[B]2 = 8V1. Скорость увеличится в 8 раз.
Задача 2. Скорость некоторой реакции при 0 0С равна 1 моль/л. час. Температурный коэффициент реакции равен 3. Какой будет скорость данной реакции при 30 0С.
Решение: По правилу Вант-Гоффа V2 = V1. 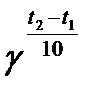 = 1.33 = 27 моль/л .час
= 1.33 = 27 моль/л .час
 2015-03-07
2015-03-07 466
466








