Теплоемкостью тела называется количество теплоты, которое надо сообщить телу, чтобы изменить его температуру на 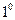 .
.
Существуют понятия удельной теплоемкости (когда нагревается тело массой 1кг) и молярной теплоемкости (когда нагревается вещество в количестве одного моля).
Воспользуемся первым законом термодинамики:
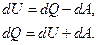
Согласно введенному определению:
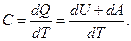
Различают 2 случая:
1) 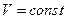 .
.
Учитывая 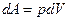 :
:
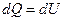 .
.
Тогда
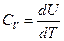 ,
,
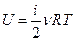 , где
, где 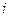 - число степеней свободы.
- число степеней свободы.
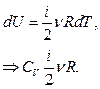
Если речь идет о молярной теплоемкости:
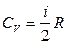 .
.
2) 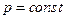 .
.
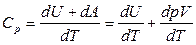 .
.
Воспользуемся уравнением Менделеева(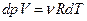 ):
):
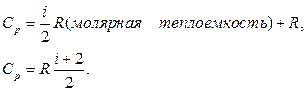
Следовательно, 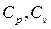 не зависят от температуры у идеальных газов.
не зависят от температуры у идеальных газов.
Для реальных одноатомных газов это почти так (например, 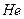 ).
).
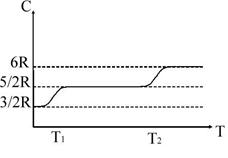 А вот для двухатомных газов (например,
А вот для двухатомных газов (например, 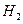 )
)
в достаточно большом интервале температур газ действительно не зависит от 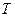 . Однако, при более низких либо достаточно высоких происходит изменения теплоемкости.
. Однако, при более низких либо достаточно высоких происходит изменения теплоемкости.
Объяснить эти явления в рамках классической физики оказалось невозможным.
 2015-03-27
2015-03-27 415
415








