Введение: Самая жестокая и беспощадная тема этого модуля. Для начала нужно вспомнить, что в прошлом году вы якобы научились оперировать с органическими веществами – спиртами, аминами, карбоновыми кислотами, при условии, что 1 молекула содержит только одну из этих групп. Теперь вас ждет усложнение. Одна молекула может содержать несколько функциональных групп: спирт + карбоновая кислота (называется гидроксикислота), амин + карбоновая кислота (аминокислота), кетон + карбоновая кислота (кетокислота), аминоспирт, многоатомный спирт, иминокислота… Это создает возможность для существования более 9000 всяческих разнообразных органических веществ – поли- и гетерофункциональных соединений. Так сложилось, что эти вещества встречаются не только в книжках, но и в организме человека, им присвоены зачастую очень странные названия типа холин, винная кислота, дигидроксиацетон и прочее. Понять эти названия логикой нельзя. Они формируют своей массой огромный список, который вы, дорогие мои любители химии, должны хотя бы иметь под рукой. Вы можете найти его в приложении 2.
В теме описано несколько видов реакций, которые могут быть совершены над этими веществами. Эти типы надо осмыслить безотносительно того, в каком виде вопросов они будут встречаться, и понимать, что-откуда-куда и зачем. Многим из вас предстоит после тестов еще и письменная часть, а там есть все то же самое. Итак:
1) Алкилирование
Общие сведения: присоединение к субстрату алкильного радикала (СН3, С2Н5 …)
Субстрат: содержит любой N, в том числе гетероциклы с азотом, кроме амида, или, что бывает намного реже, субстрат - спирт.
Реагент: галогеналкан (CH3-I, C2H5-Cl, …) или триалкилсульфониевая соль [(CH3)3S+]Cl-. Есть более жесткие варианты, но встречаются редко, поэтому мы их не описываем.
Алгоритм: словами – радикал от галогена присоединяем к атому азота, полученную конструкцию закрываем квадратными скобками. От азота ничего удалять не надо.
В формуле - RNH2 + Rr-Cl = [RNH2-Rr] Cl
Продукт: соль аммония.
Пример: НОСН2СН2NH2 + C2H5- Cl = [НОСН2СН2NH2 -C2H5 ] Cl
коламин N-этил коламин гидрохлорид
2) Ацилирование
Общие сведения: присоединение к субстрату ацетильного фрагмента СН3-С(О)-
Субстрат: амин (более предпочтительно) или спирт.
Реагент: ацетилкофермент А (СН3-С(О)-SKoA) или ацетилфосфат (CH3-C(O)-OPO3H2)
Алгоритм: словами – от атомов N или О убираем 1 Н и добавляем вместо него -СО-СН3.
В формулах - RNH 2 + СН3-С(О) -SKoA = RNH - C(O)-CH3 + HSKoA для амина
RO H + CH3-C(O) -OPO3H2 = RO - C(O)-CH3 + H3PO4 для спирта
Продукт: амид или сложный эфир, принято еще говорить ацетил-какая-нибудь хрень.
Пример: НОСН2СН2NH2 + СН3-С(О)- SKoA = НОСН2СН2NH -С(О)-СН3 + HSKoA
коламин N-ацетил коламин
заметьте, что в примере субстрат содержал две группы, способные ацилироваться, спирт и амин, и ацилирование прошло по амину, потому что он более сильный нуклеофил так надо.
3) Гидролиз
Общие сведения: сложная реакция, разделение больших молекул на маленькие под действием воды.
Субстрат: сложный эфир, амид или имин.
Реагент: Н2О
Алгоритм: словами для сложного эфира – он делится на карбоновую кислоту и спирт
Формулой – Х- С(О)-О -У + Н2О → Х- СООН + У- ОН
Словами для амида – он делится на карбоновую кислоту и амин,
Формулой – Х- С(О)-NH -У + Н2О → Х- СООН + У- NH2
Словами для имина – он делится на альдегид (кетон) и амин.
Формулой – Х- СН=N- У + Н2О → Х- СН=О + У- NH2
Тут нужно остановиться и сделать замечание. Говоря вот так, абстрактно, все вроде бы несложно. Но если попадутся огромные формулы, типа вот такой
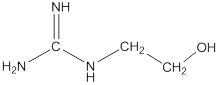 |
сразу и не поймешь, что от тебя хотят. Чтобы избежать подобных epic fail-ов, нужно очень четко помнить, как выглядит амин, амид, имин, сложный эфир и тому подобные непотребства. Учите, или хотя бы имейте под рукой список существующих функциональных групп, а главное – научитесь их узнавать в больших молекулах. Видите имин в формуле выше? В сложных молекулах, как правило, содержится несколько групп, способных гидролизоваться. Поэтому задача – найти их все, разделить сложное вещество на части и преобразовать группы. Ну, например, если в веществе есть только сложноэфирная группа, оно делится на две части, на кислоту и спирт. А если в веществе есть и сложноэфирная, и амидная группа, то оно делится на три части, например аминоспирт и две карбоновые кислоты (см. пример).
Продукт: см. раньше.
Пример: СН3- С(О)-О -СН2СН2- NН-С(О) -СН3 + 2 Н2О → 2 СН3 СООН + НО СН2СН2 NH2
Обратите внимание, что в примере слева – сложный эфир С(О)-О, а справа – амид С(О)-N, и оба гидролизуются.
4) Декарбокслирование
Общие сведения: удаление из молекулы группы СОО в виде СО2
Субстрат: карбоновая кислота -СООН или кетокарбоновая кислота -С(О)-СООН
Реагент: нет.
Алгоритм: есть просто декарбоксилирование и окислительное декарбоксилирование.
Простое декарбоксилирование: R- COO H → RH + CO2
Окислительное декарбоксилирование: R- C(O) - COO H + ½ O 2 → R- COO H + CO2
Продукт: зависит от ситуации.
Пример:
HS-CH2-CH(NH2)- COO H → HS-CH2-CH2(NH2) + CO2 простое декарбоксилированние
СН3-С(О)- СОО Н → СН3-СООН + СО2 окислительное декарбоксилирование
5) Таутомерия
Общие сведения: обратимый внутримолекулярный перенос Н и двойной связи.
Субстрат: кетон-енол, имин-енамин, лактам (циклический амид)-лактим, гидроксиальдегид-циклический полуацеталь. Енол – это вещество, содержащее -СН=С-ОН, а енамин –СН=С-NH2. Кетон, имин, гидроксиальдегид, амид – сами знаете, лактам и циклический полуацеталь – есть чуть дальше.
Реагент: нет
Алгоритм: словами – двойная связь перекидывается на место одинарной, Н перекидывается на место двойной связи. Бывает по группам кето-енольная, енамин-имнная, лактим-лактамная и циклооксотаутомерия (для гидроксиальдегидов, подробнее в разделе углеводы). Не особо понятно получилось. Формулами –
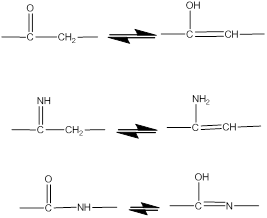 |
Продукт: поскольку реакция обратима, то при исходном кетоне получится енол и наоборот. И так далее.
Пример: СН3-С(=О)-СН2-СООН ↔ СН3-С(-ОН)=СН-СООН
6) Циклизация
Общие сведения: образование циклических замкнутых молекул из линейных с концевыми группами.
Субстрат: Гидроксикислота, аминокислота, гидроксиальдегид.
Реагент: нет
Алгоритм: Словами – концевые группы соединяются друг с другом. При циклизации гидроксикислоты получается лактон, при циклизации аминокислоты – лактам, при циклизации гидроксиальдегида – циклический полуацеталь.
Формулой –
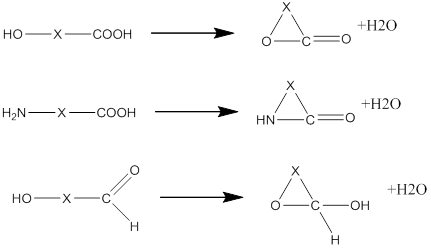 |
Продукт: в первом случае – лактон, во втором – лактам, в третьем – циклический полуацеталь. Обратите внимание на эти названия, научитесь отличать друг от друга. Весьма часто встречаются эти вопросы, где нужно их просто узнать.
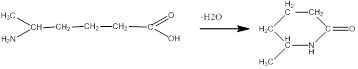 Пример:
Пример:
Узнать ее в тесте, если она уже написана – это один вопрос, и это легко. А вот если эта реакция попадется вам в письменной части (если она у вас будет) и вам нужно будет написать ее самим – это уже совсем другой вопрос, и уже не такой легкий. Рекомендации по этому делу: Предварительно записываем формулу максимально развернуто. Никаких (СН2)3, только –СН2–СН2–СН2–. Оцениваем, какие есть группы, отрывам, в случае гидроксикислоты или аминокислоты Н-ОН и связываем группы друг с другом. У вас получится что то вот такое
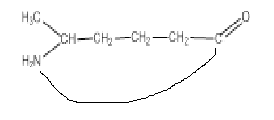
Получилось, как видите, довольно убого и колхозно, но зато правильно передает суть – образование циклической молекулы. Конечно, вам хочется эстетики, душа требует прекрасного. Тогда надо перестроить в цикл. Считаем, сколько атомов С вошло в цикл, к ним прибавляем О или NН, замыкающий цикл, при этом ответвления, типа СН3, в цикл входить не должны. В примере в цикл входит 5 С, NH цикл – итого нужен 6-угольник Строим геометрическую фигурку, это может быть только 5-ти или 6-угольник, иное невозможно. Расставляем С, которые есть в колхозной форме, по углам фигурки. Если ниче не понятно – ограничьтесь колхозной версией. Все описанные виды являются внутримоекулярной циклизацией. Существует еще межмолекулярная циклизация, она встречается редко, поэтому не описана.
7) Фосфорилирование
Общие сведения: введение в субстрат остатка фосфорной кислоты –РО3Н2
Субстрат: спирт
Реагент: АТФ
Алгоритм: словами - из ОН-группы спирта выкинуть Н и заменить его РО3Н2. Формулой
ROH + АТФ → RO-PO3H2 + АДФ
8) Хелатообразование
Общие сведения: Жесть. Образование бабочкообразных молекул. Судя по тестам, к счастью не встречается.
Субстрат: многоатомные спирты, аминоспирты, диамины, аминокислоты, гидроксикислоты.
Реагент: Сu(OH)2
Алгоритм: неописуемо
Продукт: хелатный комплекс.
Пример: неописуемо.
9) Элиминирование
Общие сведения: отрыв групп ОН, SH, NH2 в виде Н2О, Н2S, NH3.
Субстрат: спирт, тиол, амин.
Реагент: нет.
Алгоритм: словами - из спирта/тиола/амина выкидываем соответствующую группу и вместе с ней еще один Н от соседнего по отношению к группе атома С, между двумя атомами С, от которых ушли Н и группа вставляем двойную связь. Частный случай – отрыв воды – называется дегидратацией.
Формулой НО-СН-СН2- → -СН=СН- + Н2О
HS-CH-CH2- → -CH=CH- + H2S
H2N-CH-CH2- → -CH=CH- + NH3
Надо учесть, что спирт и тиол отрываются легче, чем амин. Еще нужно иметь в виду правило Зайцева – водород отрывается от менее гидрированного атома С.
Продукт: алкен.
Пример: СН3-СН(ОН)-С Н 2-СООН → СН3-СН=СН-СООН + Н2О
Пример как раз показывает это правило, Н отрывается не справа от ОН, не там, где СН3, а там, где СН2. Не нужно пытаться оторвать Н от СН, на том основании, что он еще менее гидрированный. Тогда двойную связь вставлять будет некуда. Все же Н и группа отрываются обязательно от двух разных атомов.
10) Дезаминирование
Общие сведения: удаление аминогруппы, замена ее ОН.
Субстрат: NH2
Реагент: HNO2
Алгоритм: Словами: заменяем аминогруппу на спиртовую группу.
Формулой RNH2 + HNO2 → ROH + N2 + H2O
Продукт: спирт
Пример: NH2- (CH2)4-CH(NH2)-COOH + HNO2 → HO- (CH2)4-CH (OH) -COOH + 2N2 + H2O
Типичные вопросы:
1. Истинность утверждений
Пример:
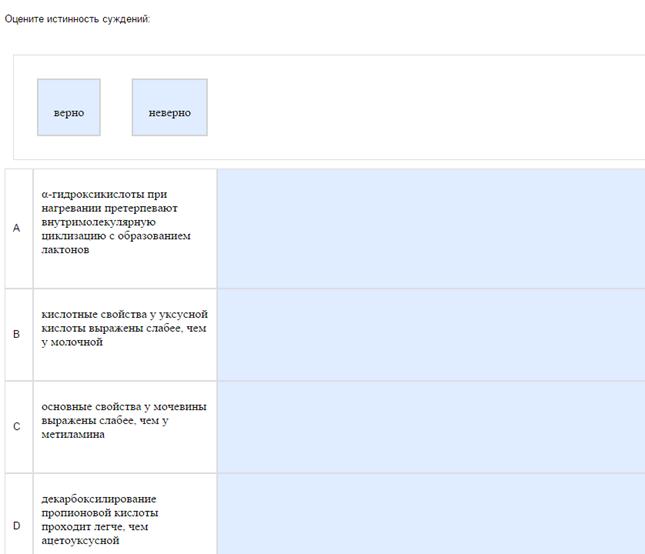
бляяяяяяяя…
Как с этим бороться:
Никак, смиритесь, вам это не дано. Обычно там бывает лютая хрень, которую и я, и даже сами авторы, вероятно, не всегда понимают. Почитайте описание реакций, иногда удается что то вытащить оттуда. Кислотные свойства гетерофункциональных кислот (молочная) сильнее, чем у монофункциональных (уксусная), а основные свойства у гетерофункциональных аминов (мочевина) наоборот, слабее моноаминов (метиламин). Декарбоксилирование гетерофункциональных карбоновых кислот (ацетоусусная) протекает легче, чем монофункциональных (та же уксусная).
2. Название по формуле.
Пример:

Простейший случай, кротоновая кислота.
Как с этим бороться:
Посмотреть приложение в конце методички, там должно быть море формул.
3. Тип реакции.
Пример:
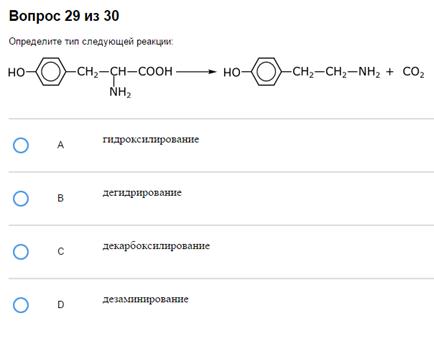
Декарбоксилирование.
Как с этим бороться:
Внимательно прочитать описание типов реакций. Обычно каждый тип узнается по какой то характерной детали. Многие типы – по реагенту, например гидролиз Н2О, ацилирование - ацетилКоА. Реакции без реагента можно узнать по «маленькому» продукту. Декарбоксилирование – СО2, Элиминирование – Н2О… Общий надежный признак – характер изменения субстрата.
4. Класс соединений.
Пример:

Ну хотя бы группы вы выучили? Кислота + амин...
Как с этим бороться:
Выучить группы и уметь их определять «на местности».
5. Гидролиз.
Пример:

Бляяяяяяя…
Как с этим бороться:
Это тяжелые вопросы. В общем, порядок такой. Находим все гидролитически неустойчивые группы, их, как правило, много. «Разрезаем» молекулу по каждой гидролизуемой группе. После гидролиза из сложного эфира получается кислота и спирт, из амида – …, и т.д. Соответственно, устанавливаем эти группы на подобающие им места, тут еще надо понять, где кислота, а где спиртовая группа должны быть. Но как то разобрались. Затем смотрим, нет ли в полученных продуктах гидродитически неустойчивых групп еще, иногда бывает и так. Если они остались – добиваем и их. Среда у вас может быть кислой или щелочной. В кислой среде (соляная кислота), если выделяется аммиак, то он будет как NH4Cl, амины как аммониевые соли (такая хрень в квадратных скобках и с хлором, как в примере), а если среда щелочная (гидроксид натрия) то в виде солей будут карбоновые кислоты (СООNa), фенолы и многоатомные спирты (ONa). Только времени на все эти операции вам не хватит.
6. Тип таутомерии.
Пример:

Кето-енольная.
Как с этим бороться:
Еще раз просмотрите общие сведения о реакции таутомерии. Общий принцип действует и тут. Если есть группа, способная к данному виду взаимодействий, в данном случае таутомерии, то оно возможно. Группа для таутомерии СН3-С=О, может участовавать в кето енольной таутомеризации.
7. Циклизация.
Пример:

Лактам.
Как с этим бороться:
Процитать описание циклизации. Научиться определять группы. При циклизации Гидроксикислот получаются лактоны, при циклизации аминокислот лактамы при циклизации гидроксиальдегидов – циклические полуацетали.
8. Карбоксилирование-декарбоксилирование и другие реакции + названия.
Пример:

А+Д.
Как с этим бороться:
Для корректного анализа вопросов такого типа нужно перевести все названия в формулы, иначе невозможно понять, чего от вас требуется. Все реакции проводят с формулами, ну не с названиями же их проводить. Применяем осознание видов реакций к конкретным молекулам. Ну, например, когда говорят о декарбоксилировании щавелевой кислоты, мы представляем щавелевую кислоту НООС-СООН, и представляем, что с ней проведено декарбоксилирование, то есть –СО2, остается Н-СООН. И затем смотрят, получили ли то, что хотели. Вопрос в примере, надо заметить, посвящен не только декарбоксилированию, но еще и ОВР. Так вот, представили себе ацетоуксусную кислоту. Представили, что из нее выкинули СО2, то есть декарбоксилировали. Получили ацетон? ААА!!! Не знаем, что такое ацтон!? Все. Не о чем говорить.
 2015-03-27
2015-03-27 4203
4203








