Реактивы:
1) 0,01н раствор KMnO4;
3) 0,01н раствор H2С2О4;
3) 4н раствор H2SO4.
Ход работы. В предварительно подготовленную коническую колбу на 250 мл отмерить 100 мл исследуемой воды, прилить 5 мл 4н раствора кислоты и прилить из бюретки точно 10 мл 0,01 раствора КМnО4. Колбу закрыть воронкой, смесь кипятить 10 мин. (считая с момента кипения). Затем снять с огня.
К горячей жидкости прилить с помощью мерного цилиндра 10 мл 0,01н раствора щавелевой кислоты. Перемешать до обесцвечивания. Горячий обесцвеченный раствор титровать 0,01н раствором KМnO4 до появления слаборозового окрашивания, не исчезающего 2 - 3 минуты. Рассчитать перманганатную окисляемость по формуле:
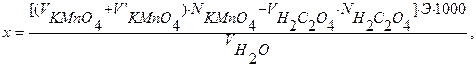 где х – окисляемость воды, мг О2 /л;
где х – окисляемость воды, мг О2 /л;
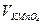 – объем раствора KMnO4, прилитого к пробе воды до кипячения, мл;
– объем раствора KMnO4, прилитого к пробе воды до кипячения, мл;
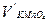 – объем раствора KMnO4, пошедший на титрование избытка щавелевой кислоты, мл;
– объем раствора KMnO4, пошедший на титрование избытка щавелевой кислоты, мл;
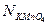 – нормальность раствора KMnO4, мг-экв/л;
– нормальность раствора KMnO4, мг-экв/л;
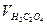 – объем 0,01н раствора щавелевой кислоты для связывания избытка KMnO4, мл;
– объем 0,01н раствора щавелевой кислоты для связывания избытка KMnO4, мл;
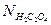 – нормальность раствора щавелевой кислоты, мг-экв/л;
– нормальность раствора щавелевой кислоты, мг-экв/л;
Э – эквивалент кислорода, (8);
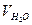 – объем пробы исследуемой воды, мл.
– объем пробы исследуемой воды, мл.
Вопросы к отчету лабораторной работы № 6
1) Что называют окисляемостью воды? Чем она обусловлена?
2) Что называют общей окисляемостью? Каким способом определяется общая окисляемость?
3) Что называют частичной окисляемостью? Каким способом определяется частичная окисляемость?
 2015-03-20
2015-03-20 2070
2070







